
- •Группа веществ, изолируемых минерализацией («металлические» яды)
- •Оглавление Введение
- •1. Изолирование соединений, содержащих «металлические» яды из биологического материала
- •1.1. Разрушение биологического материала азотной и серной кислотами
- •1.2. Разрушение биологического материала хлорной, азотной и серной кислотами
- •1.3. Разрушение биологического материала пергидролем и серной кислотой
- •1.4. Разрушение биологического материала методом сухого озоления
- •1. Дробный метод анализа минерализата
- •III. Изменение степени окисления ионов
- •V. Удаление катионов в виде осадка
- •2.1. Исследование осадка
- •Соединения Свинца Токсикологическое значение соединений свинца
- •Исследование минерализата на наличие ионов свинца. Малые количества осадка свинца сульфата (менее 2 мг)
- •Большие количества осадка свинца сульфата (свыше 2 мг)
- •2.1.2. Соединения бария Токсикологическое значение соединений бария
- •Исследование минерализата на наличие ионов бария
- •2.2. Исследование фильтрата
- •2.2.1. Соединения марганца Токсикологическое значение соединений марганца
- •Исследование минерализата на наличие ионов марганца
- •2.2.2. Соединения хрома Токсикологическое значение соединений хрома
- •Исследование минерализата на наличие ионов хрома
- •2.2.3. Соединения серебра Токсикологическое значение соединений серебра
- •Исследование минерализата на наличие ионов серебра
- •2.2.4. Соединения меди Токсикологическое значение соединений меди
- •Исследование минерализата на наличие ионов меди
- •2.2.5. Соединения сурьмы Токсикологическое значение соединений сурьмы
- •Исследование минерализата на наличие ионов сурьмы
- •2.2.6. Соединения таллия Токсикологическое значение соединений таллия
- •Исследование минерализата на наличие ионов таллия
- •2.2.7. Соединения мышьяка Токсикологическое значение соединений мышьяка
- •Исследование минерализата на наличие ионов мышьяка
- •2.2.8. Соединения висмута Токсикологическое значение соединений висмута
- •Исследование минерализата на присутствие ионов висмута
- •2.2.9. Соединения цинка Токсикологическое значение соединений цинка
- •Исследование минерализата на наличие ионов цинка.
- •2.2.10. Соединения кадмия Токсикологическое значение соединений кадмия
- •Исследование минерализата на наличие ионов кадмия
- •2.2.11. Соединения ртути Токсикологическое значение соединений ртути
- •Исследование биологического материала на наличие ионов ртути Изолирование ртути методом деструкции
- •3. Методы количественного определения «металлических» ядов в минерализате
- •3.1. Гравиметрический метод
- •3.2. Титриметрические (объемные) методы
- •3.3. Фотоколориметрический метод
- •3.4. Атомно-абсорбционная спектроскопия
- •Эмиссионный спектральный анализ
- •3.6. Рентгено-флуоресцентный метод
- •Вопросы для самоконтроля:
- •Выберите несколько правильных ответов:
- •Выберите правильный ответ
- •Литература
Исследование биологического материала на наличие ионов ртути Изолирование ртути методом деструкции
Для деструкции берут по 20 г измельченных органов (печень, почки) и подвергают деструкции отдельно. Биоматериал вносят в коническую колбу вместимостью 200 мл, в которую прибавляют 5 мл воды, 1 мл этилового спирта и 10 мл кислоты азотной концентрированной. Затем в колбу малыми порциями прибавляют 20 мл кислоты серной концентрированной с такой скоростью, чтобы окислы азота не выделялись из колбы. После окончания прибавления кислоты серной концентрированной колбу оставляют на 5—10 мин при комнатной температуре (до прекращения выделения оксидов азота). Затем колбу устанавливают на кипящую водяную баню и нагревают в течение 10—20 мин. Если после нагревания колбы на кипящей водяной бане останутся неразрушенными кусочки биологического материала, то их осторожно растирают стеклянной палочкой о стенки колбы. При бурном протекании реакции с выделением оксидов азота в колбу прибавляют 30— 50 мл горячей воды. Полученный горячий деструктат смешивают с двойным объемом кипящей воды и, не охлаждая, фильтруют через двойной увлажненный фильтр. Фильтр и остатки жира на нем 2—3 раза промывают горячей водой. Промывные воды присоединяют к деструктату. Полученную при этом жидкость собирают в колбу, содержащую 20 мл насыщенного раствора мочевины, предназначенной для денитрации деструктата. Затем деструктат охлаждают, доводят водой до определенного объема и исследуют его на наличие ртути.
Реакция с дитизоном. Половину деструктата вносят в делительную воронку, прибавляют 10 мл хлороформа и взбалтывают в течение 1 мин. Хлороформный слой, в который могут переходить различные примеси из деструктата, отбрасывают. Взбалтывание деструктата с новыми порциями хлороформа проводят до тех пор, пока не перестанет окрашиваться хлороформный слой. После этого к очищенному от примесей деструктату прибавляют 5 мл хлороформа, 0,3 мл 0,01 % раствора дитизона в хлороформе и взбалтывают. Появление желтой или оранжево-желтой окраски хлороформного слоя указывает на наличие ионов ртути в деструктате. При взбалтывании хлороформного слоя с 0,5 М раствором кислоты хлористоводородной окраска сохраняется (в отличие от серебра дитизоната).
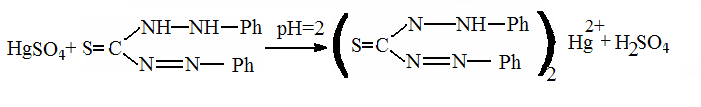
Реакция со взвесью меди иодида (I). К хлороформному раствору ртути дитизоната прибавляют 3 мл 0,25 % раствора йода в калия йодиде и энергично встряхивают. Реэкстракт отделяют от органической фазы, помещают в пробирку, добавляют насыщенный раствор йода до уравнивания окраски с контролем — 0,25 % раствором йода в калия йодиде. При добавлении 2 мл составного раствора (смесь меди сульфата, натрия сульфита и натрия бикарбоната в соотношении 1:2:1,5) образуется осадок, окрашиваемый в присутствии ионов ртути от розового до кирпично-красного цвета.
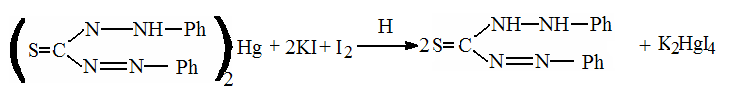
CuSO4 + 2KI CuI2 + K2SO4
2CuI2 2Cu+I2
2CuI + K2 HgI4 Cu2HgI4↓ + 2KI
Натрия сульфит прибавляют для того, чтобы выделившийся йод не маскировал окраску образующегося комплекса.
I2 + Na2SO3 + H2O 2 HI + Na2SO4
В результате реакции образуется йодистоводородная кислота, которая смещает значение рН, поэтому ее связывают натрия гидрокарбонатом.
HI + NaHCO3 NaI + СО2 + Н2О
В общем виде уравнение реакции можно записать следующим образом:
K2HgI4 + 2CuSO4 + 2KI + Na2SO3 + 2NaHCO3
Cu2HgI4↓+ Na2SO4 + 2K2SO4 + 2NaI + 2CO2 + H2O
