
Новиков Д.К. Медицинская микробиология
.pdf
ингибирует всасывание воды и активирует образование цАМФ, что приводит к стафилококковым диареям.
Энтеротоксины являются суперантигенами. Мишень их действия
– -субъединица рецептора Т-клетки. Энтеротоксины (A-F) ответственны за развитие пищевых интоксикаций. Тип А обладает рвотным действием, тип В – повреждает слизистую желудочно-кишечного тракта. Типы В и С также приводят к развитию синдрома токсического шока.
Гемолизины (4 типа) вызывают гемолиз эритроцитов: L-токсин ( -гемолизин) относится к порообразующим токсинам, который обладает цитолитическими свойствами в отношении различных типов клеток (моноцитов, лимфоцитов, эритроцитов, тромбоцитов и эндотелиоцитов). Различают три стадии повреждения клеточной мембраны под действием L-токсина: протомеры токсина связываются с мембраной клеток при помощи рецепторов и адсорбируются фосфотидилхолином или холестерином, которые входят в состав билипидного слоя мембраны, далее протомеры олигомеризуются в нелитический гептамерный комплекс, который претерпевает конформационные изменения, формируется «ножка», которая проникает через цитоплазматическую мембрану, образуется пора и происходит вход и выход небольших молекул и ионов, что ведет к набуханию и гибели клеток, имеющих ядро, и осмотическому лизису эритроцитов. Бета-гемолизины разрушают эритроциты человека, проявляют свойства холодовых гемолизинов (активны при низких температурах); гамма-лизин – двухкомпонентный гемолизин с умеренной активностью в отношении эритроцитов человека; дельта-гемолизины проявляют детергентные
свойства, оказывают цитотоксическое действие на различные клетки. Микрокапсула защищает бактерии от комплемент-зависимого
поглощения полиморфноядерными фагоцитами, способствует адгезии микроорганизмов и их распространению в тканях.
Компоненты клеточной стенки стимулируют развитие воспалительных реакций, усиливают синтез интерлейкина I макрофагами, активируют систему комплемента и являются мощными хемоаттрактантами для нейтрофилов. Белок А золотистого стафилококка связывается с Fc-фрагментом IgG и блокирует его.
Тейхоевые кислоты активируют систему комплемента по альтернативному пути, а также свертывающую и калликреин-кининовую системы, облегчают адгезию к эпителиальным клеткам, регулируют концентрацию катионов на клеточной мембране, связывают фибропептин.
К ферментам относят каталазу (защищает кокки от действия О2- зависимых микробицидных механизмов фагоцитов), -лактамазы (разрушают молекулы -лактамных антибиотиков), липазы облегчают
151
проникновение в ткани, плазмокоагулаза (существует в трех антигенных формах, активирует протромбин, что приводит к повышению свертываемости крови, препятствует фагоцитозу).
Гиалуронидаза способствует распространению стафилококков в тканях.
Лецитиназа разрушает лецитин, входящий в состав оболочек клеток, вызывает лейкопению. Фибринолизин, растворяя фибрин, способствует генерализации патологического процесса.
Экология и распространение стафилококков. Стафилококки колонизируют слизистые оболочки ротовой полости, носа, кишечника и кожу сразу после рождения. Они являются представителями нормальной микрофлоры тела человека.
Стафилококки присутствуют в окружающей среде везде. Этому способствует длительность выживания стафилококков на различных предметах. В связи с широким распространением стафилококков необходимо дифференцировать их виды, так как степень болезнетворной активности их различна.
Стафилококки хорошо переносят высушивание, пигмент хорошо защищает их от солнечных лучей. При комнатной температуре они остаются жизнеспособными на предметах ухода за больными в течение 50 дней, при температуре 70-80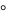 погибают через 20-30 минут. 1% раствор хлорамина убивает их через 2-5 минут, дезинфицирующие средства – за 15 минут (3% раствор фенола). Высокая чувствительность к бриллиантовой зелени, нитрофуранам позволяет широко применять эти препараты для лечения поверхностных гнойновоспалительных заболеваний.
погибают через 20-30 минут. 1% раствор хлорамина убивает их через 2-5 минут, дезинфицирующие средства – за 15 минут (3% раствор фенола). Высокая чувствительность к бриллиантовой зелени, нитрофуранам позволяет широко применять эти препараты для лечения поверхностных гнойновоспалительных заболеваний.
Роль стафилококков в патологии человека.
S.aureus вызывает (рис. 14):
1.Местные гнойно-воспалительные процессы кожи и подкожной клетчатки (пиодермии, фурункулы, карбункулы, абсцессы, флегмоны, маститы, травматические и послеоперационные нагноения ран).
2.Системные заболевания внутренних органов (бронхиты, пневмонии, ангины, фарингиты, отиты, синуситы, циститы, холециститы, менингиты, эндометриты).
3.Пищевые токсикоинфекции (отравления).
4.Септицемию и септикопиемию.
S.epidermidis занимает менее важную роль в патологии, но может быть причиной гнойно-воспалительных процессов у лиц пожилого возраста, конъюнктивитов новорожденных, послеоперационных эндокардитов.
S.saprophyticus – сапрофит, но при ослаблении иммунитета может вызывать воспалительные процессы, послеоперационные нагное-
152
ния ран. У этого вида стафилококка есть олигосахаридные рецепторы, способствующие прикреплению его к эпителию мочевыводящих путей.
В развитии стафилококковой инфекции большую роль играют инвазионные и токсигенные свойства микроорганизмов, состояние иммунной системы макроорганизма (иммунодефициты). Возбудитель проникает через поврежденную кожу и слизистые оболочки. В стационаре этому способствуют различные оперативные вмешательства, катеризация кровеносных сосудов, использование протезов сосудов, использование искусственных клапанов, использование различной диагностической аппаратуры.
Предрасполагающими факторами для развития эндогенной инфекции являются болезни, угнетающие иммунитет, диабет, почечная и печеночная недостаточность, прием иммунодепрессантов, цитостатических препаратов.
Иммунитет. Здоровые взрослые люди устойчивы к стафилококкам, что объясняется защитными механизмами и наличием специфических АТ. В иммунитете имеют значение все виды антител: антимикробные, антитоксические, антиферментные, степень их защиты определяется и титром АТ, и местом их действия. Антимикробные АТ на пептидогликан, протеин А способствуют фагоцитозу, препятствуют связыванию опсонинов, антитоксины нейтрализуют -токсин, антиферментные АТ – соответствующие ферменты; большую роль играют секреторные IgА, обеспечивающие местный иммунитет слизистых оболочек; АТ к тейхоевым кислотам определяются при остеомиелитах, сепсисе, эндокардитах.
Лабораторная диагностика
Материал для исследования – гной, кровь, мокрота, моча.
1.Бактериоскопический метод имеет ориентировочное значение. Выявляют грамположительные кокки, расположенные в виде гроздей, что позволяет выбрать необходимые питательные среды.
2.Бактериологический метод – выделение чистой культуры и ее идентификация. Материал засевают на МЖСА, ЖСА и кровяной агар. Проводят учет лецитиназы, пигмента, гемолиза. В колониях бактерий, выросших на МЖСА выявляют каталазу, что позволяет отдифферен-
цировать семейство Staphylococcaceae от семейства Streptococcaeae;
так у стафилококков каталаза имеется, а у стрептококков отсутствует. Устанавливают принадлежность бактерий к роду Staphylococcus.
Стафилококки образуют пигмент, обладают лецитиназой, гемолитической, каталазной активностью, являются факультативными анаэробами, а микрококки – облигатные аэробы. Поэтому стафилококки способны расти и ферментировать глюкозу в анаэробных условиях
153
(отмечается посинение в столбике среды под слоем вазелинового масла.
Установив принадлежность к роду Staphyloccocus, проводят видовую идентификацию стафилококков. Ведущий тест патогенности S.aureus – продукция плазмокоагулазы. Проводят посев культуры в цитратную плазму крови кролика. Отмечается коагуляция плазмы через 2-18 часов. Далее определяют анаэробную ферментацию маннита. При положительной реакции плазмокоагуляции, наличии лецитаназной, гемолитической активности, золотистого пигмента штамм может быть отнесен к виду S.aureus.
При отрицательной реакции плазмокоагуляции ставят дополнительные тесты на наличие ДНКазы, чувствительность к новобиоцину, определяют фосфатазу.
Для S.epidermidis характерны следующие тесты: чувствительность к новобиоцину, наличие фосфатазы, отсутствие окисления маннита; для S.saprophyticus – противоположные свойства.
Далее проводят определение чувствительности к антибиотикам. При необходимости по эпидпоказаниям осуществляют фаготипирование.
Заключение об этиологической роли стафилококков делают на основании многократного обильного выделения однотипных по свойствам и фаготипу стафилококков.
С целью эпидемиологического типирования изучают плазмидный профиль S.aureus: большие 2•107 Да плазмиды кодируют образование бета-лактамаз и резистентность к эритромицину. Мелкие (3•106 Да) плазмиды кодируют резистентность к тетрациклинам и хлорамфениколу.
Выделенная культура считается возбудителем инфекционного процесса при наличии следующих критериев: если из закрытых очагов, выделен один вид микроорганизма в количестве 103 и более; при открытых процессах этиологически значимыми считают культуры, численность которых более 105. Лабораторный анализ непременно включает определение чувствительности выделенных бактерий к антибиотикам.
Серологические методы. Для оценки состояния антитоксического иммунитета у больных определяют уровень антитоксических антител по лизису эритроцитов крови альфа-токсином. Антитела к тейхоевым кислотам стафилококков определяют методом ИФА.
Иммунитет зависит от уровня антитоксических и антимикробных антител. Новорожденные защищены материнскими IgG-антителами, полученными через плаценту.
Профилактика и лечение.
154
Профилактика стафилококковых инфекций направлена на выявление носителей золотистых стафилококков, главным образом, среди персонала больниц и родовспомогательных учреждений с целью их санации. Иногда для профилактики стафилококковой инфекции вакцинируют беременных в конце беременности очищенным стафилококковым анатоксином (повышается уровень IgG-антител у новорожденных).
Для лечения острых стафилококковых заболеваний назначают антибиотики под контролем антибиотикограммы.
При септических процессах вводят донорские противостафилококковый иммуноглобулин или антистафилококковую плазму.
Для лечения хронических стафилококковых инфекций применяют стафилококковый анатоксин, а также аутовакцину, которые стимулируют синтез антитоксических и антимикробных антител.
В травматологии и дерматологии используют стафилопротеин – это комплексный препарат, включающий очищенный анатоксин и цитоплазменный антиген стафилококка.
9.1.2. Род Stomatococcus
Кроду Stomatococcus относятся кокки диаметром 0,9-1,3 мкм, которые располагаются в виде гроздей винограда или по 4, неподвижны, имеют капсулу.
Факультативные анаэробы, хемоорганотрофы, имеют ферментативный и окислительный тип метаболизма. Каталазный тест вариабелен, содержат цитохромы, восстанавливают нитраты в нитриты, разлагают глюкозу в анаэробных условиях, чувствительны к бацитрацину.
На плотных питательных средах образуют колонии слизистой консистенции. Некоторые представители данного рода обитают в ротовой полости и в верхних дыхательных путях.
Стоматококки иногда выделяют от больных с сепсисом и эндокардитом.
9.2Семейство Streptococcaceae
Ксемейству Streptococcaceae отнесено 6 родов, патогенных для человека: Streptococcus, Enterococcus, Aerococcus, Leuconostoc, Pediococcus, Lactococcus. Наибольшее значение в патологии имеют роды Streptococcus и Enterococcus.
155

9.2.1. Род Streptococcus
Стрептококки впервые обнаружены в тканях человека при рожистом воспалении и раневых инфекциях (Т.Бильрот, 1874), а также при септицемиях и гнойных поражениях (Л.Пастер, 1880).
Морфология, свойства стрептококков. В род включены сферические или овоидные кокки размером 0,5-2,0 мкм, которые в мазках располагаются парами или короткими цепочками (особенно при выращивании на жидких средах). При различных внешних воздействиях они могут принимать вытянутую или ланцетовидную форму. Неподвижны, спор не образуют, некоторые имеют капсулу. Хемоорганотрофы, метаболизм бродильный, ферментируют глюкозу с образованием молочной кислоты. Факультативные анаэробы, некоторые являются микроаэрофилами, каталазоотрицательны. Большинство видов обладают гемолитической активностью. При росте на кровяном агаре различают -гемолитические стрептококки, дающие прозрачную зону гемолиза, -зеленящие, дающие вокруг колоний зону зеленого цвета (гемоглобин превращается в метгемоглобин) и негемолитические – среда не изменяется.
Классификация и антигенная структура. На основании отличий в полисахаридных антигенах Ленсфильд в 1933 г. разделила стрептококки на 20 серогрупп, обозначенных буквами от А до V. Заболевания у людей чаще вызывают стрептококки серогрупп А (S. pуogenes), В и С.
По наличию типоспецифических протеиновых антигенов стрептококки делятся на серовары M, R, T. По М-антигену различают более 100 сероваров в группе А, по Т – еще несколько десятков.
Род Streptococcus объединяет 21 вид стрептококков, которые отличаются по антигенным свойствам, биохимическим тестам и патогенности в отношении человека.
Виды стрептококков:
S. pyogenes – облигатно-патогенный для человека ( - гемолитический, группа А), который вызывает скарлатину, ангину, хронический тонзиллит, фарингит, ревматизм, гнойновоспалительные процессы кожи и подкожной клетчатки, остеомиелит, рожу, диффузный гломерулонефрит, сепсис, целлюлит.
S. pneumoniaе – (не входит в схему Ленсфильд), является возбудителем очаговой и крупозной пневмонии, сепсиса, менингита у детей, отитов, гнойных конъюнктивитов, бронхитов, ползучей язвы роговицы.
S. mitis, S. sanguis, S. salivarius, S. mutans (серогруппа К) – это условно-патогенные микроорганизмы, которые принимают участие в образовании зубных бляшек и возникновении кариеса зубов. Они имеют фермент гликозилтрансферазу, которая превращает сахарозу в
156
декстран, что способствует прикреплению стрептококков к поверхности зубов.
Стрептококки серовара 12 (нефритогенные) выделяют цитотоксины; имеют рецепторы к почечной ткани.
S. agalactiae относятся к серогруппе В, имеют капсулу, вызывают послеродовые инфекции, сепсис новорожденных, эрозивный стоматит, урогенитальные процессы. Эпидемиологически они связаны с носительством этого вида стрептококка у матери и персонала.
S.anginosus – стрептококки группы С, вызывают респираторные инфекции, заболевания мочеполовой системы.
Экология и распространение. Стрептококки группы А встречаются повсеместно. Микроорганизмы часто колонизируют кожные покровы и слизистые оболочки человека. Резервуар инфекции – больной человек или бактерионоситель. Основной путь передачи – контактный и воздушно-капельный, а также через инфицированные пищевые продукты. Стрептококки длительно сохраняются при низких температурах, устойчивы к высушиванию, в гное, мокроте сохраняются месяцами. При температуре 70оС они погибают в течение 1 часа, а 3% фенол убивает их через 15 минут.
Патогенез. Первым этапом инфекционного процесса является адгезия микроорганизмов к эпителию слизистых оболочек, что обеспечивает возможность быстрой их колонизации. Основным адгезином является липотейхоевая кислота, покрывающая поверхностные фимбрии. Фимбриальный белок (или белок М) – основной фактор вирулентности и типоспецифический антиген. Антитела к нему обеспечивают невосприимчивость к повторным заражениям. Большое разнообразие серотипов белка М значительно снижает действие гуморальных защитных реакций.
Белок М препятствует фагоцитозу за счет связывания фибриногена, фибрина и продуктов его деградации, адсорбирует их на своей поверхности, маскируя рецепторы для компонентов комплемента и опсонинов; способствует размножению стрептококков в крови. Он имеет свойства суперантигена, вызывает поликлональную активацию лимфоцитов, что ведет к нарушению толерантности к собственным тканевым АГ и развитию аутоиммунных реакций, потому что вызывает перекрестные реакции с кардиомиоцитами (антигенная мимик-
рия).
Капсула защищает стрептококки от антимикробного действия фагоцитов и облегчает адгезию к эпителию.
Факторы патогенности и ферменты инвазии и агрессии играют большую роль в патогенезе: стрептококки вызывают воспалительную реакцию, обусловленную секрецией более 20 растворимых продуктов
157
(стрептолизины О и S, гиалуронидаза, ДНКазы, стрептокиназы, эритрогенные токсины и т.д.)
Лейкоцидин стрептококков разрушает полиморфноядерные нейтрофилы, парализует фагоцитоз; гиалуронидаза облегчает проникновение бактерий в соединительную ткань; стрептокиназа активирует плазминоген, что приводит к образованию плазмина и растворению фибриновых волокон; различные виды нуклеаз разрушают ДНК; цитотоксический нефритогенный токсин пептидной природы поражет почечную ткань.
Бета-гемолитические стрептококки серогруппы А образуют ток-
сины О- и S-стрептолизины.
О-стрептолизин – белок, оказывает гемолитическое, цитотоксическое, кардиотоксическое и пирогенное действие. Этот токсин является антигеном, и у больных синтезируются антитела к нему. О- стрептолизин – порообразующий цитотоксин, повреждающий мембраны клеток посредством образования трансмембранных каналов.
S-стрептолизин – нуклеопротеид, секретируется в среду, содержащую сыворотку, оказывает гемолитическое, лейкотоксическое действие. Разрушает лизосомы и мембраны митохондрий.
Штаммы S. pyogenes выделяют токсин, который вызывает гломерулонефрит (серовар 12). При острых гломерулонефритах образуются иммунные комплексы антигенов стрептококка с IgG на базальной мембране, которые активируют систему комлемента, что стимулирует воспалительную реакцию.
Скарлатинозный эритрогенный токсин Дика (токсин сыпи) про-
дуцируется стрептококками, выделенными от больных скарлатиной; он вызывает поражение ЦНС, эндокринной, сердечно-сосудистой систем, поражение зева, паралитические изменения мелких кровеносных сосудов.
Эритрогенные токсины проявляют суперантигенные свойства, оказывают митогенное действие на Т-клетки, стимулируют выработку макрофагами ИЛ-1 и фактора некроза опухоли, являясь медиаторами септического шока.
Кардиогепатический токсин продуцируют некоторые штаммы стрептококков группы А, он вызывает поражения миокарда и диафрагмы и образование гигантоклеточных гранулем в печени.
Стрептококковый синдром токсического шока развивается как результат сочетанного действия различных эндотоксинов, продуцируемых стрептококками.
С5а–пептидаза подавляет активность фагоцитов. Фермент расщепляет и инактивирует С5а-компонент комплемента, который является хемоаттрактантом.
158

Роль стрептококков в этиологии скарлатины. Скарлатина – острое инфекционное заболевание, ее вызывает –гемолитический стрептококк группы А. В патогенезе заболевания ведущую роль играет эритрогенный токсин.
Источник инфекции – больной человек со стрептококковой ангиной, скарлатиной или носитель патогенного стрептококка. Восприимчивы лица, у которых нет антитоксического иммунитета. Путь передачи – воздушно-капельный. Стрептококки попадают на слизистую оболочку миндалин, мягкого неба, задней стенки глотки, вызывают воспалительную реакцию за счет выделения токсинов.
У ослабленных лиц местные изменения могут носить некротический характер и распространяться на близлежащие ткани – клетчатку шеи, среднее ухо, придаточные пазухи носа, сосцевидный отросток.
Клиника. Инкубационный период составляет 2-7 дней (1-12 дней). Острое начало: озноб, повышение температуры, нарастание интоксикации. Больные жалуются на головную боль, слабость, тошноту, рвоту. Отмечается гиперемия мягкого неба, дужек, задней стенки глотки, увеличение миндалин, язык обложен белым налетом, отечный. Увеличиваются регионарные лимфоузлы, поражаются периферические кровеносные сосуды, появляется мелкоточечная сыпь, которая подвергается шелушению. Характерен вид больного – на фоне яр- ко-розовой окраски кожи лица – отчетливо выделяется бледный носогубный треугольник. Сыпь держится 3-5 дней, а затем угасает. Стрептококки могут гематогенно проникать в различные ткани и вызывать нефрит, миокардит, ревматизм.
Выделяют особую – экстрабуккальную – форму скарлатины (раневую, ожоговую), когда входными воротами инфекции является не слизистая оболочка зева, а раны, вокруг которых возникает яркая мелкоточечная сыпь. Заболевание сопровождпется лихорадкой и интоксикацией.
Иммунитет после перенесенной скарлатины стойкий, антитоксический.
Лечение. Антибиотики пенициллинового и цефалоспоринового ряда, при аллергии на -лактамные антибиотики – эритромицин, азитромицин.
Лабораторная диагностика
Материалом для исследования являются гной, мокрота, слизь из зева и носа, кровь.
Микроскопический метод включает приготовление мазка и окраска его по Граму, при обнаружении грамположительных цепочек кокков необходимо производить посев на чашки с кровяным и сахарным агарами.
159

Бактериологический метод – основной, при посеве на чашках с кровяным агаром обращают внимание на рост гемолитических и зеленящих стрептококков, из колоний делают мазки, окрашивают по Граму, при обнаружении грам(+) цепочек кокков ставят каталазный тест, который у стрептококков отрицательный. Далее колонии пересевают на сывороточный бульон или тиогликолевую среду, где стрептококки дают придонный рост. Затем определяют серогруппу путем постановки реакции преципитации в геле или ИФА с группоспецифическими сыворотками. Следующий этап – определяют серотип путем постановки реакции латекс-агглютинации с М-антисыворотками.
Более 99% изолятов чувствительны к бацитрацину. Серологические методы. Определяют АТ к токсинам и фермен-
там. При ревматизме оценивают нарастание титра антител к О- стрептолизину, ДНКазе, гиалуронидазе.
При заболеваниях мочеполовой системы и инфекциях новорожденных штаммы гемолитических стрептококков дифференцируют со S. agalactiae используя САMР-тест (название произошло от первых букв фамилий австралийских исследователей, предложивших тест). Для этого проводят совместное выращивание на кровяном агаре с добавлением глюкозы штамма стафилококка, вырабатывающего бетагемолизин, и исследуемых культур стрептококка; при наличии S. agalactiae в месте пересечения культур образуется гемолиз, приобретающий форму бабочки. S. agalactiae нечувствительны к бацитрацину.
Дальнейшую идентификацию проводят после обработки мазков противострептококковыми моноклональными антителами, меченными флюорохромами: свечение при взаимодействии с определенным антителом указывает на тип и серовар.
Роль стрептококков в этиологии ревматизма. Ревматизм представляет собой врспалительное заболевание, возникающее как отерогенное следствие инфекционного поражения глотки - гемолитическими стрептококками группы А.
Этиологическая связь стрептококков группы А с ревматизмом подтверждается клиническими и эпидемиологическими данными. В острой фазе ревматизма всегда обнаруживаются иммунологические признаки перенесенной ранее стрептококковой инфекции и повышение титров антител к стрептококковым антигенам.
Обычно ревматизм обостряется после перенесенной стрептококковой инфекции. Первичные и повторные атаки ревматизма можно предотвратить с помощью антибактериальной терапии (бициллина, пенициллина).
Воротами инфекции при начале ревматического процесса служит глотка.
160
