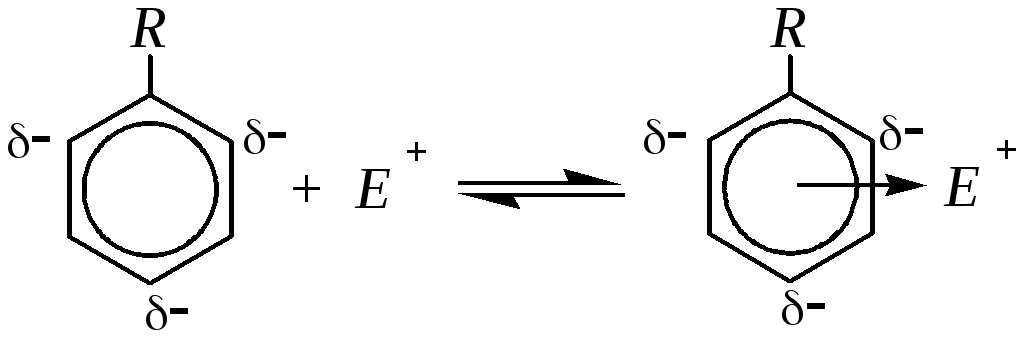- •Глава 1. Основы теоретических представлений в органической химии
- •1.1. Учение а.М. Бутлерова
- •1.2. Теория гибридизации атомных орбиталей
- •1.3. Ковалентная связь
- •1.3.3. Водородные связи
- •1.4. Теория электронных смещений
- •1.5. Классификация и номенклатура органических соединений
- •1.5.1. Заместительная номенклатура
- •1.5.2. Радикало-функциональная номенклатура
- •1.5.4. Рациональная Номенклатура
- •1.6. Представление о Кислотно-оснÓвных свойствах органических соединений
- •1.7. Основы стереохимии
- •1.7.1. Оптическая изомерия
- •1.7.2. Геометрическая изомерия
- •1.7.3. Конформационная изомерия
- •1.8. Классификация органических реакций. Понятие о механизме реакций. Растворители и катализаторы
- •1.9. Методы идентификации органических соединений. Основные физические константы
- •1.10. Методы разделения и очистки органических веществ
- •1.10.1. Разделение твёрдых смесей и очистка твёрдых веществ
- •1.10.2. Разделение жидких смесей и очистка жидкостей
- •1.11. Представление о биологическом действии и метаболизме органических соединений
- •Глава 2. Алканы
- •2.1. Номенклатура. Изомерия
- •2.2. Строение
- •2.3. Физические свойства
- •2.4. Химические свойства
- •2.4.1. Реакции радикального замещения
- •2.4.2. Реакции дегидрирования и разложения
- •2.4.3. Реакции изомеризации
- •Способы получения и природные источники
- •2.6. Применение и физиологическая роль
- •Глава 3. Функциональные производные алканов
- •3.1. ОбщноСть Химических свойств
- •3.1.1. Реакции нуклеофильного замещения
- •3.1.2. Реакции отщепления (элиминирования)
- •3.2. Галогеналканы
- •3.2.1. Классификация, номенклатура, изомерия
- •3.2.2. Строение и свойства
- •3.2.3. Способы получения
- •3.2.4. Полигалогеналканы
- •3.2.5. Физиологическая роль и Важнейшие представители
- •3.3. Насыщенные спирты
- •3.3.1. Классификация, номенклатура, изомерия
- •3.3.2. Строение и физические свойства
- •3.3.3. Химические свойства
- •3.3.4. Способы получения
- •3.3.5. Многоатомные спирты
- •3.3.6. Физиологическое действие
- •3.3.7. Важнейшие представители
- •3.4. Простые насыщенные эфиры
- •3.4.1. Номенклатура и изомерия
- •3.4.2. Физические и химические свойства
- •3.4.3. Способы получения
- •3.4.4. Циклические простые эфиры
- •3.4.5. Физиологическая роль и Важнейшие представители
- •3.5. Эфиры минеральных кислот
- •3.5.1. Эфиры серной кислоты
- •3.5.2. Эфиры фосфорной кислоты
- •3.6. Тиоспирты и тиоэфиры
- •3.7. Насыщенные амины
- •3.7.1. Классификация, номенклатура, изомерия
- •3.7.2. Физические свойства
- •3.7.3. Строение и химические свойства
- •3.7.4. Способы получения
- •3.7.5. Физиологическая роль и Важнейшие представители
- •3.8. Нитроалканы
- •3.8.1. Строение
- •3.8.2. Свойства
- •3.8.3. Способы получения
- •3.8.4. Физиологическое действие и Важнейшие представители
- •3.9. Кремний-, фосфор- и мышьякорганические соединения
- •3.9.1. Кремнийорганические соединения
- •3.9.2. Фосфорорганические соединения
- •3.9.3. Мышьякорганические соединения
- •Глава 4. Непредельные углеводороды
- •4.1. ОБщность строения и химических свойств
- •4.1.1. Реакции электрофильного присоединения
- •4.1.2. Реакции радикального присоединения
- •4.1.3. Реакции радикального замещения
- •4.1.4. Другие реакции
- •4.2. Этиленовые углеводороды
- •4.2.1. Номенклатура, изомерия
- •4.2.2. Физические свойства
- •4.2.3. Химические свойства
- •4.2.4. Способы получения
- •4.2.5. Физиологическое действие и Важнейшие представители
- •4.3. Диеновые (и полиеновые) углеводороды
- •4.3.1. Классификация, номенклатура
- •4.3.5. Способы получения
- •4.3.6. Важнейшие представители
- •4.4. Ацетиленовые углеводороды
- •4.4.1. Номенклатура, изомерия
- •4.4.2. Особенности строения и свойств
- •4.4.3. Способы получения
- •4.4.4. Физиологическое действие и Важнейшие представители
- •Глава 5. Функциональные производные непредельнЫх углеводороДов
- •5.1. ОБщность строения и химических свойств
- •5.1.1. Классификация
- •5.1.2. Субстраты винильного типа
- •5.1.3. Субстраты аллильного типа
- •5.2. Галогеналкены
- •5.2.1. Винилгалогениды
- •5.2.2. Аллилгалогениды
- •5.2.3. Способы получения
- •5.2.4. Важнейшие представители
- •5.3. Непредельные спирты и эфиры
- •5.3.1. Виниловый спирт и его эфиры
- •5.3.2. Аллиловый и пропаргиловый спирты
- •5.3.3. Способы получения
- •5.3.4. Важнейшие представители
- •Глава 6. Алифатические альдегиды, кетоны и карбоновые кислоты
- •6.1. Насыщенные альдегиды и кетоны
- •6.1.1. Изомерия, номенклатура
- •6.1.2. Строение карбонильной группы
- •6.1.3. Физические свойства
- •6.1.4. Химические свойства
- •6.1.5. Способы получения
- •6.1.6. Физиологическая роль
- •6.1.7. Важнейшие представители
- •6.2. Непредельные альдегиды и кетоны
- •6.2.1. Кетен
- •6.2.2. Непредельные карбонильные соединения
- •Примерами соединений с сопряжёнными -связями являются
- •6.2.3. Важнейшие представители
- •6.3. Дикарбонильные соединения
- •6.3.3. Важнейшие представители
- •6.4. Насыщенные монокарбоновые кислоты и их производные
- •6.4.1. Номенклатура
- •6.4.2. Строение функциональной группы
- •6.4.3. Физические свойства
- •6.4.4. Химические свойства
- •6.4.5. Способы получения
- •6.4.6. Пероксикарбоновые кислоты и ацилпероксиды
- •6.4.7. Физиологическая роль и Важнейшие представители
- •6.5. Непредельные монокарбоновые кислоты
- •6.5.1. Номенклатура, изомерия
- •6.5.2. Строение
- •6.5.3. Химические свойства
- •6.5.4. Способы получения
- •6.5.5. Физиологическая роль и Важнейшие представители
- •6.5.6. Омыляемые липиды
- •6.6. Дикарбоновые кислоты и их производные
- •6.6.1. Особенности химического поведения
- •6.6.2. Малоновый эфир и синтезы на его основе
- •2 H5c2ooc-ch2-cooc2h5
- •2 H5c2ooc-ch2-cooc2h5
- •6.6.3. Способы получения
- •2 Rooc-(ch2)n-сoo¯ 2 rooc-(ch2)n-сoo rooc-(ch2)2n-coor hooc-(ch2)2n-cooh
- •6.6.4. Важнейшие представители
- •6.7. Гидроксикислоты
- •6.7.1. Классификация, номенклатура, изомерия
- •6.7.2. Химические свойства
- •6.7.3. Способы получения
- •6.7.4. Физиологическая роль и Важнейшие представители
- •6.8. Оксокислоты
- •6.8.1. Особенности химического поведения
- •6.8.2. Ацетоуксусный эфир и синтезы на его основе
- •6.8.3. Способы получения
- •6.8.4. Важнейшие представители
- •6.9. Аминокарбоновые кислоты. Пептиды
- •6.9.1. Классификация, номенклатура, изомерия аминокислот
- •6.9.2. Строение, физические и Химические свойства
- •6.9.3. Способы получения аминокислот
- •6.9.4. Важнейшие представители аминокислот
- •6.9.5. Пептиды
- •Глава 7. Углеводы
- •7.1. Моносахариды
- •7.1.1. Изомерия, номенклатура
- •7.1.2. Химические свойства
- •7.1.3. Важнейшие представители моносахаридов и их производных
- •7.2. Олигосахариды
- •7.2.1. Классификация и номенклатура дисахаридов
- •7.2.2. Химические свойства дисахаридов
- •7.2.3. Важнейшие представители дисахаридов
- •7.3. Полисахариды
- •7.3.1. Целлюлоза
- •7.3.2. Амилоза и амилопектин
- •7.3.3. Гликоген
- •7.3.4. Декстраны
- •7.3.5. Хитин
- •7.3.6. Пектовая кислота
- •7.3.7. Гетерополисахариды
- •Глава 8. Алициклические углеводороды и их производные
- •8.1. Номенклатура моно- и бициклических соединений
- •8.2. Пространственное строение и изомерия циклоалканов
- •8.2.1. Циклопропан
- •8.2.2. Циклобутан
- •8.2.3. Циклопентан
- •8.2.4. Циклогексан
- •8.3. Химические свойства
- •8.3.1. Реакции циклопропана, циклопропена и их производных
- •8.3.2. Реакции циклобутана и его производных
- •8.3.3. Реакции средних циклов
- •8.3.4. Реакции изомеризации цикла
- •8.4. Способы получения циклоалканов
- •8.5. Терпены и терпеноиды. Каротиноиды
- •8.5.1. Ациклические терпены и терпеноиды
- •8.5.2. Моноциклические терпены и терпеноиды
- •8.5.3. Бициклические терпены и терпеноиды
- •8.5.4. Каротиноиды
- •8.6. Физиологическая роль и важнейшие представители
- •8.7. Стероиды
- •Глава 9. Бензол. Ароматичность. Углеводороды ряда бензола
- •9.1. Строение бензола
- •Тепловой эффект реакции гидрирования бензола составляет
- •9.2. Номенклатура и изомерия аренов
- •9.3. Строение аренов
- •9.3.1. Строение толуола
- •9.3.2. Строение винилбензола
- •9.4. Физические свойства
- •9.5. Химические Свойства
- •9.5.1. Химические свойства бензола
- •9.5.2. Химические свойства аренов
- •9.6. Способы получения
- •9.7. Физиологическое действие и важнейшие представители аренов
- •9.8. Небензоидные ароматические системы
- •Глава 10. Функциональные производные углеводородов ряда бензола
- •10.1. Общность строения и свойств монозамещённых бензолов
- •10.1.1. Электронные эффекты заместителей
- •10.1.2. Реакции электрофильного замещения
- •10.1.3. Реакции нуклеофильного замещения
- •10.2. Галогенарены
- •10.2.1. Классификация, номенклатура
- •10.2.2. Строение арилгалогенидов
- •10.2.3. Физические свойства
- •10.2.4. Химические свойства
- •10.2.5. Способы получения
- •10.2.6. Важнейшие представители
- •10.3. Ароматические сульфокислоты
- •10.3.1. Номенклатура
- •10.3.2. Строение
- •10.3.3. Физические и химические свойства
- •10.3.4. Способы получения
- •10.3.5. Производные сульфокислот
- •10.3.6. Медико-биологическое значение и Важнейшие представители
- •10.4. Ароматические нитросоединения
- •10.4.1. Строение нитробензола
- •10.4.2. Физические свойства
- •10.4.3. Химические свойства
- •10.4.4. Способы получения
- •10.4.5. Физиологическое действие и Важнейшие представители
- •10.5. Фенолы. Ароматические спирты. Хиноны
- •10.5.1. Классификация, номенклатура, изомерия фенолов и ароматических спиртов
- •10.5.2. Строение фенола и бензилового спирта
- •Ароматические амины и продукты неполного восстановления нитросоединений
- •10.6.1. Классификация, номенклатура, изомерия ароматических аминов
- •10.6.2. Строение анилина
- •10.6.3. Физические и химические свойства ароматических аминов
- •10.6.4. Способы получения ароматических аминов
- •10.6.5. Важнейшие представители ароматических аминов
- •10.6.6. Продукты неполного восстановления нитросоединений
- •10.7. Ароматические диазосоединения
- •10.7.2. Механизм образования солей арендиазония и строение катиона бензолдиазония
- •10.7.3. Амфотерность диазосоединений
- •10.7.4. Реакции солей арендиазония
- •10.8. Ароматические альдегиды и кетоны
- •10.9. Ароматические карбоновые кислоты и их производные
- •10.10. Физиологическая роль функциональных производных бензола
- •Глава 11. Полициклические ароматические углеводороды и их производные
- •11.1. Классификация углеводородов с конденсированными циклами
- •11.2. Нафталин
- •11.2.1. Строение, изомерия, номенклатура
- •11.2.2. Свойства
- •11.2.3. Способы получения
- •11.2.4. Важнейшие представители
- •11.3. Антрацен
- •11.3.1. Строение, изомерия, номенклатура
- •11.3.2. Свойства
- •Продукт исчерпывающего гидрирования (пергидроантрацен) можно получить, проводя реакцию в жёстких условиях с применением металлических катализаторов.
- •11.3.3. Способы получения
- •11.3.4. Важнейшие представители
- •11.4. Фенантрен
- •11.4.1. Строение, изомерия, номенклатура
- •11.4.2. Свойства
- •11.4.3. Способы получения
- •11.5. Физиологическое действие полициклических углеводородов
- •Глава 12. Гетероциклические соединения
- •12.1. Классификация и номенклатура
- •12.2. Пятичленные гетероциклические
- •12.2.1. Номенклатура пиррола, фурана и тиофена и их производных
- •12.2.2. Строение пиррола, фурана и тиофена
- •12.2.3. Физические и химические свойства пиррола, фурана и тиофена
- •12.2.4. Особенности индола
- •12.2.5. Способы получения пиррола, фурана, тиофена, индола
- •12.2.6. Важнейшие представители и медико-биологическое значение
- •12.3. Пятичленные гетероциклические
- •12.3.1. Номенклатура имидазола и пиразола
- •12.3.2. Строение имидазола и пиразола
- •12.3.3. Физические и химические свойства имидазола и пиразола
- •12.3.4. Способы получения
- •12.3.5. Важнейшие представители и медико-биологическое значение
- •12.4. Шестичленные гетероциклические
- •12.4.1. Номенклатура пиридина и его производных
- •12.4.2. Строение пиридина
- •12.4.3. Химические свойства пиридина
- •Но если оба -положения заняты, то замещается водород в-положении. При нагревании с избытком амида натрия можно получить 2,6-диаминопиридин.
- •12.4.4. Особенности химического поведения пиколинов и функциональных производных пиридина
- •12.4.5. Хинолин и изохинолин
- •12.4.7. Способы получения
- •Реакция аналогична получению бензола, протекает при высоких температурах, но представляет только теоретический интерес.
- •12.4.8. Важнейшие представители и медико-биологическое значение
- •12.5. Шестичленные гетероциклические
- •12.5.1. Строение и свойства диазинов
- •12.5.2. Пурин
- •12.5.3. Способы получения
- •12.5.4. Важнейшие представители и медико-биологическое значение
- •12.5.5. Нуклеозиды, нуклеотиды и нуклеиновые кислоты
- •12.6. Алкалоиды
9.5.2. Химические свойства аренов
Природа таких заместителей в бензольном кольце может быть различной: они могут быть насыщенными, а могут содержать одну или несколько по-разному расположенных кратных связей. Всё это может сильно влиять на поведение данного углеводорода в тех или иных реакциях. Здесь будут рассмотрены наиболее типичные превращения соединений с заместителями, не содержащих кратных связей и содержащих двойную связь у -углеродного атома.
9.5.2.1. Реакции электрофильного замещения
Как показано в химических свойствах бензола, реакции электрофильного замещения (SE) в ароматическом ряду занимают наиболее значимое место. В связи с этим механизм реакций, общие закономерности и условия их протекания для различных ароматических соединений подробно рассмотрены в главе 10.1.2.
Для алкилбензолов характерны те же электрофильные реакции, что и для незамещённого бензола. Это прежде всего нитрование, сульфирование, галогенирование, алкилирование и ацилирование. Продуктами этих реакций могут быть различные функциональные производные аренов, в связи с чем такие реакции могут использоваться как способы получения разнообразных ароматических соединений.
Однако при рассмотрении реакций электрофильного замещения необходимо иметь в виду, что, так как алкильные группы обладают электронодонорными эффектами по отношению к бензольному кольцу, то взаимодействие таких соединений с электрофилами будет протекать легче, чем незамещённого бензола. Это выражается в возрастании скорости реакции и замещении, как правило, не одного, а нескольких водородных атомов кольца. Кроме того, следует иметь в виду, что в молекулах алкилбензолов электронная плотность распределена неравномерно по бензольному кольцу. Поэтому подвергаться электрофильной атаке будут атомы углерода кольца с повышенной электронной плотностью.
|
|
|
|
-комплекс
|
-комплекс
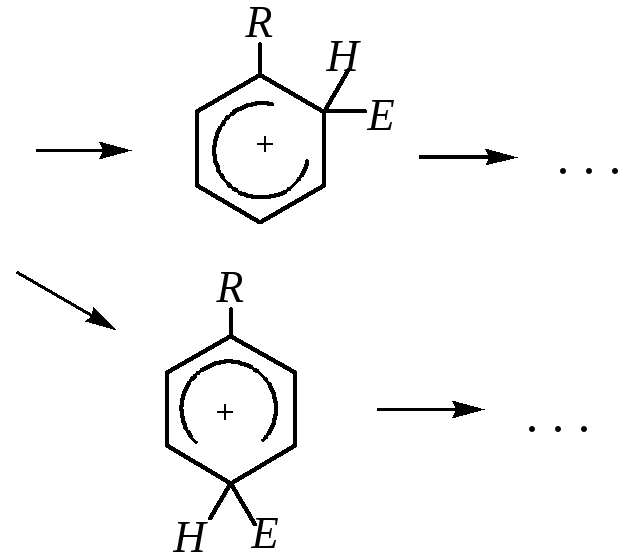
Если в реакцию вступает моноалкилзамещённый бензол, то в результате электрофильного замещения образуются о- и п-дизамещённые бензолы, а при протекании реакции до конца — продукт исчерпывающего замещения:
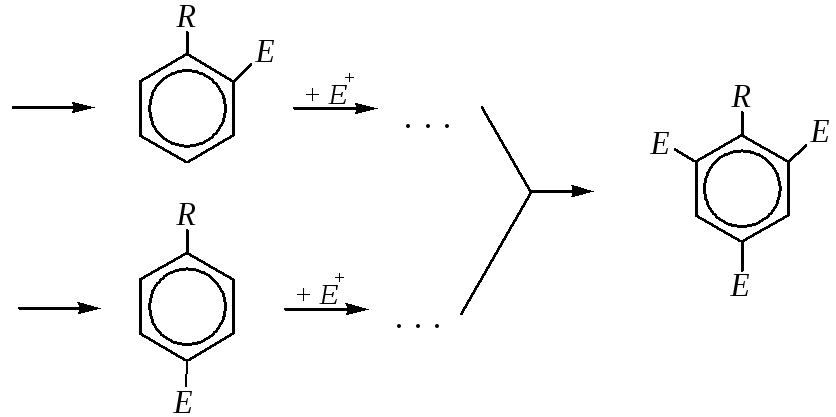
С другой стороны, в реакциях замещения ориентирующее направление алкильной группы в орто- и пара-положениях бензольного кольца может быть объяснено и динамическим подходом, то есть сравнением устойчивости образующихся -комплексов. Рассмотрим образование -комплексов на примере взаимодействия с электрофильной частицей молекулы толуола. При образовании -связи между электрофилом и углеродным атомом, находящимся в орто-, мета- или пара-положении бензольного кольца, образуются соответственно три -комплекса, строение которых описывается следующими граничными структурами:
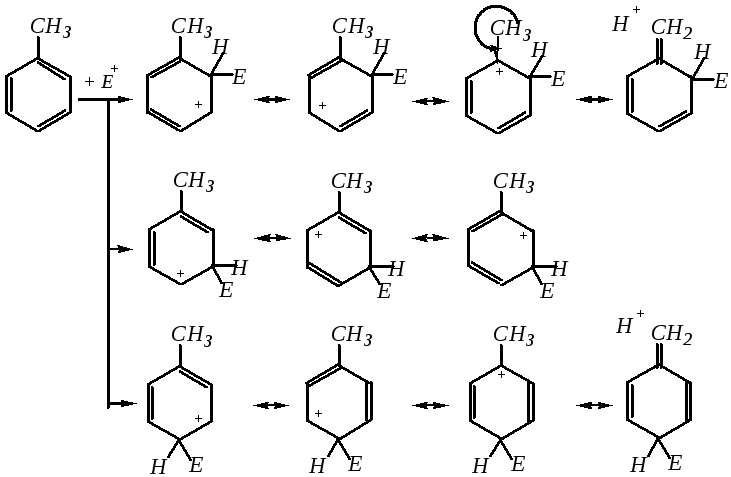
Как видно, в случаях вступления электрофила в о- и п-положения число граничных структур данных -комплексов больше, чем при вступлении электрофила в м-положение бензольного кольца (четыре против трёх). К тому же среди о- и п-изомеров присутствуют такие структуры, в которых подчёркивается участие электронодонорной (метильной) группы в делокализации положительного заряда -комплекса, — это последние из изображённых в соответствующих рядах структур. Всё это подтверждает, что направление электрофильной атаки в о- и п-положения бензольного кольца энергетически выгоднее атаки в м-положение.
Однако необходимо иметь в виду, что о- и п-ориентация определяет лишь преимущественное направление реакции электрофильного замещения в алкилбензолах, то есть замещение идёт в эти положения бензольного кольца преобладающим образом, но не исключительно. Обычно образуется смесь всех трёх изомеров (орто-, мета-, пара-), но они находятся в разных соотношениях. Доля м-изомера определяется, главным образом, силой ориентирующего влияния алкильной группы R в бензольном кольце. Чем больше число атомов водорода при -углеродном атоме, тем выше значение электронной плотности на кольце (эффект Натана–Бейкера*). Это может быть объяснено величиной эффекта сверхсопряжения данной алкильной группы с ароматическим кольцом. По мере уменьшения проявляемого эффекта --сопряжения алкильные группы располагаются в следующем порядке:
-CH3 > -CН2СН3 > -CH(CH3)2 > -C(CH3)3 ,
так как число -водородных атомов в этом ряду уменьшается от 3 до 0. При этом уменьшается реакционная способность соединений с такими заместителями (от толуола дотрет-бутилбензола). Но кроме того, силао-п-ориентирующего влияния тоже ослабевает, то есть доляо- и п-изомеров несколько уменьшается и увеличивается относительное количество продуктам-замещения. Но даже для реакций с участием толуола доля образующегосям-изомера может достигать 10%. Поэтому метильную и другие алкильные группы называют слабыми ориентантами.
Нитрование — один из примеров реакций электрофильного замещения в ароматическом кольце.
Так, при мононитровании толуола образуется 58%о-изомера и38%п-изомера. При дальнейшем нитровании смеси нитротолуолов при 350Кполучается смесь изомеров с преобладанием 2,4-динитротолуола. В смеси содержится также заметное количество 2,6-динитротолуола. Для нитрования динитротолуолов в 2,4,6-тринитротолуол (тротил) применяют безводную смесь серной и азотной кислот с двойным избытком азотной кислоты по сравнению с теоретически необходимым. Нитрование проводят при температуре около 370К.
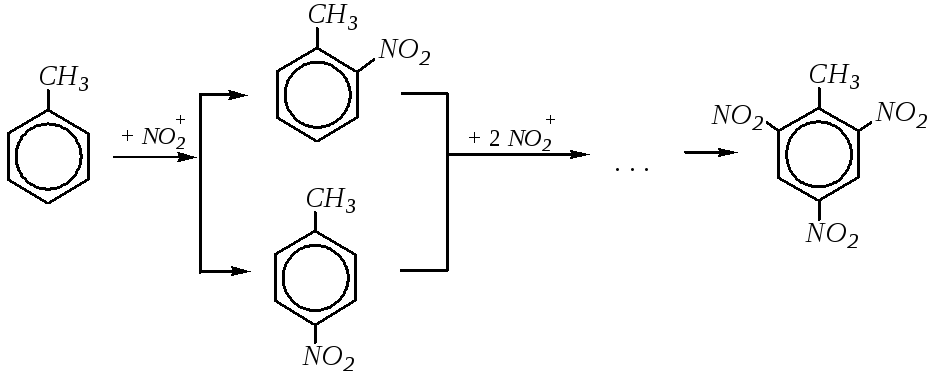
Другой пример SE-реакций алкилбензолов — алкилирование по Фриделю–Крафтсу. Эта реакция среди других реакций ароматического замещения наиболее неселективна: кроме моноалкилированного, образуются ди- и полиалкилзамещённые соединения.

Реакция Фриделя–Крафтса обратима, поэтому при нагревании протекает перегруппировка о- и п-диалкилбензолов в термодинамически более устойчивый м-диалкилбензол:
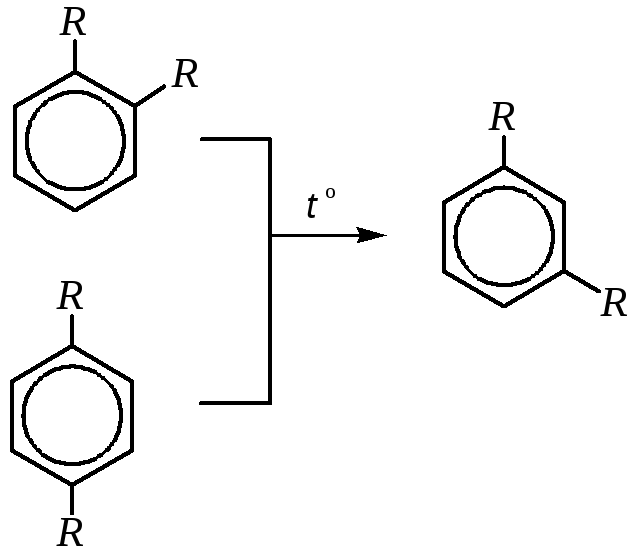
Следует заметить, что углеводороды с непредельными связями в боковой цепи взаимодействуют с электрофилами прежде всего по этим связям, а не по бензольному кольцу. Такое направление обусловлено тем, что электрофильное присоединение с сохранением ароматичности протекает значительно легче, чем замещение в бензольном кольце:
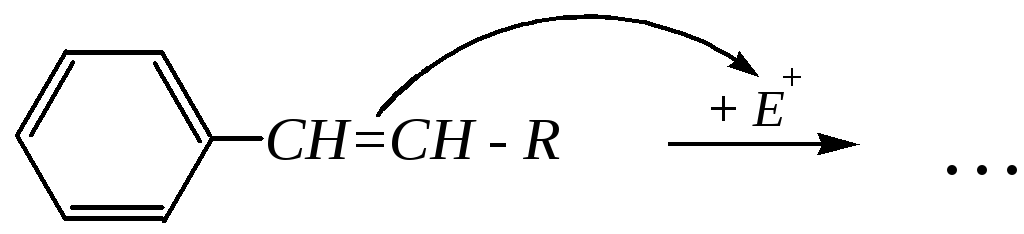
9.5.2.2. Восстановление бензольного кольца по Бёрчу
Как и сам бензол, алкилбензолы могут быть восстановлены до циклодиенов действием щелочных металлов и спирта в среде жидкого аммиака. При этом селективно образуются 1-алкилциклогексадиены-1,4, как это следует из механизма реакции, протекающей через образование наиболее стабильной структуры анион-радикала:
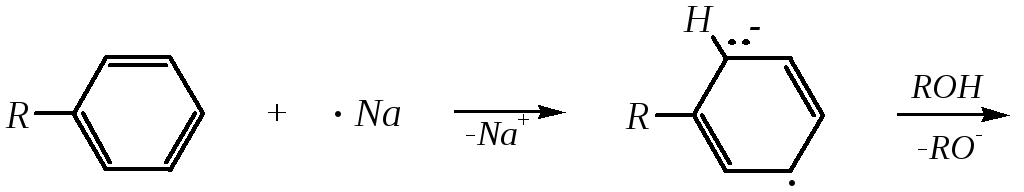
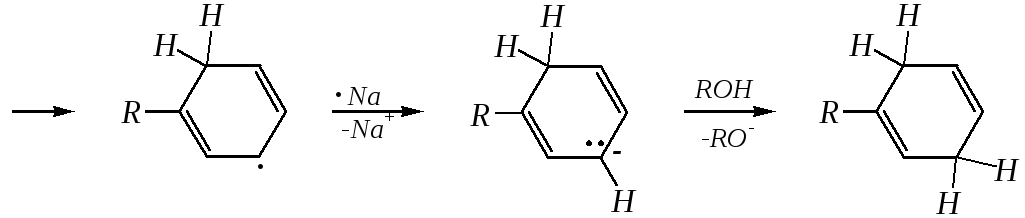
1-алкилциклогексадиены-1,4
9.5.2.3. Реакции боковых цепей
Химические реакции, протекающие с участием углеводородных заместителей, определяются прежде всего природой этих заместителей, а также влиянием на них -электронного секстета ароматического кольца. Поэтому должно наблюдаться существенное различие в химическом поведении соединений с предельными и непредельными боковыми цепями.
Радикальное замещение
В алифатическом ряду SR-реакции характерны главным образом для алканов. Поэтому аналогично алканам для аренов, содержащих насыщенные углеводородные заместители, в условиях свободнорадикальных реакций (облучение, нагревание) наблюдаются реакции замещения в боковой цепи. Общий механизм радикального замещения включает те же стадии, что и в случае радикального замещения в алканах: инициирование, рост цепи, обрыв цепи (гл. 2.4.1). Однако влияние бензольного кольца на алкильный радикал приводит к одной особенности: всегда замещается -водородный атом (если он имеется). Такая селективность — существенное отличие от реакции радикального замещения алканов.
Так, например, галогенирование любого алкилбензола приводит к образованию -галогенозамещённого и является распространённым способом получения галогенозамещённых аренов с атомом галогена у -углеродного атома боковой цепи:
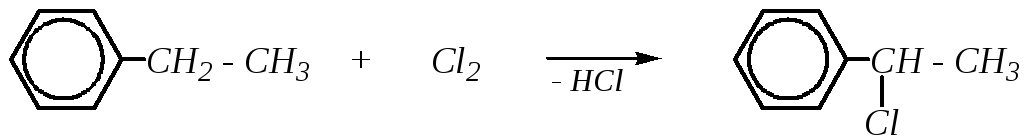
Причина такого направления реакции кроется во влиянии бензольного кольца на стабильность образующегося алкильного радикала.
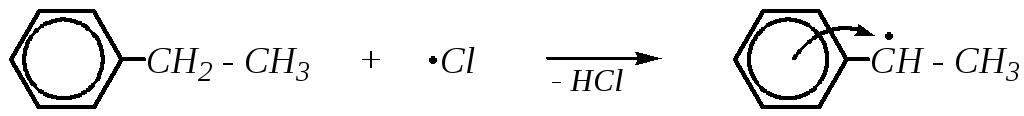
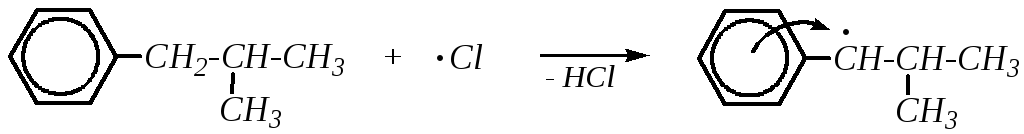
Образующиеся таким образом радикалы бензильного типа значительно устойчивее третичного, вторичного и тем более первичного радикалов, не сопряжённых с бензольным кольцом. В результате р--сопряжения происходит делокализация спиновой плотности радикала бензильного типа. Истинное строение радикала можно представить как промежуточное между пятью граничными структурами:
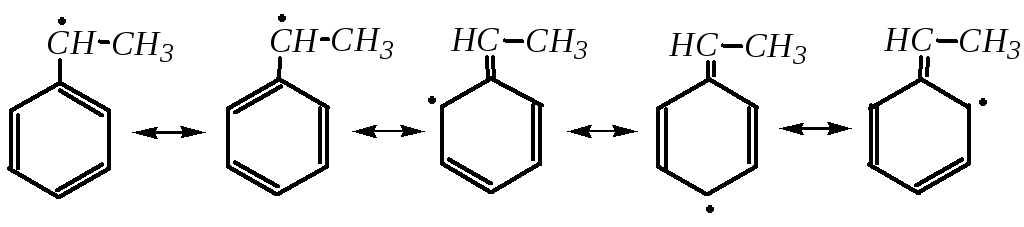
Электрофильное и радикальное присоединение
Реакции электрофильного присоединения (АdЕ) характерны для углеводородов, содержащих кратные связи в боковой цепи. При этом наиболее существенно влияние бензольного кольца на химическое поведение таких соединений, молекулы которых содержат двойную связь в -положении к ароматическому кольцу. Например, гидрогалогенирование таких соединений протекает селективно и приводит только к одному продукту — -галогенопроизводному:
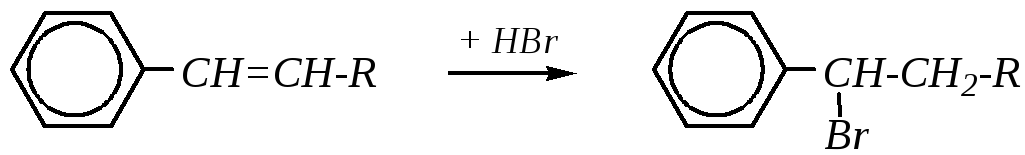
Именно такое направление присоединения объясняется устойчивостью образующегося карбокатиона (-комплекса) при присоединении электрофильной частицы к молекуле субстрата.
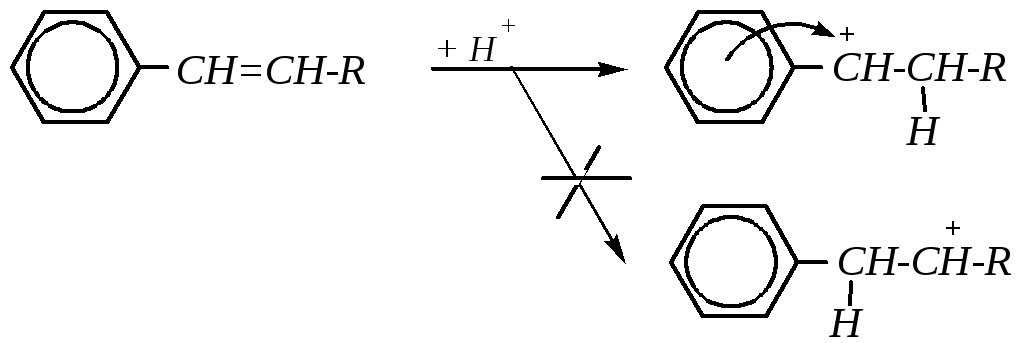
Только катион бензильного типа будет стабилизирован р--сопряжением, и положительный заряд этого катиона делокализован с участием -электронной системы бензольного кольца. Истинное строение такого катиона является промежуточным между пятью граничными структурами:
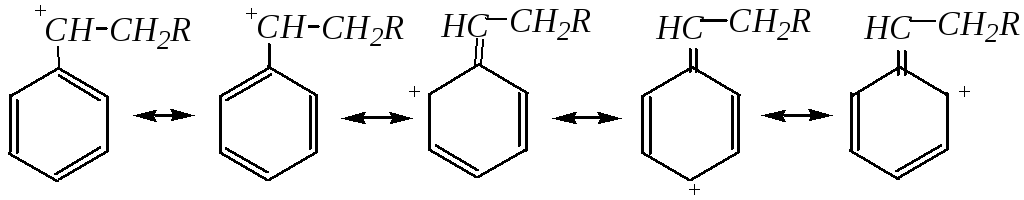
Присоединение в присутствии пероксидов (по механизму АdR) протекает, как это следует из рассмотрения механизма реакции, с образованием -галогенопроизводного (гл. 4.1.2).
Дегидрирование, окисление
Дегидрирование характерно для насыщенных боковых цепей, протекает при повышенной температуре (800—900 К) на поверхности катализаторов; для этих целей используются оксиды магния, кальция, алюминия. При этом образование -связи в -положении к бензольному кольцу термодинамически выгодно, так как в этом случае возникает --сопряжённая система.
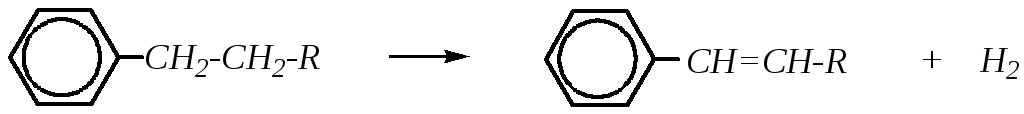
Окислению перманганатом или дихроматом калия могут подвергаться углеводороды с любыми алкильными заместителями в бензольном кольце, хотя ни алканы, ни бензол не окисляются подобным образом. Так, алкилбензолы, имеющие -водородный атом, окисляются до бензойной кислоты при кипячении в течение нескольких часов. Независимо от длины и строения алкильного радикала образуются карбоновые кислоты с карбоксильной группой, связанной с бензольным кольцом. Например:


Каталитическое окисление кислородом воздуха приводит к тем же продуктам, и в данном случае механизм реакции — радикальный и связан с участием образующегося радикала бензильного типа, из которого в качестве промежуточного продукта образуется -гидропероксид:

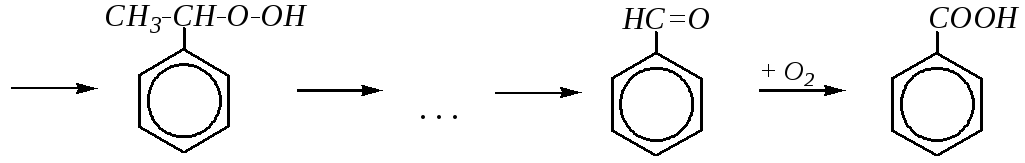
Данный процесс катализируется солями некоторых металлов переменной валентности (в частности Co3+).
Арены с кратными связями в боковых цепях подвергаются окислению аналогично этиленовым и ацетиленовым углеводородам (гл. 4.1.4.3). При действии озона на такие углеводороды реакция протекает одновременно как по кратной связи боковой цепи, так и по бензольному кольцу. Окисление озоном гомологов бензола протекает так же, как и для бензола (гл. 9.5.1.4).