- •Глава 1. Основы теоретических представлений в органической химии
- •1.1. Учение а.М. Бутлерова
- •1.2. Теория гибридизации атомных орбиталей
- •1.3. Ковалентная связь
- •1.3.3. Водородные связи
- •1.4. Теория электронных смещений
- •1.5. Классификация и номенклатура органических соединений
- •1.5.1. Заместительная номенклатура
- •1.5.2. Радикало-функциональная номенклатура
- •1.5.4. Рациональная Номенклатура
- •1.6. Представление о Кислотно-оснÓвных свойствах органических соединений
- •1.7. Основы стереохимии
- •1.7.1. Оптическая изомерия
- •1.7.2. Геометрическая изомерия
- •1.7.3. Конформационная изомерия
- •1.8. Классификация органических реакций. Понятие о механизме реакций. Растворители и катализаторы
- •1.9. Методы идентификации органических соединений. Основные физические константы
- •1.10. Методы разделения и очистки органических веществ
- •1.10.1. Разделение твёрдых смесей и очистка твёрдых веществ
- •1.10.2. Разделение жидких смесей и очистка жидкостей
- •1.11. Представление о биологическом действии и метаболизме органических соединений
- •Глава 2. Алканы
- •2.1. Номенклатура. Изомерия
- •2.2. Строение
- •2.3. Физические свойства
- •2.4. Химические свойства
- •2.4.1. Реакции радикального замещения
- •2.4.2. Реакции дегидрирования и разложения
- •2.4.3. Реакции изомеризации
- •Способы получения и природные источники
- •2.6. Применение и физиологическая роль
- •Глава 3. Функциональные производные алканов
- •3.1. ОбщноСть Химических свойств
- •3.1.1. Реакции нуклеофильного замещения
- •3.1.2. Реакции отщепления (элиминирования)
- •3.2. Галогеналканы
- •3.2.1. Классификация, номенклатура, изомерия
- •3.2.2. Строение и свойства
- •3.2.3. Способы получения
- •3.2.4. Полигалогеналканы
- •3.2.5. Физиологическая роль и Важнейшие представители
- •3.3. Насыщенные спирты
- •3.3.1. Классификация, номенклатура, изомерия
- •3.3.2. Строение и физические свойства
- •3.3.3. Химические свойства
- •3.3.4. Способы получения
- •3.3.5. Многоатомные спирты
- •3.3.6. Физиологическое действие
- •3.3.7. Важнейшие представители
- •3.4. Простые насыщенные эфиры
- •3.4.1. Номенклатура и изомерия
- •3.4.2. Физические и химические свойства
- •3.4.3. Способы получения
- •3.4.4. Циклические простые эфиры
- •3.4.5. Физиологическая роль и Важнейшие представители
- •3.5. Эфиры минеральных кислот
- •3.5.1. Эфиры серной кислоты
- •3.5.2. Эфиры фосфорной кислоты
- •3.6. Тиоспирты и тиоэфиры
- •3.7. Насыщенные амины
- •3.7.1. Классификация, номенклатура, изомерия
- •3.7.2. Физические свойства
- •3.7.3. Строение и химические свойства
- •3.7.4. Способы получения
- •3.7.5. Физиологическая роль и Важнейшие представители
- •3.8. Нитроалканы
- •3.8.1. Строение
- •3.8.2. Свойства
- •3.8.3. Способы получения
- •3.8.4. Физиологическое действие и Важнейшие представители
- •3.9. Кремний-, фосфор- и мышьякорганические соединения
- •3.9.1. Кремнийорганические соединения
- •3.9.2. Фосфорорганические соединения
- •3.9.3. Мышьякорганические соединения
- •Глава 4. Непредельные углеводороды
- •4.1. ОБщность строения и химических свойств
- •4.1.1. Реакции электрофильного присоединения
- •4.1.2. Реакции радикального присоединения
- •4.1.3. Реакции радикального замещения
- •4.1.4. Другие реакции
- •4.2. Этиленовые углеводороды
- •4.2.1. Номенклатура, изомерия
- •4.2.2. Физические свойства
- •4.2.3. Химические свойства
- •4.2.4. Способы получения
- •4.2.5. Физиологическое действие и Важнейшие представители
- •4.3. Диеновые (и полиеновые) углеводороды
- •4.3.1. Классификация, номенклатура
- •4.3.5. Способы получения
- •4.3.6. Важнейшие представители
- •4.4. Ацетиленовые углеводороды
- •4.4.1. Номенклатура, изомерия
- •4.4.2. Особенности строения и свойств
- •4.4.3. Способы получения
- •4.4.4. Физиологическое действие и Важнейшие представители
- •Глава 5. Функциональные производные непредельнЫх углеводороДов
- •5.1. ОБщность строения и химических свойств
- •5.1.1. Классификация
- •5.1.2. Субстраты винильного типа
- •5.1.3. Субстраты аллильного типа
- •5.2. Галогеналкены
- •5.2.1. Винилгалогениды
- •5.2.2. Аллилгалогениды
- •5.2.3. Способы получения
- •5.2.4. Важнейшие представители
- •5.3. Непредельные спирты и эфиры
- •5.3.1. Виниловый спирт и его эфиры
- •5.3.2. Аллиловый и пропаргиловый спирты
- •5.3.3. Способы получения
- •5.3.4. Важнейшие представители
- •Глава 6. Алифатические альдегиды, кетоны и карбоновые кислоты
- •6.1. Насыщенные альдегиды и кетоны
- •6.1.1. Изомерия, номенклатура
- •6.1.2. Строение карбонильной группы
- •6.1.3. Физические свойства
- •6.1.4. Химические свойства
- •6.1.5. Способы получения
- •6.1.6. Физиологическая роль
- •6.1.7. Важнейшие представители
- •6.2. Непредельные альдегиды и кетоны
- •6.2.1. Кетен
- •6.2.2. Непредельные карбонильные соединения
- •Примерами соединений с сопряжёнными -связями являются
- •6.2.3. Важнейшие представители
- •6.3. Дикарбонильные соединения
- •6.3.3. Важнейшие представители
- •6.4. Насыщенные монокарбоновые кислоты и их производные
- •6.4.1. Номенклатура
- •6.4.2. Строение функциональной группы
- •6.4.3. Физические свойства
- •6.4.4. Химические свойства
- •6.4.5. Способы получения
- •6.4.6. Пероксикарбоновые кислоты и ацилпероксиды
- •6.4.7. Физиологическая роль и Важнейшие представители
- •6.5. Непредельные монокарбоновые кислоты
- •6.5.1. Номенклатура, изомерия
- •6.5.2. Строение
- •6.5.3. Химические свойства
- •6.5.4. Способы получения
- •6.5.5. Физиологическая роль и Важнейшие представители
- •6.5.6. Омыляемые липиды
- •6.6. Дикарбоновые кислоты и их производные
- •6.6.1. Особенности химического поведения
- •6.6.2. Малоновый эфир и синтезы на его основе
- •2 H5c2ooc-ch2-cooc2h5
- •2 H5c2ooc-ch2-cooc2h5
- •6.6.3. Способы получения
- •2 Rooc-(ch2)n-сoo¯ 2 rooc-(ch2)n-сoo rooc-(ch2)2n-coor hooc-(ch2)2n-cooh
- •6.6.4. Важнейшие представители
- •6.7. Гидроксикислоты
- •6.7.1. Классификация, номенклатура, изомерия
- •6.7.2. Химические свойства
- •6.7.3. Способы получения
- •6.7.4. Физиологическая роль и Важнейшие представители
- •6.8. Оксокислоты
- •6.8.1. Особенности химического поведения
- •6.8.2. Ацетоуксусный эфир и синтезы на его основе
- •6.8.3. Способы получения
- •6.8.4. Важнейшие представители
- •6.9. Аминокарбоновые кислоты. Пептиды
- •6.9.1. Классификация, номенклатура, изомерия аминокислот
- •6.9.2. Строение, физические и Химические свойства
- •6.9.3. Способы получения аминокислот
- •6.9.4. Важнейшие представители аминокислот
- •6.9.5. Пептиды
- •Глава 7. Углеводы
- •7.1. Моносахариды
- •7.1.1. Изомерия, номенклатура
- •7.1.2. Химические свойства
- •7.1.3. Важнейшие представители моносахаридов и их производных
- •7.2. Олигосахариды
- •7.2.1. Классификация и номенклатура дисахаридов
- •7.2.2. Химические свойства дисахаридов
- •7.2.3. Важнейшие представители дисахаридов
- •7.3. Полисахариды
- •7.3.1. Целлюлоза
- •7.3.2. Амилоза и амилопектин
- •7.3.3. Гликоген
- •7.3.4. Декстраны
- •7.3.5. Хитин
- •7.3.6. Пектовая кислота
- •7.3.7. Гетерополисахариды
- •Глава 8. Алициклические углеводороды и их производные
- •8.1. Номенклатура моно- и бициклических соединений
- •8.2. Пространственное строение и изомерия циклоалканов
- •8.2.1. Циклопропан
- •8.2.2. Циклобутан
- •8.2.3. Циклопентан
- •8.2.4. Циклогексан
- •8.3. Химические свойства
- •8.3.1. Реакции циклопропана, циклопропена и их производных
- •8.3.2. Реакции циклобутана и его производных
- •8.3.3. Реакции средних циклов
- •8.3.4. Реакции изомеризации цикла
- •8.4. Способы получения циклоалканов
- •8.5. Терпены и терпеноиды. Каротиноиды
- •8.5.1. Ациклические терпены и терпеноиды
- •8.5.2. Моноциклические терпены и терпеноиды
- •8.5.3. Бициклические терпены и терпеноиды
- •8.5.4. Каротиноиды
- •8.6. Физиологическая роль и важнейшие представители
- •8.7. Стероиды
- •Глава 9. Бензол. Ароматичность. Углеводороды ряда бензола
- •9.1. Строение бензола
- •Тепловой эффект реакции гидрирования бензола составляет
- •9.2. Номенклатура и изомерия аренов
- •9.3. Строение аренов
- •9.3.1. Строение толуола
- •9.3.2. Строение винилбензола
- •9.4. Физические свойства
- •9.5. Химические Свойства
- •9.5.1. Химические свойства бензола
- •9.5.2. Химические свойства аренов
- •9.6. Способы получения
- •9.7. Физиологическое действие и важнейшие представители аренов
- •9.8. Небензоидные ароматические системы
- •Глава 10. Функциональные производные углеводородов ряда бензола
- •10.1. Общность строения и свойств монозамещённых бензолов
- •10.1.1. Электронные эффекты заместителей
- •10.1.2. Реакции электрофильного замещения
- •10.1.3. Реакции нуклеофильного замещения
- •10.2. Галогенарены
- •10.2.1. Классификация, номенклатура
- •10.2.2. Строение арилгалогенидов
- •10.2.3. Физические свойства
- •10.2.4. Химические свойства
- •10.2.5. Способы получения
- •10.2.6. Важнейшие представители
- •10.3. Ароматические сульфокислоты
- •10.3.1. Номенклатура
- •10.3.2. Строение
- •10.3.3. Физические и химические свойства
- •10.3.4. Способы получения
- •10.3.5. Производные сульфокислот
- •10.3.6. Медико-биологическое значение и Важнейшие представители
- •10.4. Ароматические нитросоединения
- •10.4.1. Строение нитробензола
- •10.4.2. Физические свойства
- •10.4.3. Химические свойства
- •10.4.4. Способы получения
- •10.4.5. Физиологическое действие и Важнейшие представители
- •10.5. Фенолы. Ароматические спирты. Хиноны
- •10.5.1. Классификация, номенклатура, изомерия фенолов и ароматических спиртов
- •10.5.2. Строение фенола и бензилового спирта
- •Ароматические амины и продукты неполного восстановления нитросоединений
- •10.6.1. Классификация, номенклатура, изомерия ароматических аминов
- •10.6.2. Строение анилина
- •10.6.3. Физические и химические свойства ароматических аминов
- •10.6.4. Способы получения ароматических аминов
- •10.6.5. Важнейшие представители ароматических аминов
- •10.6.6. Продукты неполного восстановления нитросоединений
- •10.7. Ароматические диазосоединения
- •10.7.2. Механизм образования солей арендиазония и строение катиона бензолдиазония
- •10.7.3. Амфотерность диазосоединений
- •10.7.4. Реакции солей арендиазония
- •10.8. Ароматические альдегиды и кетоны
- •10.9. Ароматические карбоновые кислоты и их производные
- •10.10. Физиологическая роль функциональных производных бензола
- •Глава 11. Полициклические ароматические углеводороды и их производные
- •11.1. Классификация углеводородов с конденсированными циклами
- •11.2. Нафталин
- •11.2.1. Строение, изомерия, номенклатура
- •11.2.2. Свойства
- •11.2.3. Способы получения
- •11.2.4. Важнейшие представители
- •11.3. Антрацен
- •11.3.1. Строение, изомерия, номенклатура
- •11.3.2. Свойства
- •Продукт исчерпывающего гидрирования (пергидроантрацен) можно получить, проводя реакцию в жёстких условиях с применением металлических катализаторов.
- •11.3.3. Способы получения
- •11.3.4. Важнейшие представители
- •11.4. Фенантрен
- •11.4.1. Строение, изомерия, номенклатура
- •11.4.2. Свойства
- •11.4.3. Способы получения
- •11.5. Физиологическое действие полициклических углеводородов
- •Глава 12. Гетероциклические соединения
- •12.1. Классификация и номенклатура
- •12.2. Пятичленные гетероциклические
- •12.2.1. Номенклатура пиррола, фурана и тиофена и их производных
- •12.2.2. Строение пиррола, фурана и тиофена
- •12.2.3. Физические и химические свойства пиррола, фурана и тиофена
- •12.2.4. Особенности индола
- •12.2.5. Способы получения пиррола, фурана, тиофена, индола
- •12.2.6. Важнейшие представители и медико-биологическое значение
- •12.3. Пятичленные гетероциклические
- •12.3.1. Номенклатура имидазола и пиразола
- •12.3.2. Строение имидазола и пиразола
- •12.3.3. Физические и химические свойства имидазола и пиразола
- •12.3.4. Способы получения
- •12.3.5. Важнейшие представители и медико-биологическое значение
- •12.4. Шестичленные гетероциклические
- •12.4.1. Номенклатура пиридина и его производных
- •12.4.2. Строение пиридина
- •12.4.3. Химические свойства пиридина
- •Но если оба -положения заняты, то замещается водород в-положении. При нагревании с избытком амида натрия можно получить 2,6-диаминопиридин.
- •12.4.4. Особенности химического поведения пиколинов и функциональных производных пиридина
- •12.4.5. Хинолин и изохинолин
- •12.4.7. Способы получения
- •Реакция аналогична получению бензола, протекает при высоких температурах, но представляет только теоретический интерес.
- •12.4.8. Важнейшие представители и медико-биологическое значение
- •12.5. Шестичленные гетероциклические
- •12.5.1. Строение и свойства диазинов
- •12.5.2. Пурин
- •12.5.3. Способы получения
- •12.5.4. Важнейшие представители и медико-биологическое значение
- •12.5.5. Нуклеозиды, нуклеотиды и нуклеиновые кислоты
- •12.6. Алкалоиды
1.7. Основы стереохимии
Стереохимия — это учение о пространственном расположении атомов в молекуле. Оно исследует пространственное строение молекул и влияние его на физические и химические свойства веществ. Поэтому различают статическую стереохимию, занимающуюся проблемами стереоизомерии, и динамическую. Динамическая стереохимия изучает пространственные закономерности химических реакций. Здесь имеют значение размеры атомов, длины и углы связей. В настоящее время эта область развивается особенно плодотворно, и при рассмотрении химических свойств веществ каждого класса органических соединений необходимо учитывать пространственные возможности молекул.
Но основу стереохимии составляет прежде всего статическая стереохимия. Поэтому далее необходимо рассмотреть пространственную изомерию (то есть стереоизомерию).
Явление изомерии состоит в том, что могут существовать несколько отличных друг от друга по свойствам веществ, имеющих один и тот же состав и одну и ту же молекулярную массу. Эти вещества называют изомерами. Явления структурной изомерии довольно-таки подробно изучаются в школьном курсе органической химии. Там рассматриваются её разновидности — скелетная изомерия (или изомерия углеродного скелета), например, бутан и изобутан, и позиционная изомерия (или изомерия положения функциональной группы или кратной связи), например, 1-хлорпропан и 2-хлорпропан.
Стереоизомерия — изомерия, вызванная различиями в пространственном расположении атомов в молекулах. Выделяют два вида пространственной изомерии: конфигурационную и конформационную. Конфигурация — закономерность или порядок расположения в пространстве атомов или атомных группировок относительно другого атома, двойной связи и некоторых других структурных элементов. Для превращения одного конфигурационного изомера в другой необходим разрыв химических связей и образование новых связей в молекуле. Конформация — порядок пространственного расположения атомов в молекуле, обусловленный их внутренним вращением вокруг одинарных связей.
Конфигурационную изомерию подразделяют на оптическую и геометрическую.
1.7.1. Оптическая изомерия
Многие органические соединения, в том числе и алканы, начиная с изомеров гептана, проявляют оптическую активность, то есть способность вращать плоскость поляризации света. Свет представляет собой электромагнитные волны, колебания которых перпендикулярны направлению их распространения. В естественном свете такие колебания происходят в разных плоскостях, а в поляризованном — только в одной плоскости.
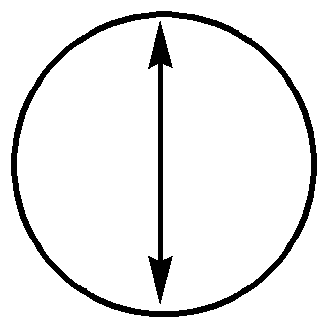

поляризованный свет неполяризованный свет
(стрелками обозначена плоскость электромагнитных колебаний)
При прохождении луча плоскополяризованного света через раствор оптически активного вещества плоскость поляризации этого луча отклоняется на некоторый угол , то есть происходит поворот луча плоскополяризованного света.
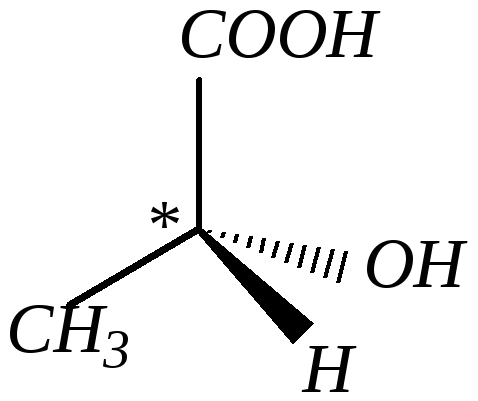
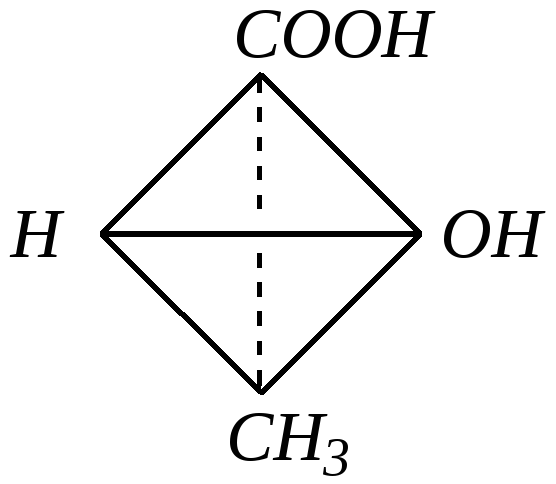
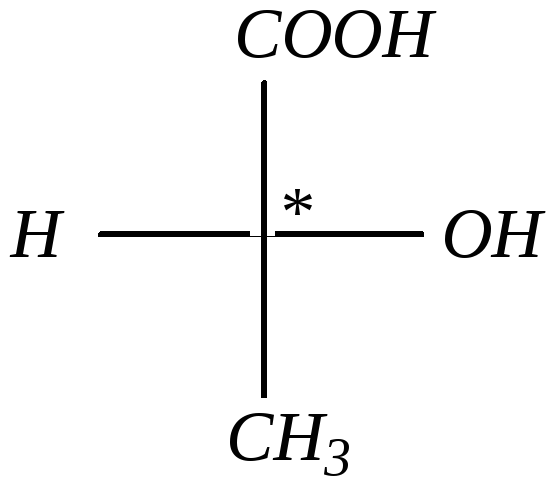
Оптическая активность веществ связана с наличием в их молекулах атомов углерода, имеющих четыре разных заместителя и называющихся асимметрическими или хиральными (от греческого — рука). Оптическая изомерия обусловлена различным расположением в пространстве заместителей при асимметрическом атоме углерода. Например, в молекуле
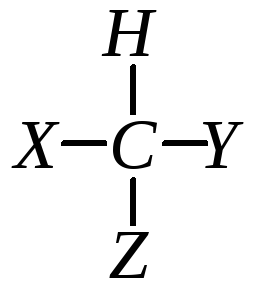
атом углерода связан -связями с четырьмя различными заместителями, то есть он находится в центре тетраэдра. Но такой структурной формуле могут соответствовать две разных пространственных:
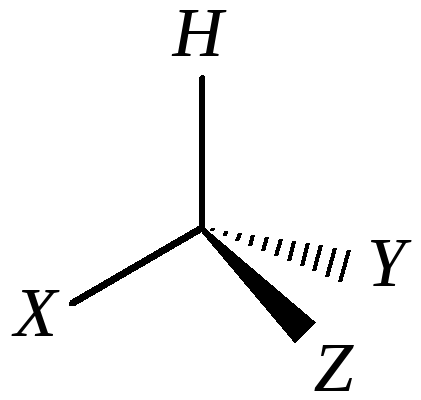 и
и

Они не идентичны друг другу, поскольку их невозможно совместить, но они являются зеркальным отображением друг друга. Молекулы, имеющие такие пространственные формулы, называются энантиомерами или зеркальными изомерами. Энантиомеры поворачивают луч плоскополяризованного света на один и тот же угол, но в разные стороны. Для обозначения правовращающего изомера используют знак (+), левовращающего — знак (–).
хиральный атом углерода в составе молекулы иногда обозначают звёздочкой «*», например, C*HXYZ. Молекулы, имеющие в своем составе хиральный атом углерода, также называются хиральными.
Необходимым условием появления таких пространственных изомеров является наличие четырёх различных заместителей у тетраэдрического углерода. Если среди окружения атома углерода будут хотя бы две одинаковые атомные группировки
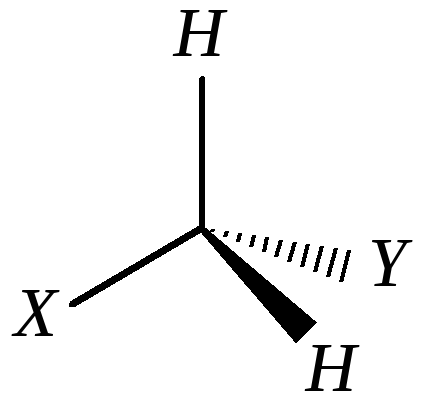 ,
,
то молекула не будет хиральна, так как зеркальное изображение её в пространстве можно совместить с оригиналом, оптическая изомерия отсутствует.
Для различия названий пространственных изомеров Р. Кан*, К. Ингольд* и В. Прелог* в 1951 году разработали удобную систему обозначения конфигурации хиральных центров молекул. В этой системе первоначально определяют порядок старшинства заместителей у хирального центра. Чем больше порядковый номер химического элемента в периодической таблице, тем старше заместитель. Затем располагают модель молекулы так, чтобы самый младший заместитель был удалён от наблюдателя, а остальные три — приближены к нему. Если атомные номера этих трёх заместителей убывают по часовой стрелке, конфигурацию обозначают буквой R (от латинского rectus – правый), если против часовой стрелки — буквой S (от латинского sinister – левый). например, для энантиомеров бромфторхлорметана CHBrFCl это будет выглядеть так:

(R)-бромфторхлорметан (S)-бромфторхлорметан
В случае более сложных заместителей их старшинство определяется порядковым номером первого атома (т.е. непосредственно связанного с хиральным центром). Если же первые атомы одинаковы, то старшинство между этими заместителями устанавливается по вторым атомам и т.д.
Таким образом, по системе Кана–Ингольда–Прелога можно установить R- или S-конфигурацию любого оптического изомера, в том числе и среди углеводородов. Например, для простейшего из алканов, молекулы которого обладают хиральностью, пространственное расположение заместителей вокруг асимметрического атома углерода может быть таким:
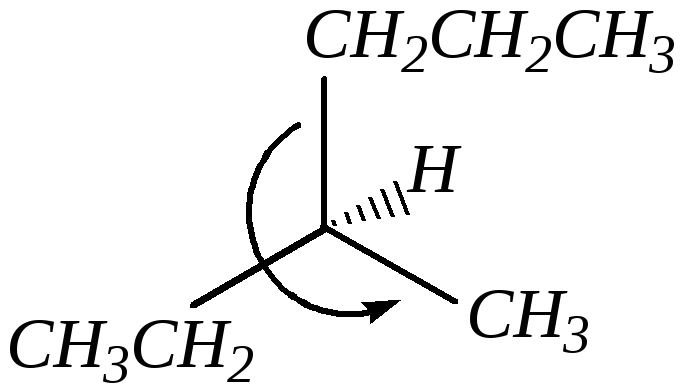
(S)-3-метилгексан
данная система определения конфигурации (R- или S-) является абсолютной. Существует ещё система определения относительной конфигурации (D- или L-) по конфигурации соответственно D- или L-глицеринового альдегида. Но она пригодна далеко не для всех веществ и широко применяется для аминокислот, сахаров, гидроксикислот, родственных им соединений, природных веществ, обладающих оптической активностью.
Для этого строение молекулы данного оптического изомера изображают при помощи проекционных формул, предложенных в 1890 году немецким химиком Э. Фишером* первоначально для углеводов. Для перевода тетраэдрических изображений в плоскостные руководствуются следующими правилами.
наиболее длинную углеродную цепь молекулы (но обязательно содержащую хиральный центр) располагают вертикально, при этом наиболее окисленный атом углерода должен быть наверху, или более строго — чтобы нумерация атомов в этой цепи по заместительной номенклатуре осуществлялась сверху вниз.
два других заместителя хирального атома углерода, находящиеся в тетраэдрическом изображении на переднем плане, располагают горизонтально.
тетраэдр проецируют на плоскость, то есть как бы сплющивают.
Применим эти правила для изображения проекционной формулы одного из оптических изомеров молочной кислоты CH3-C*HOH-COOH
|
|
|
|
|
|
Для определения относительной конфигурации сравнивают расположение атома водорода и гидроксигруппы у хирального центра с расположением этих же групп в молекуле D- или L-глицеринового альдегида, взятого за своеобразный стандарт:
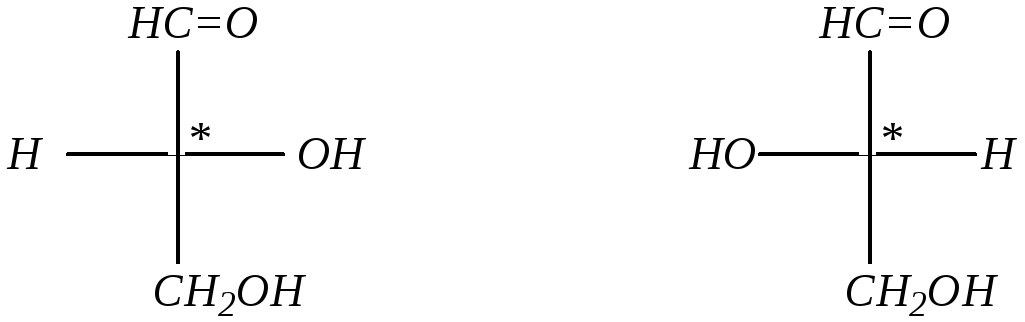
D-глицериновый альдегид L-глицериновый альдегид
В нашем примере, таким образом, оптический изомер молочной кислоты относится к D-ряду. Соответственно, может существовать и другой оптический изомер, имеющий иное расположение атома водорода и ОН-группы относительно асимметрического центра:
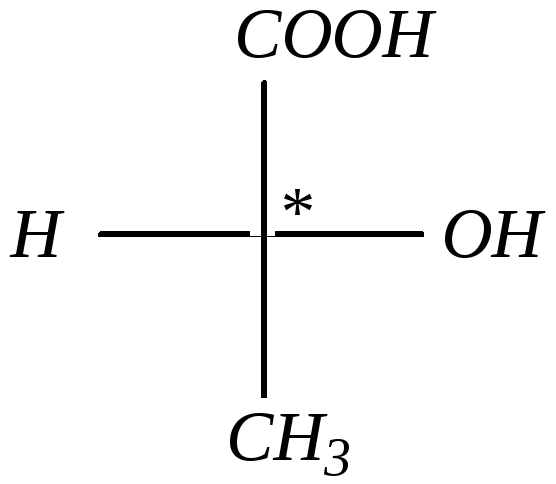 и
и
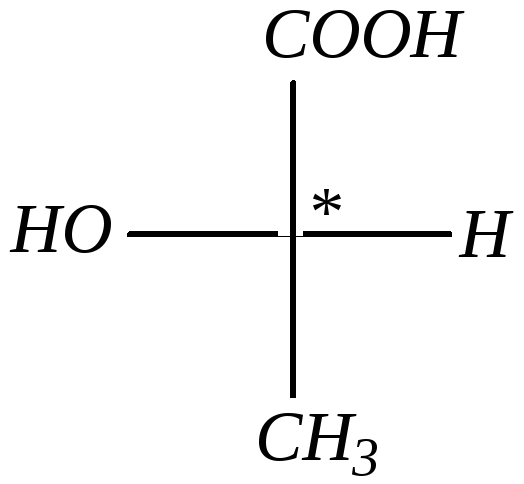
D-молочная кислота L-молочная кислота
Формулы Фишера можно как угодно поворачивать в плоскости листа, но нельзя вынимать из плоскости и переворачивать. Этим они отличаются от обычных структурных формул.
Смесь равных количеств двух энантиомеров называется рацемической смесью или рацематом. Рацемат представляет либо механическую смесь двух изомеров, либо новый продукт, образовавшийся при их взаимодействии. Рацематы обладают физическими свойствами, отличными от свойств обоих энантиомеров. Они оптически не активны; можно представить, что оптическая активность одного антипода нейтрализуется противоположной оптической активностью другого.
При наличии в молекуле нескольких асимметрических атомов число оптических изомеров увеличивается. При этом при числе асимметрических центров n максимальное количество оптических изомеров N вычисляется по формуле: N = 2n. В качестве примера оптически активного соединения с несколькими хиральными атомами углерода можно взять 2,3-дигидроксибутановую кислоту CH3-C*HOH-C*HOH-COOH. Здесь два хиральных центра и, следовательно, должно быть четыре оптических изомера. Изобразим их с помощью проекционных формул Фишера.
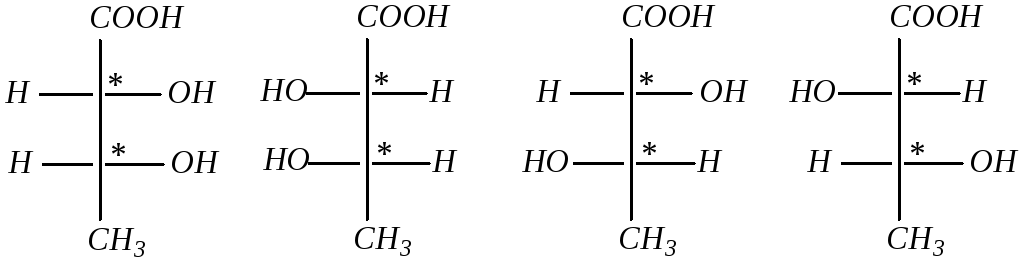
(1) (2) (3) (4)
Изомеры 1 и 2 по отношению друг к другу, а также 3 и 4 по отношению друг к другу являются антиподами, то есть зеркальным отображением друг друга. А оптические изомеры 1 и 3, 1 и 4, 2 и 3, 2 и 4 не являются оптическими антиподами. Такие оптические изомеры называются диастереомерами. В отличие от антиподов диастереомеры имеют различные физические свойства, так как в их молекулах отдельные фрагменты по-разному располагаются относительно друг друга.
Для различия стереоизомеров, содержащих два хиральных центра, используют также названия эритро-форма и трео-форма. Эритро-изомерами называются те, в проекционных формулах которых боковые неводородные заместители находятся на одной стороне; трео-изомеры имеют боковые заместители на разных сторонах проекционных формул. Так, из вышеприведённых примеров стереоизомерных 2,3-дигидроксибутановых кислот формулы 1 и 2 относятся к эритро-изомерам, a формулы 3 и 4 — к трео-изомерам.
Поскольку диастереомеры различаются по физическим свойствам, разделение их смесей обычно не вызывает затруднений. Для этого используют различия в растворимости (разделение кристаллизацией), различие в температурах кипения (разделение перегонкой), различия в адсорбционной способности (разделение с помощью различных хроматографических методов). В отличие от этого энантиомеры различаются только направлением вращения луча плоскополяризованного света, ни по каким другим свойствам они не различимы и, следовательно, никакими обычными физическими методами разделить пару оптических антиподов непосредственно нельзя.
В основе почти всех современных методов разделения рацематов лежат классические работы Л. Пастера. Эти работы дали следующие основные методы разделения рацемических смесей:
1. Механический способ применим, если при кристаллизации энантиомеры образуют кристаллы различной формы. Разделение проводят при помощи лупы и пинцета. Путём механического отбора кристаллов Пастер в 1848 году впервые выделил оптически активное вещество.
2. Биологический способ заключается в преимущественном разрушении микроорганизмами только одного из оптических антиподов. При этом если действию микроорганизмов подвергается рацемат, то за счёт разрушения одного антипода другой энантиомер накапливается в чистом виде. В 1857 году Пастер наблюдал поглощение D-винной кислоты плесневым грибком Penicillum glaucum.
3. Химический способ заключается в образовании диастереомеров или, как вариант, молекулярных комплексов. Практически наиболее важным является способ разделения через диастереомеры. Сущность этого метода может быть выражена схемой:
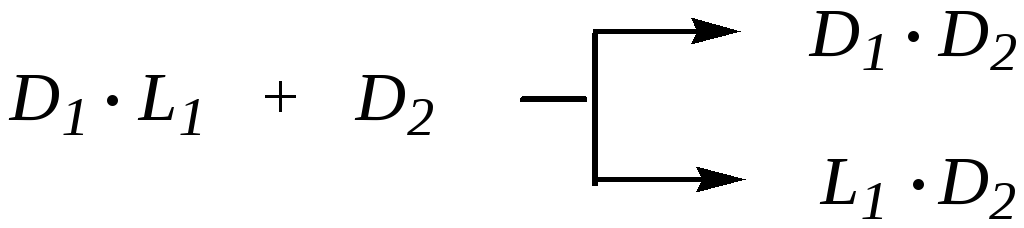
Рацемическая смесь D1L1 подвергается действию оптически активного реагента D2. При этом образуется новая пара веществ D1D2 и L1D2, являющихся диастереомерами по отношению друг к другу. Диастереомеры можно разделить на основании различия их физических свойств (см. выше).
Примером может служить расщепление рацемической смеси D- и L-молочных кислот с помощью оптически активного амина:
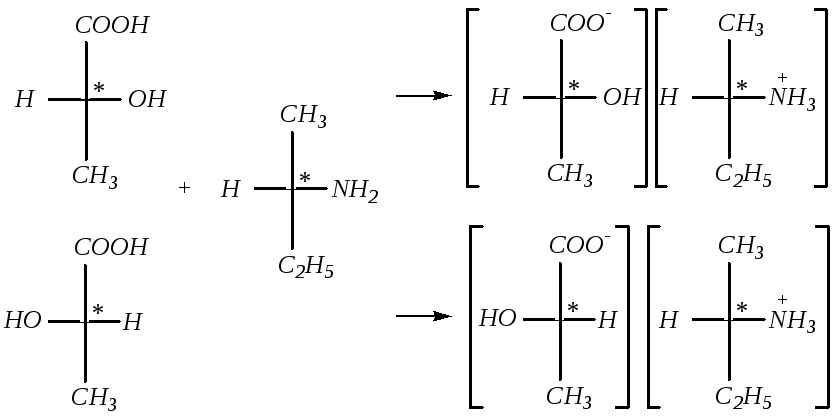
Образующиеся соли диастереомерны, обладают разной растворимостью, на основании чего и могут быть разделены.