
- •Программа курса
- •Тема 1. Моль. Эквиваленты простых и сложных веществ. Закон эквивалентов
- •Контрольные вопросы и задачи
- •Тема 2. Периодическая система элементов д.И. Менделеева
- •Контрольные вопросы и задачи
- •Тема 3. Химическая связь. Строение молекул Контрольные вопросы и задачи
- •Тема 4. Энергетика химических процессов. Внутренняя энергия. Энтальпия
- •Контрольные вопросы и задачи
- •Тема 5. Энтропия. Энергия Гиббса. Направленность химических реакций
- •Контрольные вопросы и задачи
- •Тема 6. Растворы
- •Контрольные вопросы и задачи
- •Тема 7. Окислитeльнo-вoccтaнoвитeльньIe реакции
- •Контрольные вопросы и задачи
- •Тема 8. Электрохимические системы. Электродные потенциалы. Электродвижущие силы. Химические источники тока
- •Контрольные вопросы и задачи.
- •Тема 9. Электролиз
- •Контрольные вопросы и задачи
- •Тема 10. Коррозия металлов
- •Контрольные вопросы и задачи.
- •Тема 11. Жесткость воды
- •Классификация воды по уровню жесткости
- •Решение.
- •Контрольные вопросы и задачи
- •Тема 12. Комплексные соединения
- •В соответствии с уравнением равновесия суммарной реакции диссоциации комплекса константу нестойкости можно выразить уравнением:
- •Контрольные вопросы и задачи
- •Приложение
- •Рекомендательный библиографический список
Тема 6. Растворы
Способы выражения концентрации растворов
Концентрацией раствора называется количество растворенного вещества, содержащееся в определенном массовом или объемном количестве раствора или растворителя.
Пример 1.
Вычислите: а) процентную (С%); б) молярную (CМ); в) нормальную (Cн); г) моляльную (Cm) концентрации раствора Н3РO4, полученного при растворении 18 г кислоты в 283 см3воды, если плотность его 1,031 г/см3. Чему равен титр (Т) этого раствора?
Решение:
а) массовая процентная концентрация показывает число граммов (единиц массы) вещества, содержащееся в 100 г (единиц массы) раствора. Так как массу 282 см3воды можно принять равной 282 г, то масса полученного раствора 18 + 282 = 300 г и, следовательно:
300 г составляют 100 %
18 г составляют х %
![]() .
.
б) мольно-объемная концентрация, или молярность показывает число молей растворенного вещества, содержащихся в 1 л раствора. Масса 1 л раствора 1031 г. Массу кислоты в литре раствора находим из соотношения:
в 300 г раствора содержится 18 г растворённого вещества,
в 1031 г раствора – хг растворённого вещества.
![]()
Молярность раствора получим делением числа граммов Н3РO4в 1 л раствора на мольную массу Н3РO4(97,99 г/моль):
CМ = 61,86 / 97,99 = 0,63 М;
в) нормальная концентрация, или нормальность показывает число молей эквивалентов растворенного вещества, содержащихся в 1 л раствора.
Так как мольная масса эквивалентов ортофосфорной кислоты Н3РO4= М/3 = 97,99/3 = 32,66 г/моль, тоCH= 61,86 / 32,66 = 1,89 н.;
г) мольно-массовая концентрация, или моляльность показывает число молей растворенного вещества, содержащихся в 1000 г растворителя. Массу Н3РO4в 1000 г растворителя находим из соотношения:
в 282 г растворителя находится 18 г растворённого вещества,
в 1000 г растворителя – хг растворённого вещества;
![]() Отсюда
Cm= 63,83 /97 = 0,65m;
Отсюда
Cm= 63,83 /97 = 0,65m;
г) титром раствора называется количество граммов растворенного вещества в 1см3(мл) раствора. Так как в 1 л раствора содержится 61,86 г кислоты, то
T= 61,86 / 1000 = 0,06186 г/см3.
Зная нормальность раствора и мольную массу эквивалентов (МЭ) растворенного вещества, титр легко найти по формуле
Т = СH ∙МЭ/ 1000.
Пример 2.
На нейтрализацию 50 см3 раствора кислоты израсходовано 25 см3 0,5 н. раствора щелочи. Чему равна нормальность кислоты?
Решение.
Так как вещества взаимодействуют между собой в эквивалентных количествах, то растворы равной нормальности реагируют в разных объемах. При разных нормальностях объемы растворов реагирующих веществ обратно пропорциональны их нормальностям, т.е.
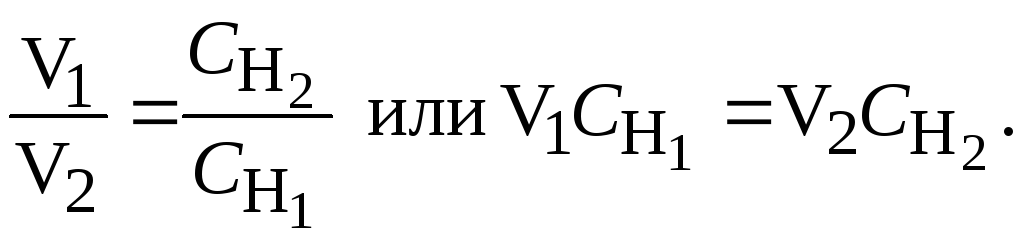
![]()
Пример 3.
К 1 л 10%-го раствора КОН (= 1,092 г/см3) прибавили 0,5 л 5%-го раствора КОН (= 1,045 г/см3). Объем смеси довели до 2 л. Вычислите молярную концентрацию полученного раствора.
Решение.
Масса одного литра 10%-го раствора КОН 1092 г. В этом растворе содержится
![]()
Масса 0,5 л 5%-го раствора 1045∙0,5 = 522,5 г. В этом растворе содержится
![]()
В общем объеме полученного раствора (2 л) масса КОН составляет 109,2 + 26,125=135,325 г. Отсюда молярность этого раствора
![]() где 56,1 г/моль –
мольная масса КОН.
где 56,1 г/моль –
мольная масса КОН.
Пример 4.
Какой объем 96%-ной кислоты, плотность которой 1,84 г/см3, потребуется для приготовления 3 л. 0,4 н. раствора?
Решение.
Мольная эквивалентность H2SO4 = M/2 = 98,08/2 = 49,04 г/моль. Для приготовления 3 л. 0,4 н. раствора требуется 49,04 ∙ 0,4 ∙ 3 = 58,848 г. H2SO4. Масса 1 см3 96%-ной кислоты 1,84 г. В этом растворе содержится 1,84∙96/100 = 1,766 г. H2SO4.
Следовательно, для приготовления 3 л. 0,4 н. раствора надо взять 58,848/1,766 = 33,32 см3этой кислоты.
