
ВНЕДРЕНИЕ СМК В МЕДИЦИНСКИХ ОРГАНИЗАЦИЯХ
.pdf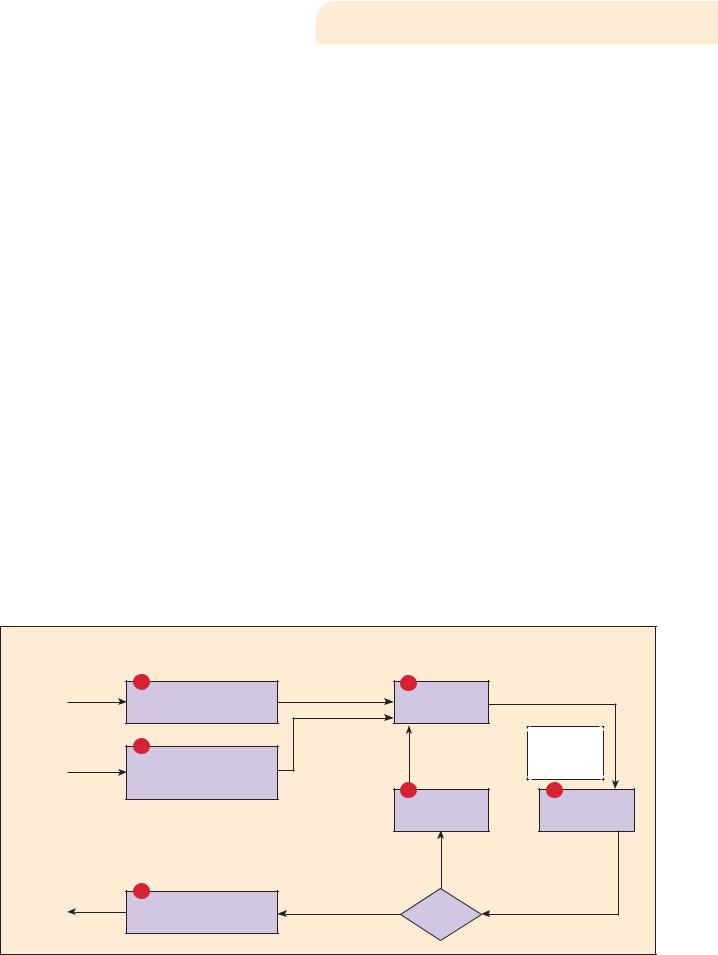
|
|
|
|
|
|
УПРАВЛЕНИЕ КАЧЕСТВОМ В ФАРМАЦИИ |
|
|||||
Документированная СМК — это модель, которая описыва- |
ства, характеристики сырья и материалов, процедуры вы- |
|
||||||||||
ет деятельность организации в соответствии с требования- |
полнения отдельных видов операций. |
|
|
|
||||||||
ми ГОСТ Р ИСО 9001-2008, ГОСТ Р 52249-2009. |
|
3. Организационно-распорядительная документация (ОРД). |
|
|||||||||
Документация дает возможность передать смысл и по- |
4. Записи — информационные и справочные документы |
|
||||||||||
следовательность действий, зафиксировать распределение |
(документы, установленные для представления свидетельств |
|
||||||||||
обязанностей, полномочий и ответственности персонала, |
соответствия требованиям, получения объективных доказа- |
|
||||||||||
взаимодействие между сотрудниками и подразделениями, |
тельств о проделанной работе и достигнутых результатах). |
|
|
|||||||||
информационные потоки, а также документирование вы- |
5. Нормативные и законодательные документы внешне- |
|
||||||||||
полненных работ. Ее применение способствует достижению |
го происхождения — документы, выпущенные внешними |
|
||||||||||
соответствия требованиям потребителя и улучшению каче- |
органами. |
|
|
|
|
|
|
|
||||
ства, обеспечению подготовки кадров, идентификации и |
Документы каждого уровня дают ответы на конкретные |
|
||||||||||
прослеживаемости, получению объективных доказательств |
вопросы. Содержание документов в зависимости от группы |
|
||||||||||
при оценке эффективности и результативности СМК. Схема |
и вопросы,на которые дают ответы документы каждой груп- |
|
||||||||||
управления документации внутреннего и внешнего проис- |
пы, представлены в таблице 1. |
|
|
|
|
|||||||
хождения представлена на рисунке 1. |
|
|
|
|
|
|
|
|
|
|
||
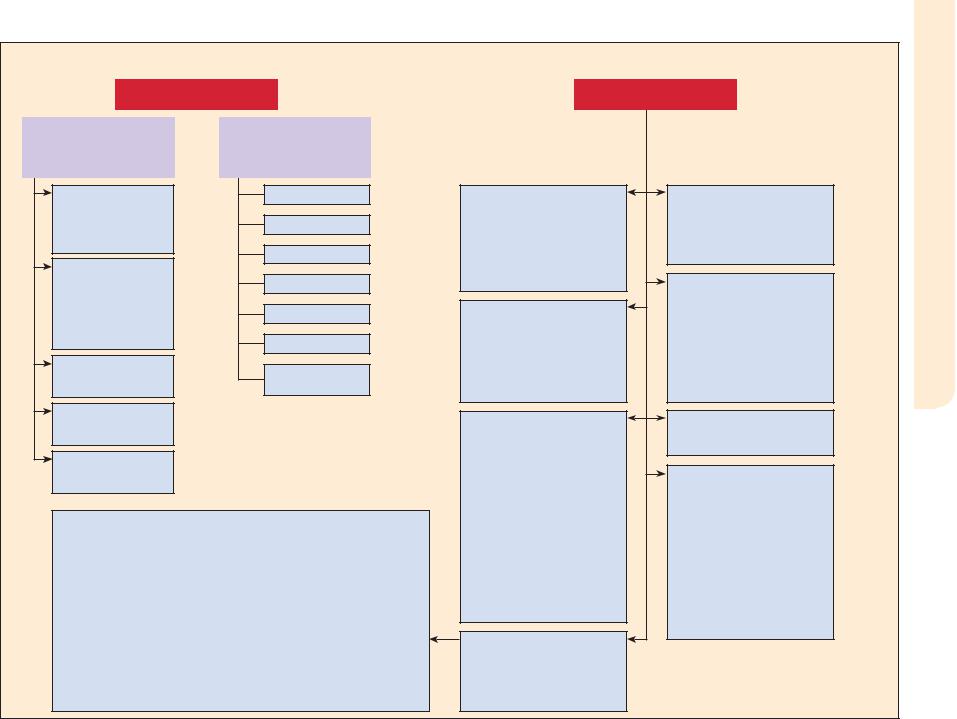
Все документы системы обеспечения качества можно |
|
|
|
|
|
|
|
|
||||
объединить в пять больших групп (см. «Классификатор до- |
ОПРЕДЕЛЕНИЕ ОТВЕТСТВЕННОСТИ ПОДДЕРЖАНИЯ |
|
|
|||||||||
кументов», рис. 2). |
|
|
|
СИСТЕМЫ ДОКУМЕНТАЦИИ |
|
|
|
|
|
|||
1. Описывающие систему менеджмента качества — ре- |
|
|
|
|
|
|
|
|
||||
гламентирующие документы, разрабатываемые на пред- |
Определение ответственности за поддержание системы |
|
||||||||||
приятии. Они включают нормативные документы, регла- |
документации |
на |
предприятии |
в |
соответствии |
с |
|
|||||
ментирующие производственную деятельность предприя- |
ГОСТ Р 52249-2009 «Правила производства и контроля ка- |
|
||||||||||
тия: описание информации о предприятии (требования к |
чества лекарственных средств» возложены на отдел обе- |
|
||||||||||
системе управления качеством, контролю качества, персо- |
спечения качества. |
|
|
|
|
|
|
|||||
налу, помещениям и оборудованию, документации, произ- |
Определение ответственности зависит от структуры пред- |
|
||||||||||
водству продукции и проведению анализов по контрактам, |
приятия, его размеров и характера деятельности. Схема, |
|
||||||||||
рекламациям, порядку отзыва продукции и организации са- |
представленная в таблице 2, распределяет ответственность |
|
||||||||||
моинспекций (внутренних аудитов)). |
|
|
следующим образом: |
|
|
|
|
|
|
|||
2. Нормативные документы (НД) — документы, регла- |
директор — определение миссии, политики, целей и за- |
|
||||||||||
ментирующие |
процесс |
производства |
лекарственных |
дач предприятия в области качества, утверждение доку- |
|
|||||||
средств: стандарты, содержащие перечень показателей и |
ментов предприятия; |
|
|
|
|
|
|
|||||
методов контроля качества лекарственного средства, ха- |
представитель руководства по качеству (директор по |
|
||||||||||
рактеристики лекарственного средства, схемы производ- |
качеству) — общее руководство, постановка задач и кон- |
|
||||||||||
Рисунок 1. Схема процесса управления документацией внутреннего и внешнего происхождения [11] |
|
|
|
|
|
|||||||
Информация о потребности |
|
|
|
|
|
|
|
|
|
|
|
|
в разработке внутренних |
1А |
|
|
2 |
|
|
|
|
|
|
|
|
|
документов |
РАЗРАБОТКА |
|
Утвержденный документ |
ВНЕДРЕНИЕ |
Зарегистрированный документ |
|
|
||||
|
|
|
|
|
|
|
||||||
|
|
ВНУТРЕННЕГО ДОКУМЕНТА |
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
Документ |
|
|
|
|
Идентификация |
|
|
|
|
|
1Б |
|
и изменения |
Листы изменений |
|
|
|
||||
|
Запросы |
|
|
мест нахождения: |
|
|
||||||
|
|
к нему |
|
|
|
|
||||||
исполнителей |
ПРИОБРЕТЕНИЕ |
|
|
и дополнений |
|
описи, дела |
|
|
||||
|
|
|
|
|
|
|||||||
|
|
ВНЕШНЕГО ДОКУМЕНТА |
|
|
или новый выпуск |
|
(папки), полки |
|
|
|||
Информация о новых |
И/ИЛИ ИЗМЕНЕНИЙ К НЕМУ |
|
|
документа |
|
|
|
|
|
|
||
|
4 |
|
|
|
|
3 |
|
|
||||
и действующих внешних |
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
ПРИМЕНЕНИЕ |
|
|
||
|
документах |
|
|
|
АКТУАЛИЗАЦИЯ |
|
|
|
|
|||
|
|
|
|
|
|
|
И ПРОВЕРКА |
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
5 |
|
|
|
|
|
|
Принятие решения о |
|
|
|
|
Архив |
|
|
|
|
|
|
пересмотре или отмене |
|
|
||
|
ХРАНЕНИЕ И ИЗЪЯТИЕ |
Для отмененных zокументов |
|
|
|
внутреннего документа |
|
|
||||
Уничтожение |
ИЗ ОБРАЩЕНИЯ |
|
|
|
|
|
Проверка статуса и наличие |
|
|
|||
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
изменений во внешних документах |
|
|
||
|
|
|
|
МЕНЕДЖМЕНТ КАЧЕСТВА В СФЕРЕ ЗДРАВООХРАНЕНИЯ И СОЦИАЛЬНОГО РАЗВИТИЯ № 4 (10)/ 2011 |
79 |
|||||||
80 |
|
|
|
|
|
|
|
|
СОЦИАЛЬНОГОИ ЗДРАВООХРАНЕНИЯ СФЕРЕ В КАЧЕСТВА МЕНЕДЖМЕНТ |
Рисунок 2. Классификатор документов |
|
|
|
ФАРМАЦИИ В КАЧЕСТВОМ УПРАВЛЕНИЕ |
|||
|
|
ВНЕШНИЕ ДОКУМЕНТЫ |
ВНУТРЕННИЕ ДОКУМЕНТЫ |
|||||
|
ВХОДЯЩИЕ |
|
|
ИСХОДЯЩИЕ |
|
|
||
(документы от вышестоящих, |
|
(документы, создаваемые |
|
|
||||
подведомственных, |
на предприятии и отправляемые |
|
|
|||||
несоподчиненных организаций) |
|
за его пределы) |
|
|
||||
ГОСУДАРСТВЕННЫЕ |
|
|
ПИСЬМА |
ОРГАНИЗАЦИОННО-ПРАВОВЫЕ |
РАСПОРЯДИТЕЛЬНЫЕ |
|||
указы; |
|
|
|
устав; |
приказы по основной деятельности; |
|||
законы; |
|
|
ДОГОВОРЫ |
коллективный договор; |
указания; |
|||
постановления; |
|
|
организационная структура предприятия; |
распоряжения; |
||||
|
|
|
||||||
ГОСТы |
|
|
|
штатное расписание; |
решения; |
|||
|
|
|
|
ОБЗОРЫ |
положения о подразделениях; |
уведомления |
||
ОТРАСЛЕВЫЕ |
|
|
|
инструкции должностные и о трудо- |
|
|||
распоряжения; |
|
|
СПРАВКИ |
вых обязанностях (ДИ, ИТО) |
ИСПОЛНИТЕЛЬНЫЕ |
|||
указания; |
|
|
|
|||||
|
|
|
|
докладные записки; |
||||
приказы; |
|
|
ОТЧЕТЫ |
ДОКУМЕНТЫ ПО ПЕРСОНАЛУ |
объяснительные записки; |
|||
|
письма; |
|
|
приказы; |
служебные записки; |
|||
|
|
|
|
|||||
инструкции; |
|
|
|
трудовые контракты; |
пояснительные записки; |
|||
ОСТы, СанПиНы и пр. |
|
УВЕДОМЛЕНИЯ |
личные заявления; |
акты; |
||||
РАЗВИТИЯ |
МЕЖДУНАРОДНЫЕ |
|
|
|
личные дела; |
протоколы; |
|
|
|
|
АНКЕТЫ, |
личные карточки; |
справки; |
|
|||
|
стандарты; |
|
|
лицевые счета по зарплате; |
обзоры; |
|
||
|
|
|
ОПРОСНЫЕ ЛИСТЫ |
|
||||
требования |
|
|
заявления о приеме, увольнении |
отчеты |
|
|||
|
|
|
|
|
||||
4 № |
ИНФОРМАЦИОННЫЕ |
|
|
ПРОИЗВОДСТВЕННО-ТЕХНОЛОГИЧЕСКИЕ |
КОММЕРЧЕСКИЕ КОНТРАКТЫ |
|
||
(10)/ |
|
|
|
|||||
рекламные материалы; |
|
|
|
|||||
|
|
промышленные регламенты; |
договоры о поставке; |
|
||||
письма |
|
|
|
|
||||
2011 |
|
|
|
фармакопейные статьи; |
протоколы согласования цены |
|
||
|
|
|
|
|
|
|||
АРБИТРАЖНЫЕ |
|
|
|
фармакопейные статьи предприятия; |
|
|
||
|
|
|
|
|
|
|||
|
|
|
|
спецификации на: |
|
|
||
|
уведомления; |
|
|
|
ДОКУМЕНТЫ СИСТЕМЫ КАЧЕСТВА |
|
||
|
|
|
|
— сырье, |
|
|||
|
решения |
|
|
|
Политика в области качества; |
|
||
|
|
|
|
|
|
— полупродукты, |
Руководство по качеству; |
|
|
|
|
|
|
|
— продукцию, |
|
|
|
|
|
|
|
|
Мастер-файл; |
|
|
|
ЗАПИСИ: |
|
|
|
— вспомогательные материалы, |
|
||
|
|
|
|
Управление документацией; |
|
|||
|
|
|
|
— упаковочные материалы; |
|
|||
|
записи, требуемые стандартом ГОСТ Р ИСО |
идентификация и прослеживаемость про- |
Управление записями; |
|
||||
|
9001-2008 (4.2.1); |
|
|
цессов и продукции на всех стадиях (7.5.3); |
технико-экономические нормативы; |
Подготовка персонала; |
|
|
|
|
|
стандартные операционные процедуры; |
|
||||
|
управление записями (4.2.3); |
|
записи об утере, повреждении собствен- |
Внутренний аудит; |
|
|||
|
|
инструкции технологические; |
|
|||||
|
анализ со стороны руководства (5.6.1); |
ности потребителей (7.5.4); |
Управление несоответствующей про- |
|
||||
|
инструкции по оборудованию; |
|
||||||
|
об образовании, подготовке, навыках, опы- |
результаты калибровки и поверки (7.6); |
дукцией; |
|
||||
|
инструкции по охране труда; |
|
||||||
|
те персонала (6.2.2); |
|
|
проведение аудитов и отчеты о результа- |
Предупреждающие действия; |
|
||
|
|
|
инструкции по пожарной безопасности; |
|
||||
|
свидетельство |
соответствия |
процессов |
тах (8.2.); |
Корректирующие действия; |
|
||
|
справочники, перечни |
|
||||||
|
жизненного цикла продукции и произведен- |
мониторинг и измерение продукции (8.2.4); |
Инструкции административные; |
|
||||
|
|
|
||||||
|
ной продукции требованиям (7.1); |
|
характер несоответствий продукции, а так- |
ЗАПИСИ |
Номенклатуры дел |
|
||
|
результаты анализа требований, относя- |
же любых последующих предпринятых дей- |
|
|
||||
|
щихся к продукции, и последующих действий, |
ствий; |
маршрутные карты/листы; |
|
|
|||
|
вытекающих из анализа (7.2.2); |
|
результаты предпринятых корректирую- |
планы производства; |
|
|
||
|
результаты оценки поставщиков (7.4.1); |
щих действий (8.5.2); |
планы ППР; |
|
|
|||
|
валидация процессов производства и |
результаты предпринятых предупреждаю- |
заявки на сырье и материалы; |
|
|
|||
|
обслуживания (7.5.2); |
|
щих действий (8.5.3) |
журналы |
|
|
||

УПРАВЛЕНИЕ КАЧЕСТВОМ В ФАРМАЦИИ
Таблица 1. Содержание документов в зависимости от уровня в структуре документации СМК
|
|
Нормативные документы |
Организационно- |
|
Нормативные и |
|
Группы |
Описывающие СМК |
распорядительная |
Записи |
законодательные документы внешне- |
||
(НД) |
||||||
|
|
документация (ОРД) |
|
го происхождения |
||
|
|
|
|
|||
Определе- |
Регламентирующие доку- |
Документы, регламентирую- |
Совокупность взаимо- |
Документы, установлен- |
Документы, |
|
ние |
менты, разрабатываемые на |
щие процесс производства |
связанных документов, |
ные для представления |
выпущенные |
|
|
предприятии. Они включают |
лекарственных средств: |
функционирующих в |
свидетельств соот- |
внешними органами |
|
|
нормативные документы, |
стандарты, содержащие |
сфере управления |
ветствия требованиям, |
|
|
|
регламентирующие произ- |
перечень показателей и |
|
получение объектив- |
|
|
|
водственную деятельность |
методов контроля качества |
|
ных доказательств о |
|
|
|
предприятия: описание |
лекарственного средства, ха- |
|
проделанной работе и |
|
|
|
информации о предприятии |
рактеристики лекарственного |
|
достигнутых результатах |
|
|
|
(требования к системе управ- |
средства, схемы производ- |
|
|
|
|
|
ления качеством, контролю |
ства, характеристики сырья |
|
|
|
|
|
качества, персоналу, по- |
и материалов, процедуры |
|
|
|
|
|
мещениям и оборудованию, |
выполнения отдельных видов |
|
|
|
|
|
документации, производству |
операций |
|
|
|
|
|
продукции и проведению |
|
|
|
|
|
|
анализов по контрактам, ре- |
|
|
|
|
|
|
кламациям, порядку отзыва |
|
|
|
|
|
|
продукции и организации |
|
|
|
|
|
|
самоинспекций (внутренних |
|
|
|
|
|
|
аудитов)) |
|
|
|
|
|
Документы |
Руководство по качеству (РК). |
Фармакопейные статьи пред- |
Организационные до- |
Протоколы. |
Государственные стандарты РФ |
|
|
Мастер-файл (МФ). |
приятия (ФСП). |
кументы (ОД). |
Акты. |
(ГОСТ Р). |
|
|
Политика в области качества |
Фармакопейные статьи (ФС). |
Положения о структурных |
Справки. |
Межгосударственные стандарты (ГОСТ). |
|
|
(ПК). |
Промышленные регламенты |
подразделениях (ПП). |
Отчеты. |
Руководящие документы (РД). |
|
|
Стандарт предприятия на |
(ПР). |
Должностные инструкции |
Журналы и др. |
Методические указания (МУ). |
|
|
процесс (СТО). |
Технологические инструкции |
(ДИ). |
|
Строительные нормы (СН). |
|
|
Методические инструкции |
(ТИ). |
Инструкции о трудовых |
|
Строительные нормы и правила (СНиП). |
|
|
(МИ). |
Рабочие инструкции (РИ). |
обязанностях (ИТО). |
|
Санитарные правила и нормы |
|
|
|
Технологические планы (ТП). |
Приказы. |
|
(СанПиН). |
|
|
|
Стандартные операционные |
Распоряжения. |
|
Санитарные правила и гигиенические |
|
|
|
процедуры (инструкции) (СОП, |
Указания и др. |
|
требования (СП). |
|
|
|
GMP). |
|
|
Общероссийские классификаторы |
|
|
|
Маршрутные карты (МК) и др. |
|
|
(ОК) и др. |
|
Вопросы, |
Какие цели в области |
В каком порядке, при |
Кто, где, в каком по- |
Чем подтверждается |
Какие требования действующего рос- |
|
на которые |
качества ставит высшее |
взаимодействии с кем, на |
рядке, на основании каких |
качество продукции и |
сийского законодательства и других |
|
даются |
руководство? |
основании каких требований, |
документов-требований, |
его улучшение? |
правовых документов, дающих право |
|
ответы в |
Какие задачи надо решить |
в течение какого времени |
при взаимодействии с кем |
Чем подтверждается |
организации осуществлять деятель- |
|
документах |
руководству предприятия, |
и как именно конкретное |
на уровне организации |
факт выполнения дея- |
ность и/или регламентирующих эту |
|
|
чтобы достичь поставленных |
подразделение выполня- |
выполняет требования |
тельности в соответствии |
деятельность, и/или регламентирую- |
|
|
целей? |
ет требования системы |
системы менеджмента ка- |
с конкретным требова- |
щих отношения с другими сторонами, |
|
|
Каким образом высшее |
качества? |
чества при осуществлении |
нием системы качества и |
должна выполнять организация при |
|
|
руководство предприятия |
Каким образом подраз- |
деятельности в рамках |
факт ее улучшения? |
осуществлении деятельности? |
|
|
обеспечивает решение задач |
деление документально |
реализации Политики |
|
Какие работы (мероприятия) |
|
|
для достижения поставлен- |
подтверждает факт поопе- |
в области качества и |
|
планирует провести организация в |
|
|
ных целей? |
рационного выполнения |
достижения поставленных |
|
целом, каждое подразделение и ис- |
|
|
|
установленного порядка? |
целей? |
|
полнители для реализации Политики |
|
|
|
Как именно исполнитель на |
|
|
и достижения поставленных целей в |
|
|
|
своем рабочем месте выпол- |
|
|
области качества? |
|
|
|
няет конкретную операцию |
|
|
Кто и какие виды работ должен вы- |
|
|
|
и фиксирует ее фактическое |
|
|
полнять при решении поставленных |
|
|
|
выполнение? |
|
|
задач? |
|
|
|
|
|
|
Как правильно документировать |
|
|
|
|
|
|
фактическое выполнение операций |
|
|
|
|
|
|
в установленных в организации |
|
|
|
|
|
|
формах? |
|
|
|
|
|
|
Какие именно требования к продук- |
|
|
|
|
|
|
ции, технологическим процессам ее |
|
|
|
|
|
|
изготовления, контроля и испытаний |
|
|
|
|
|
|
следует неукоснительно выполнять? |
МЕНЕДЖМЕНТ КАЧЕСТВА В СФЕРЕ ЗДРАВООХРАНЕНИЯ И СОЦИАЛЬНОГО РАЗВИТИЯ № 4 (10)/ 2011 81
УПРАВЛЕНИЕ КАЧЕСТВОМ В ФАРМАЦИИ
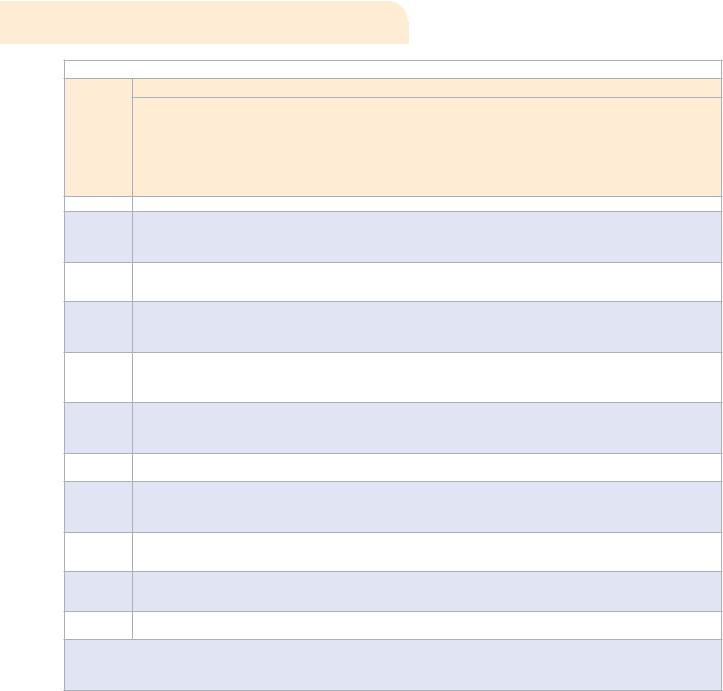
Таблица 2. Порядок обращения с документацией системы менеджмента качества (матрица ответственности)
Наименование
документации
1
Политика и цели в области качества на уровне предприятия
Руководство по качеству предприятия
Стандарты предприятия на уровне предприятия
Методические инструкции на уровне предприятия
Документация по процессам для анализа деятельности СМК
Положение о подразделении
Цели в области качества на уровне подразделений
Спецификации
Стандартные
операционные процедуры (СОП)
Должностные
инструкции
Список сокращений:
|
|
Разработка, издание, введение в действие |
|
|
|
|
|
|
Внесение изменений |
|
|
Проверка |
Изъятие |
Хранение |
||||||||||||
ответственный за разработку |
|
утверждает |
|
согласует |
|
ответственный за регистрацию, за издание |
|
ответственный за рассылку |
|
ответственный за введение в действие |
|
ответственный за обучение |
ответственный за разработку |
|
утверждает |
|
согласует |
|
ответственный за издание, рассылку |
|
ответственный за внесение изменений в подлинник |
|
ответственный за внесение изменений в копию |
ответственный за проверку |
Ответственный за изъятие |
Ответственный за хранение |
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
2 |
|
3 |
|
4 |
|
5 |
|
6 |
|
7 |
|
8 |
9 |
|
10 |
|
11 |
|
12 |
|
13 |
|
14 |
15 |
16 |
17 |
ПРК |
|
Директор |
|
- |
|
ООК |
|
ООК |
|
Директор |
|
ООК |
|
|
Аналогично |
|
|
ООК |
|
ООК |
Директор |
ООК |
ООК |
|||
|
|
|
|
|
|
|
«Разработке» |
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
ООК |
|
Директор |
|
ПРК |
|
ООК |
|
ООК |
|
ПРК |
|
ООК |
|
|
Аналогично |
|
|
ООК |
|
ОзДП |
ООК |
ООК |
ООК |
|||
|
|
|
|
|
|
|
«Разработке» |
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
Директор, |
|
|
|
|
|
|
|
|
|
|
|
|
Аналогично |
|
|
|
|
|
|
|
|
|||
ООК |
|
главный |
|
ПРК |
|
ООК |
|
ООК |
|
Директор |
|
ООК |
|
|
|
|
ООК |
|
ОзДП |
ООК |
ООК |
ООК |
||||
|
|
|
|
|
|
|
«Разработке» |
|
|
|
||||||||||||||||
|
|
инженер |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ООК |
|
Директор |
|
ПРК |
|
ООК |
|
ООК |
|
Директор |
|
Директор |
|
|
Аналогично |
|
|
ООК |
|
ОзДП |
ООК |
ООК |
ООК |
|||
|
|
|
|
|
|
|
«Разработке» |
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
РП, ВП |
|
РП, ВП |
|
- |
|
ООК |
|
- |
|
- |
|
- |
|
|
Аналогично |
|
|
РП, ВП |
|
РП, ВП |
ПРК |
- |
ООК |
|||
|
|
|
|
|
|
|
«Разработке» |
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
РП |
|
Директор |
|
ПРК |
|
ОзДП |
|
ОзДП |
|
РП |
|
РП |
|
|
Аналогично |
|
|
ОзДП |
|
ОзДП |
РП |
ОзДП |
ОзДП |
|||
|
|
|
|
|
|
|
«Разработке» |
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
РП |
|
РП |
|
ПРК |
|
ОзДП |
|
ОзДП |
|
РП |
|
РП |
|
|
Аналогично |
|
|
ОзДП |
|
ОзДП |
ПРК |
ОзДП |
ОзДП |
|||
|
|
|
|
|
|
|
«Разработке» |
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
Директор, |
|
|
|
|
|
|
|
|
|
|
|
|
Аналогично |
|
|
|
|
|
ЗДК, |
|
|
|||
ООК |
|
главный |
|
РП |
|
ООК |
|
ООК |
|
ООК |
|
ООК |
|
|
|
|
ООК |
|
ООК |
ООК |
ООК |
|||||
|
|
|
|
|
|
|
«Разработке» |
|
|
|
ПРК |
|||||||||||||||
|
|
инженер |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Директор, |
|
|
|
|
|
|
|
|
|
|
|
|
Аналогично |
|
|
|
|
|
|
|
|
|||
ООК |
|
главный |
|
РП |
|
ООК |
|
ООК |
|
ЗДК |
|
ЗДК |
|
|
|
|
ООК |
|
РД |
ООК |
ООК |
ООК |
||||
|
|
|
|
|
|
|
«Разработке» |
|
|
|
||||||||||||||||
|
|
инженер |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ИК |
|
Директор |
|
ЮК, ПРК |
|
ИК |
|
ИК |
|
ИК |
|
ИК |
|
|
Аналогично |
|
|
ИК |
|
ИК |
ЮК |
ИК |
ИК |
|||
|
|
(ПРК) |
|
|
|
|
|
|
|
|
|
|
|
«Разработке» |
|
|
|
|
|
|
|
|
||||
ЗДК — заместитель директора по качеству; МК — менеджер по качеству; ПРК — представитель руководства по качеству; РП — руководитель подразделения; ОзДП — ответственный за документацию в подразделении; ООК — отдел обеспечения качества; РД — разработчик документации; ИК — инспектор по кадрам; ЮК — юрисконсульт; ВП — владелец процесса.
троль исполнения по предприятию, согласование документов по предприятию; в его обязанности входит документальное оформление Политики в области качества, целей и задач предприятия в области качества;
начальник отдела обеспечения качества — разработка руководства по качеству, мастер-файла «Информация о предприятии», планирование и согласование вновь разрабатываемых документов, контроль своевременности пересмотра действующих документов и их соответствия вновь вводимым законодательным и нормативным требованиям и принятым технологическим решениям, общее руководство разработкой стандартов предприятия, документации по обеспечению качества предприятия, согласование документов;
менеджер по качеству отдела обеспечения качества, ответственный за документацию — текущая работа по соблюдению порядка обращения с документами, поддержание эффективности функционирования системы документации на предприятии;
начальник ПТО — планирование и общее руководство разработкой промышленных регламентов, технологических инструкций, инструкций по упаковке; также осуществляет согласование вновь разрабатываемых документов, контроль своевременности пересмотра действующих документов и их соответствия вновь вводимым законодательным и нормативным требованиям и принятым технологическим решениям;
руководитель подразделения — контроль за выполнением требований документации, разработка стандартов пред-
82 МЕНЕДЖМЕНТ КАЧЕСТВА В СФЕРЕ ЗДРАВООХРАНЕНИЯ И СОЦИАЛЬНОГО РАЗВИТИЯ № 4 (10)/ 2011

приятия по принадлежности, анализ состояния управления документацией в подразделении;
ответственный за документацию в подразделении — текущая работа по соблюдению порядка обращения с документами, поддержание эффективности функционирования системы документации в подразделении;
разработчик документации — представитель подразделения предприятия; разрабатывает документы, содержащие указания по выполнению отдельных видов операций (например, по очистке, контролю окружающей среды, проведению испытаний и т.д.).
СТРУКТУРА ДОКУМЕНТАЦИИ СИСТЕМЫ ОБЕСПЕЧЕНИЯ
КАЧЕСТВА
Структура документации системы обеспечения качества должна разрабатываться в соответствии с принятой на предприятии структурой управления.
Использование такого принципа позволяет правильно распределить ответственность и полномочия и установить четкие взаимодействия руководителей всех уровней, вести эффективный контроль за качеством выполнения работ и своевременно осуществлять корректирующие и предупреждающие действия на каждом этапе жизненного цикла продукции.
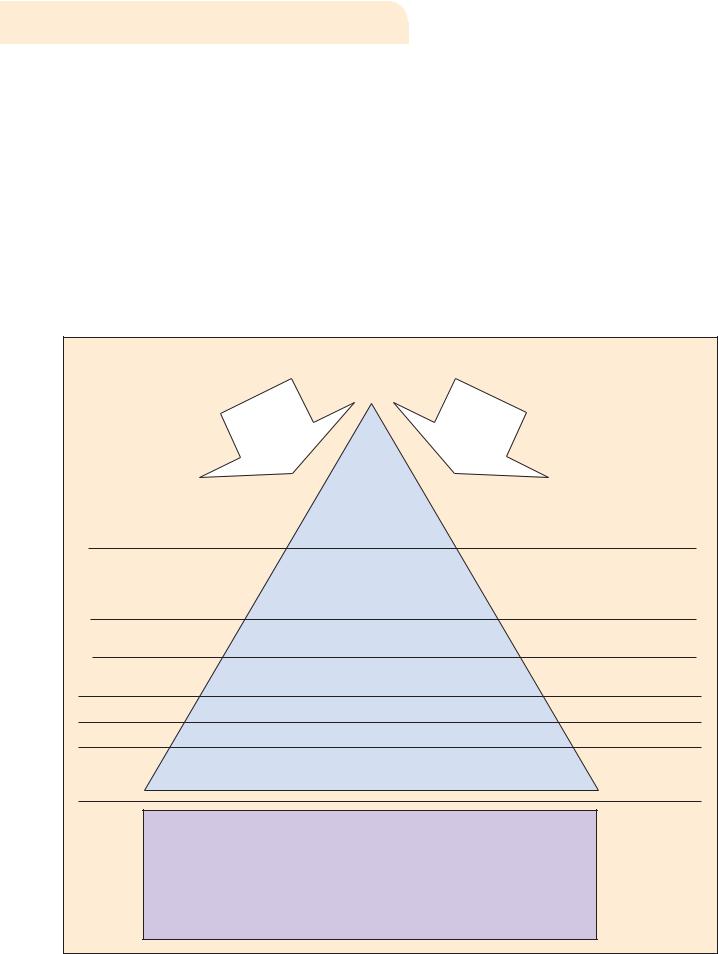
Структуру документации системы обеспечения качества можно представить схематично в виде «домика», в котором документы по качеству формируют:
«фундамент» (документы по планированию, обеспечению и улучшению качества);
УПРАВЛЕНИЕ КАЧЕСТВОМ В ФАРМАЦИИ
«крышу» (документы по управлению качеством);
«стены» (документы по подтверждению качества и подтверждению улучшения качества).
Примеры документов каждого уровня в структуре документации системы обеспечения качества представлены на
рисунке 3.
Общие требования к организации работ по созданию документов системы обеспечения качества
При разработке документации необходимо руководствоваться принципом «5W и 1H»:
Why? — Почему это делается? Надо ли это делать? Что случится, если этого не делать?
What? — Что делается? Понимаем ли мы точно и ясно детали операции?
When? — Когда это делается? Не будет ли лучше, если это делать раньше или позже?
Where? — Где это делается? Наилучшая ли это позиция? Who? — Кто это делает? Нет ли кого более подходящего? How? — Как это делается? Можно ли сделать лучше? При разработке и внедрении документации необходимо
показать, «что?» и «как?» предприятие представляет в целом, «что?» и «как?» его подразделения и отдельные исполнители делают для реализации Политики в области качества и «как?» именно выполняют требования системы обеспечения качества. В самой документации разработчики описывают «как?» осуществляется управление процессами с учетом требований СМК. Поэтому при описании порядка управления процессами не рекомендуется использовать слова: «должен», «следует», «необходимо» и т.п. Текст раз-
Таблица 3. Детализация при документировании процессов
Документ |
Назначение, основное содержание, степень детализации |
|
|
Политика руководства |
Основной «стартовый» документ системы обеспечения качества, содержащий основные направления, цели и задачи |
в области качества |
руководства в области качества. |
|
Оформляется отдельным документом, а также обязательно включается в «Руководство по качеству», «Мастер-файл» |
Руководство по качеству |
Основной документ руководства предприятия — путеводитель по системе качества, включающий Политику в об- |
|
ласти качества и организационную функциональную структуру предприятия. |
|
Устанавливает ответственность руководителей за выполнение требований системы качества. |
|
Описывает систему обеспечения качества с указанием ссылок на документы — стандарты предприятия (СТО). |
|
Степень детализации зависит от наличия СТО и масштабов предприятия |
Мастер-файл |
Основной документ руководства предприятия содержит данные о производстве и контроле лекарственных средств |
|
на предприятии. |
|
Описывает требования к системе управления качеством, контролю качества, персоналу, помещениям и оборудова- |
|
нию, документации, производству продукции и проведению анализов по контрактам, рекламациям, порядку отзыва |
|
продукции и организации самоинспекций с указанием ссылок на документы — стандарты предприятия (СТО), |
|
инструкции (СОП) и т.д. |
СТО, СОП (уровень предприятия) |
Стандарты предприятия и стандартные операционные процедуры, охватывающие все структурные подразделения. |
|
Описывают установленный порядок выполнения деятельности (процесса), формы и виды взаимодействий и пути |
|
прохождения информации ввода/вывода с указанием ссылок на необходимые документы (степень детализации |
|
средняя) |
СТО, СОП |
Управляющие процедуры, в которых описывается специфика выполнения требований системы обеспечения |
(уровень подразделения) |
качества, как правило, в отдельном подразделении применительно к производству конкретной продукции или |
|
конкретной деятельности (максимальная степень детализации процессов) |
СОП (уровень отдельного |
Документ, подробно описывающий условия и приемы выполнения операций на конкретных рабочих местах |
исполнителя — РИ) |
(максимально уместная степень детализации конкретных операций) |
МЕНЕДЖМЕНТ КАЧЕСТВА В СФЕРЕ ЗДРАВООХРАНЕНИЯ И СОЦИАЛЬНОГО РАЗВИТИЯ № 4 (10)/ 2011 83
УПРАВЛЕНИЕ КАЧЕСТВОМ В ФАРМАЦИИ
дела следует излагать в повелительном наклонении, напри- |
При изложении документов СМК необходимо соблюдать |
мер: «Подготовить помещение», «Перемешать...», «Переве- |
следующие требования: |
сти...», «Сделать запись...». |
четкость и логическую последовательность; |
Степень детализации при описании процессов увеличи- |
краткость и точность формулировок, исключающих воз- |
вается при переходе с верхних уровней на нижние (рис. 3, |
можность неоднозначного толкования; |
табл. 3). |
использование стандартизованной терминологии; |
Для обеспечения внедрения и облегчения использова- |
использование терминологии, принятой на предприятии, |
ния документов системы обеспечения качества необходи- |
только при ее отсутствии в нормативных документах внеш- |
мо провести унификацию форм документов каждого уров- |
него происхождения. |
ня, т.е. обеспечить единообразие их структуры, изложения и |
Порядок разработки документации представлен в та- |
оформления. Такой подход способствует единому понима- |
блице 4. |
нию документов системы обеспечения качества как всеми |
При рассмотрении документов системы обеспечения ка- |
пользователями, так и проверяющими сторонами при про- |
чества всегда определяется цель их разработки и роль в си- |
ведении внутренних и внешних аудитов системы качества. |
стеме обеспечения качества. |
Рисунок 3. Структура документации системы обеспечения качества
Законодательство, |
|
международные |
|
государственные |
|
и |
стандарты |
|
|
Миссия, стратегия
Статус у тверждения
|
Политика предприятия |
|
|
|
в области качества. |
|
|
Директор |
Цели в области качества |
Все подразделения предприятия |
|
|
|||
|
Документы по описанию системы качества |
|
|
|
на уровне предприятия |
|
|
|
(РСМ, РК, МФ, процессы предприятия, |
Директора, руководители, |
|
|
инструкции (SOP)) |
||
Директор |
специалисты подразделений |
||
|
Директор
Директор
Директор, главный инженер
Директор, главный инженер
Цели в области качества процессов, применяемых на предприятии. Методические указания (МУ)
Документы по описанию системы качества на уровне подразделений
(Цели в области качества подразделений, СТО СМ, СТО СК)
Инструкции, методики (SOP, спецификации, ИК СМК, МО СК)
Положение о подразделении, должностные инструкции (ПП, ДИ)
Руководители подразделений, специалисты подразделений
Руководители подразделений, специалисты, персонал подразделений
Руководители подразделений, специалисты подразделений
Руководители подразделений, специалисты подразделений
Область распространения
Руководитель |
|
Руководители подразделений, |
|
Документы по подтверждению качества (протоколы, акты, отчеты, рабочие журналы, записи и т.д.) |
специалисты, рабочие |
||
подразделения |
|||
подразделений |
|||
|
|||
|
|
Правовые документы
1.1 – Правовые документы государственного уровня (законы РФ, указы Президента РФ, постановления Правительства РФ, постановления федеральных органов исполнительной власти РФ и т.п.).
1.2– Правовые документы на уровне организации.
1.2.1Правовые документы, обеспечивающие организации право осуществлять деятельность (учредительные документы (устав и др.), лицензии и т.п.).
1.2.2Правовые документы, регламентирующие отношения организации с другими сторонами при осуществлении деятельности (договоры, контракты и т.п.)
84 МЕНЕДЖМЕНТ КАЧЕСТВА В СФЕРЕ ЗДРАВООХРАНЕНИЯ И СОЦИАЛЬНОГО РАЗВИТИЯ № 4 (10)/ 2011

|
УПРАВЛЕНИЕ КАЧЕСТВОМ В ФАРМАЦИИ |
|
|
|
|
Таблица 4. Порядок определения разработки документации СМК |
|
|
|
|
|
Документ |
Каким документом определяется порядок разработки |
|
|
|
|
Руководство по качеству, мастер-файл, |
Разрабатываются в соответствии с требованиями ГОСТ Р ИСО 9001-2008, ГОСТ Р 52249-2009, |
|
Политика в области качества, стандарт пред- |
ГОСТ Р 52537-2006 и внутренним документом «Управление документацией» |
|
приятия, методические инструкции |
|
|
Положение о подразделении |
В соответствии с ГОСТ Р 52537-2006, п. 4.5.4, внутренним документом «Порядок разработки, содержа- |
|
|
ния, согласования, оформления и утверждения положений о структурных подразделениях» |
|
Должностные инструкции и инструкции о |
В соответствии с Трудовым кодексом, ГОСТ Р 52537-2006, п. 4.5.5, п. 4.5.6 и внутренним документом |
|
трудовых обязанностях |
«Порядок разработки и оформления должностных инструкций и инструкций о трудовых обязанностях» |
|
Инструкции (СОП) |
В соответствии с п. 4 ГОСТ Р 52249-2009, п. 5.5 ГОСТ Р 52550-2006, внутренним документом «Порядок |
|
|
составления инструкций» |
|
Спецификации |
В соответствии с п. 4 ГОСТ Р 52249-2009, п. 5.3 ГОСТ Р 52550-2006, внутренним документом «Порядок |
|
|
составления спецификации» |
|
Организационно-распорядительная до- |
В соответствии с СТО «Система менеджмента качества. О ведении делопроизводства на предприятии» |
|
кументация |
|
|
Нормативные документы |
В соответствии с фармакопейными статьями и отраслевыми стандартами |
|
|
|
|
Далее представлены подходы к разработке некоторых документов системы обеспечения качества.
ПОЛИТИКА В ОБЛАСТИ КАЧЕСТВА
Политика и цели в области качества устанавливаются, чтобы служить ориентиром для организации. Они определяют желаемые результаты и способствуют использованию организацией ресурсов для достижения этих результатов. Политика в области качества обеспечивает основу для разработки и анализа целей в области качества [2].
Политика в области качества играет особую роль в системе качества. Она предназначена для того, чтобы расставлять акценты в отношениях руководства предприятия с заинтересованными сторонами:
1 — потребителями продукции (различные организации (предприятия) и государство);
2 — поставщиками сырья, полуфабрикатов и комплектующих;
3 — персоналом предприятия;
4 — вышестоящими организациями (владельцы, совет акционеров);
ГОСТ Р ИСО 9001-2008, п. 5.3 Политика качества (извлечение):
Высшее руководство должно гарантировать, что политика в области качества:
а) соответствует целям организации; б) включает обязательство соответствовать требовани-
ям и постоянно повышать результативность системы менеджмента качества; в) создает основу для постановки и анализа целей в области качества;
г) доведена до сведения персонала организации и понятна ему; д) анализируется на постоянную пригодность
ГОСТ Р 52537-2006, п. 4.8.
Политика предприятия в области качества:
Для подчеркивания первостепенной роли обеспечения качества и постоянного акцентирования внимания всех сотрудников на обеспечении качества на предприятии может быть принята политика качества, которая оформляется в виде отдельного документа под названием «Политика в области качества». Это краткий общий документ, определяющий цель работы коллектива в отношении качества.
Документ должен отражать предмет деятельности предприятия, понимание коллективом предприятия своей основной задачи как всемерное удовлетворение нужд потребителей, установку на постоянное совершенствование работы с целью обеспечения стабильности показателей качества выпускаемой продукции. Документ подписывается руководителем предприятия, доводится до каждого работника, постоянно находится в доступном месте, публикуется в информационных материалах и пр.
Политика предприятия в области качества должна быть ясной, понятной и воспринятой всеми работающими. Ее цели должны быть реальными. При ее формулировании следует избегать многословия, ничего не значащих фраз и формализма
5 — органами социальной инфраструктуры (района, города, республики, государства).
«Высшему руководству необходимо использовать политику в области качества как средство управления с целью улучшения деятельности предприятия» [1].
Политика в области качества — это набор основных целей, направлений, планов для достижения этих целей, сформированных таким образом, чтобы определить, чем это предприятие является сейчас или планирует стать.
МЕНЕДЖМЕНТ КАЧЕСТВА В СФЕРЕ ЗДРАВООХРАНЕНИЯ И СОЦИАЛЬНОГО РАЗВИТИЯ № 4 (10)/ 2011 85
УПРАВЛЕНИЕ КАЧЕСТВОМ В ФАРМАЦИИ
В соответствии с стандартом ГОСТ Р ИСО 9001-2008: «Политика в области качества — это общие намерения и направления деятельности предприятия в области качества, официально сформулированные высшим руководством».
Политика в области качества может и должна использоваться для улучшения деятельности, если она:
согласуется с прогнозом и стратегией высшего руководства по перспективам предприятия;
позволяет понять и реализовать цели в области качества на предприятии;
подтверждает приверженность высшего руководства качеству и обязательства обеспечивать необходимыми ресурсами работы по достижению целей;
помогает разъяснению этой приверженности качеству на предприятии при четком лидерстве высшего руководства;
включает постоянное улучшение, связанное с удовлетворением потребностей и ожиданий потребителей и других заинтересованных сторон;
четко сформулирована и умело доведена до сведения всего персонала.
ЦЕЛИ В ОБЛАСТИ КАЧЕСТВА
Отсутствие четких целей при разработке, внедрении, управлении и совершенствовании системы качества может оказаться фатальной ошибкой. Без цели нет основы для создания приоритетов, единения усилий или оценки успеха. По этой причине, до начала разработки, внедрения, управления и совершенствования системы качества необходимо уделить время выявлению природы и степени важности тех вопросов, на которые необходимо найти ответы.
ГОСТ Р ИСО 9001-2008, п. 5.4.1 Цели в области качества (извлечения):
Высшее руководство организации должно гарантировать, что цели в области качества, включая те, которые необходимы для выполнения требований к продукции (см. 7.1 а), установлены для значимых функций и уровней. Цели в области качества должны быть измеримыми и согласовываться с политикой в области качества
Согласно ГОСТ Р ИСО 9001-2008 п. 5.4.1 «высшее руководство должно гарантировать, что цели в области качества были установлены в соответствующих подразделениях организации и на соответствующих ее уровнях» [1]. Ответственность за достижение целей в области качества в рамках каждого подразделения, выполняющего конкретную функцию в подсистеме линейного управления, распределяется по вертикали сверху вниз между руководителями соответствующих уровней.
Согласно ГОСТ Р ИСО 9000-2008 «цели в области качества — это цели, которых добиваются или к которым стре-
мятся в области качества» [2]. Цель считается достигнутой, если в итоге предпринятых действий получен соответствующий этой цели результат.Таким образом, наличие возможности проверки (контроля, оценки) достижения цели и следует считать измеримостью цели. Другими словами, цель в области качества, достижение (степень достижения) которой можно проверить (проконтролировать, оценить), является измеримой целью.
ГОСТ Р ИСО 9000-2008, п. 5 (извлечения):
Цели в области качества необходимо согласовывать с политикой в области качества и приверженностью к постоянному улучшению, а результаты должны быть измеримыми. Достижение целей в области качества может оказывать позитивное воздействие на качество продукции, эффективность работы и финансовые показатели и, следовательно, на удовлетворенность и уверенность заинтересованных сторон
Цель можно считать измеримой в двух случаях, если:
цель представлена значением некоторого показателя (в явном или неявном виде), называемым «целевым значением показателя»;
цель представляет собой некоторое событие, которое должно произойти (в течение некоторого промежутка времени).
МАСТЕР ФАЙЛ «ИНФОРМАЦИЯ О ПРЕДПРИЯТИИ»
В «Информации о предприятии» приводятся следующие данные:
наименование и адрес предприятия;
номенклатура выпускаемой продукции (если допустимо);
данные о численном составе персонала (если допустимо);
организационная структура предприятия;
наличие руководителей службы контроля качества;
ГОСТ Р 52537-2006, приложение А:
«Информация о предприятии» — документ, подготовленный производителем и содержащий данные о производстве и (или) контроле лекарственных средств на предприятии (производстве), а также о любых связанных с ними операциях, выполняемых в соседних или близлежащих зданиях. Если в данном месте выполняется только часть операций, то в «Информации о предприятии» следует приводить только эти операции, например, проведение анализа, упаковка и пр. «Информация о предприятии» должна быть краткой (объемом не более 25 страниц)
86 МЕНЕДЖМЕНТ КАЧЕСТВА В СФЕРЕ ЗДРАВООХРАНЕНИЯ И СОЦИАЛЬНОГО РАЗВИТИЯ № 4 (10)/ 2011
перечень основных стандартов, на которых основана система обеспечения качества;
систематизированный перечень документов, по которым ведется работа предприятия, подразделений и отдельных исполнителей, проводится аттестация и испытания оборудования, ведется обучение персонала и пр.; при большом количестве документов могут приводиться виды (наименования групп) документов.
Приложениями к «Информации о предприятии» могут быть:
политика предприятия в области качества (необязательный документ);
сводный перечень всех документов на предприятии (инструкции, методики, приказы и пр.) с системой кодирования документов (при необходимости).
На предприятии должно быть определено лицо, ответственное за разработку «Информации о предприятии». Руководителям подразделений также следует принимать активное участие в данной работе.
«Информация о предприятии» должна быть по возможности краткой, написанной в ясной форме и широко использоваться в практической деятельности. Вместе с тем она должна быть открытым (за исключением данных для служебного пользования) и полезным для сотрудников и руководителей предприятия документом.
ИНСТРУКЦИИ
Инструкции и методики охватывают все сферы производства и контроля качества и регламентируют действия, общие для различных видов продукции; могут оформляться в виде стандарта предприятия. Они не включают требования к производству конкретной продукции, которые изложены в промышленном регламенте.
ГОСТ Р 52249-2009 (извлечение):
Инструкция, методика, процедура (procedure): документ, содержащий указания по выполнению отдельных видов операций (например, по очистке, переодеванию, контролю окружающей среды, отбору проб, проведению испытаний, эксплуатации оборудования)
Инструкции и методики регламентируют:
получение и контроль качества исходных и упаковочных материалов;
контроль качества промежуточной и готовой продукции;
работу лабораторий;
аттестацию «критических процессов» и оборудования;
работу складов, обращение материалов, промежуточной и готовой продукции;
технологическое и инженерное оборудование (системы отопления, вентиляции и кондиционирования воздуха, под-
УПРАВЛЕНИЕ КАЧЕСТВОМ В ФАРМАЦИИ
готовки воды, пара, технологических жидкостей и газов, сжатого воздуха, чистые помещения, эксплуатацию, техническое обслуживание и ремонт оборудования, калибровку приборов и т.д.);
требования к поведению, гигиене и состоянию здоровья персонала;
порядок ведения документации и т.д.
Персонал должен знать инструкцию и уметь ответить на любой вопрос, ее касающийся.
Инструкции, включая изменения к ним, должны соответствовать требованиям нормативных документов, промышленных регламентов, технической документации на процессы и оборудование.
Инструкции разрабатываются в следующих случаях: организации нового производства; реконструкции производства;
введения нового оборудования и процессов или внесения в них изменений;
изменения нормативных документов,требующего разработки новой инструкции.
ЗАПИСИ
Управление записями и организация информационных потоков имеют многоуровневую иерархическую структуру и осуществляется на различных уровнях: исполнитель, бригада, участок, цех, смена, функциональные службы, руководство предприятия. Записи должны вестись в строгом соответствии с установленной формой журнала, бланка или иного носителя информации. Как правило, все графы журнала (бланка) должны быть заполнены. Информация, занесенная в носители, должна быть понятна работникам подразделений, уполномоченным контролирующих органов. Информация же, относящаяся к качеству готовой продукции, условиям поставок, статусу испытаний, рассмотрению предложений и жалоб,— понятна и потребителю.
Записи должны быть:
легко и однозначно читаемы;
ИСО 9001-2008, п. 4.2.4 Управление записями (извлечение):
Записи, предусмотренные для обеспечения доказательств соответствия требованиям и результативности деятельности системы менеджмента качества, должны управляться.
Организация должна разработать документированную процедуру с тем, чтобы определить средства контроля, необходимые для идентификации, хранения, защиты, восстановления, определения сроков сохранения и изъятия записей.
Записи должны оставаться четкими, легко идентифицируемыми и восстанавливаемыми
МЕНЕДЖМЕНТ КАЧЕСТВА В СФЕРЕ ЗДРАВООХРАНЕНИЯ И СОЦИАЛЬНОГО РАЗВИТИЯ № 4 (10)/ 2011 87

УПРАВЛЕНИЕ КАЧЕСТВОМ В ФАРМАЦИИ
датированными, включая даты просмотра соответствую- |
соответствие правовым и законным требованиям и по- |
|
щими должностными лицами; |
литике организации; |
|
идентифицируемыми по номеру (шифру) предприятия, |
обеспечение хранения записей в безопасной и надеж- |
|
виду документов, году или содержать идентификационные |
ной среде; |
|
признаки объекта, записи по которому зарегистрированы; |
обеспечение хранения записей в необходимых сроках; |
|
ориентированы на конкретные виды продукции; |
определение и оценка возможностей для улучшения ре- |
|
содержать фамилию и подпись лица, сделавшего записи. |
зультативности, эффективности или качества процессов, ре- |
|
Записи позволяют предприятию: |
шений, действий. |
|
вести дела аккуратно, эффективно и понятно; |
|
Управление записями осуществляется для обеспечения |
поставлять услуги последовательно и справедливо; |
возможности: |
|
документировать и поддерживать формирование поли- |
постоянно располагать достоверными сведениями о со- |
|
тики и административное принятие решений; |
стоянии качества продукции от маркетинговых исследова- |
|
обеспечивать последовательность, непрерывность и про- |
ний до ее использования; |
|
дуктивность в управлении и администрировании; |
выявлять и фиксировать все возможные несоответствия в |
|
облегчать результативное выполнение действий по всей |
осуществлении процессов СМК и качества продукции; |
|
организации; |
своевременно выявлять причины несоответствия, анали- |
|
обеспечивать непрерывность в случае стихийного бед- |
зировать их, предупреждать их появление в дальнейшем; |
|
ствия; |
контролировать состояние производственных процессов, |
|
удовлетворять требованиям законодательных органов и |
разрабатывать и реализовывать необходимые корректиру- |
|
обязательным требованиям, включая архивную, провероч- |
ющие воздействия; |
|
ную и надзорную деятельность; |
располагать необходимыми сведениями для оценки ре- |
|
предоставлять защиту и поддержку в судебных процес- |
зультативности мероприятий по качеству и оценки эффек- |
|
сах, включая управление рисками, связанными с деятель- |
тивности системы менеджмента качества в целом. |
|
ностью организации; |
|
Для реализации этих целей решаются следующие задачи: |
защищать интересы организации и права служащих, клиен- |
распределение задач и ответственности по подразделе- |
|
тов, а также нынешних и будущих заинтересованных сторон; |
ниям предприятия в части регистрации данных о качестве; |
|
поддерживать и документировать текущую и будущую |
разработка организационных процедур регистрации |
|
исследовательскую и опытно-конструкторскую работу, со- |
данных: определение регистрируемых показателей каче- |
|
бытия и достижения, а также поддерживать исторические |
ства, параметров процессов, выбор видов носителей ин- |
|
исследования; |
формации, разработка их форм и маршрутов движения, |
|
предоставлять свидетельства деятельности (деловой, |
определение порядка сбора, обработки и использования |
|
личной и культурной); |
информации; |
|
устанавливать деловую, личную и культурную идентич- |
контроль за управлением записями; |
|
ность; |
анализ регистрируемых данных о качестве. |
|
сохранять общую, личную или коллективную память. |
|
|
Для обеспечения управления записями предприятие |
|
|
должно ввести и выполнять комплексную программу, кото- |
ПОЛОЖЕНИЯ О СТРУКТУРНЫХ ПОДРАЗДЕЛЕНИЯХ |
|
рая включает: |
|
|
|
|
|
определение того, какие записи должны быть созданы в |
|
ГОСТ Р 52537-2006, п. 4.5.4 (извлечение): |
каждом процессе, и какая информация должна быть вклю- |
|
|
|
|
|
чена в них; |
|
Для подразделений и структурных единиц должны |
решение о том, в какой форме должны быть созданы и |
|
|
|
быть разработаны положения, в которых определены |
|
зафиксированы записи, и какой будет их структура, а также, |
|
структура, задачи, функции, права, взаимоотношения с |
какие технологии необходимо использовать; |
|
другими подразделениями и ответственность |
определение требований к поиску, использованию и пере- |
|
|
даче записей между «владельцами» рабочих процессов и дру- |
|
|
гими пользователями, а также определение сроков хранения |
|
Положения о структурных подразделениях разрабатыва- |
записей, чтобы удовлетворять установленным требованиям; |
ются на основе: |
|
решение о том, как организовать записи, чтобы поддер- |
четко сформулированных основных задач и функций |
|
живать требования к использованию; |
подразделения в составе организационной структуры пред- |
|
оценка рисков, которые будут вызваны отсутствием ау- |
приятия; |
|
тентичных записей деятельности; |
работ, выполняемых подразделением, и обязанностей |
|
обеспечение сохранности и доступности записей по про- |
руководителя подразделения в соответствии с рекоменда- |
|
шествии длительного периода времени, для удовлетворе- |
циями квалификационных справочников должностей руко- |
|
ния требований бизнеса и ожиданий общества; |
водителей, специалистов и служащих. |
|
88 МЕНЕДЖМЕНТ КАЧЕСТВА В СФЕРЕ ЗДРАВООХРАНЕНИЯ И СОЦИАЛЬНОГО РАЗВИТИЯ № 4 (10)/ 2011
