
|
. п „nvrofl Форме продуктивного остеомиелита |
|||||||||||||||
надкостницей. При дру' |
|
изуется в области угла и ветви челю- |
||||||||||||||
патологическии очаг лок• С ) г и ч е с к и |
выявляются участки раз- |
|||||||||||||||
•сти; в толще кости Pel" |
|
|
|
краями. На поверхности ветви и |
||||||||||||
режения кости с нече1* |
енная КОСть имеет |
нежный |
трабеку- |
|||||||||||||
•угла периостально посту |
|
. |
тонким склер0тическим ободком, |
|||||||||||||
лярныйрисунок,окаим. < |
|
|
продуктивного |
остеомиелита раз- |
||||||||||||
|
Обе формы хроническ |
i |
^ |
|
|
дко при ИНТактном зубном |
||||||||||
|
виваются у детей старш |
|
в |
|
|
ферической крови и моче, |
||||||||||
ряде, в отсутствие измен |
^ |
неограниченному |
|
прогрессивному |
||||||||||||
|
Первая форма склон |
^ распр0странению |
патологического |
|||||||||||||
|
избыточному росту кос! |
стИ) |
что напоминает рост опухоли, |
|||||||||||||
очага вдоль |
нижней |
|
_стическим признаком |
воспалительной |
||||||||||||
|
Дифференциально-диагв |
|
считаем выявление на рентгенограм- |
|||||||||||||
|
природы заболевания |
|
|
|
кости> |
имеющей продольное сло |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
ме периостально построе |
|||||
истое строение. |
прнтгенологическая |
форма |
хронического |
|||||||||||||
Вторая |
клинико'рГ,нИКНуть |
после ушиба кости в результа- |
|
|||||||||||||
остеомиелита может во |
|
В0спаления. |
|
Длительное |
|
время мы |
||||||||||
те развития асептическ |
|
омиелита как первично-костный ак- |
||||||||||||||
расценивали эту форму |
|
|
ностику |
на |
показателях |
кожной |
||||||||||
тиномикоз, основывая |
|
|
^ серологической |
реакции крови по |
||||||||||||
реакции с актинолизз! |
н |
|
|
расширенном |
иммунологическом |
|||||||||||
|
наК |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Борде-Жангу. ОД °аКТ иЯОМИКОз быловыявлено, что умно- |
||||||||||||||||
обследовании детей на |
^ ^^ специфичности, |
|
|
|
|
|||||||||||
гих больных воспаление |
|
|
ическом продуктивном остеомиели- |
|||||||||||||
Таким образом, при - к ^ ^^^ |
можно установить |
клини- |
|
|||||||||||||
те нижней челюсти дал |
|
^ |
жалоб? данных анамнеза и кли- |
|||||||||||||
ческий диагноз на оси |
|
исследОБания. Заболевание приходит- |
||||||||||||||
нико-рентгенологическш KQCTHOH capKOMbIj При |
наличииобост- |
|
||||||||||||||
ся дифференцировать " |
|
мы |
юинга, |
При выраженном склерозе |
||||||||||||
рения процесса —от Cdp |
|
нтодисплазии. |
Окончательный кли- |
|||||||||||||
кости —от фиброили |
|
|
|
|
вить |
только |
После гистологиче- |
|||||||||
нический диагноз можно |
^^ |
|
|
|
|
|
|
|
|
|
||||||
ского исследования KOL |
|
ия при диагностике вызывают забо- |
||||||||||||||
Чрезвычаиные затрУ£ |
|
х |
|
тера |
в КОСтях верхней челю- |
|||||||||||
левания гиперпластичесъю интерпретации |
рентгенологиче- |
|||||||||||||||
сти, что связано с тР^ажеНИИ |
в верхней |
челюсти в проекции |
||||||||||||||
ских данных пРи ее пиу |
обнаруживается |
тень |
той или иной |
|||||||||||||
веРхнечелюстнои пазу• |
|
^ патологический очаг имеет четкие |
||||||||||||||
плотности. В одних и . |
|
^к доброкачественная опухоль, чаще |
||||||||||||||
гРаницы и Расценивае1 осснфицирующая |
или |
цементирующая |
||||||||||||||
фиброзная дисплазия, |
|
п |
ессы деструкции и последующе- |
|||||||||||||
фиброма. В других слу |
|
фф |
|
й характер, |
создают впечатле- |
|||||||||||
го склеРоза, носящие |
дов^разования. |
Гиперпластические |
Раз- |
|||||||||||||
ние злокачественного " |
остной |
ткани |
иногда |
заполняют всю |
||||||||||||
растания фиброзной |
|
|
|
ВЫЗывая полную облитерацию ее. |
||||||||||||
верхнечелюстную п^' |
ить |
диагноз |
|
актиномикоза |
крайне |
|||||||||||
Гистологически уст ^^ можно выявить внутрикостные |
|
|||||||||||||||
трудно, так как далеки |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
262 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
микроабсцессы, содержащие друзы актиномицета. Первичнокостный актиномикоз можно диагностировать лишь на основании совокупности данных иммунологического обследования ребенка и морфологического исследования костной ткани.
Изредка в биоптатах встречаются участки с хаотическим расположением примитивных гр>убоволокнистых костных тРабе-кул различной форшы и величины и обильным развитием между ними фиброретикулярной ткани, что имитирует фиброзную дисплазию.
Исходом гиперпластического воспаления кости является развитие гиперостоза, состоящего из зрелых костных структур, напоминающих губчатую остеому.
Оссифицирующий миозит (син.: экзостоз, мышечная остеома) возникает, как правило, вследствие травмы жевательной мышцы. Рентгенологическая картина сфоршировавшегося оссифицирующего миозита довольно характерна. В толще мышцы видно образование костной плотности и костного строения в виде массива компактной кости или ветвящегося образования неправильныхочертаний.
В литературе нет единого мнения о строгом отличии оссифицирующего миозита от посттравматических оссификатов, оссифицирующей гематомы, развивающихся не в толще самой мышцы, а периостально («травматический периостит», «травматические экзостазы»).
Рентгенологически подобные оссификаты обычно характеризуются более отчетливыми контурами округлой формы, иногда симулируютопухоль.
Клиническая картина . Наблюдаются не сильные, ноющие боли и твердое образование в мягких тканях.
Течение оссифицирующего миозита благоприятное. Со временем очаг может уменьшаться и полностью исчезать, особенно если он невелик [Спекторова 3. Г., 1939]. В других случаях очаг в течение многих лет существует, не изменяясь (в одном нашем наблюдении этот срок составил 18 лет). У ряда больных отмечается склонность процесса к рецидивированию после операции. Т. П. Виноградова (1973) связывает рецидивы к конституциональными особенностями.
Оссифицирующий миозит и посттравматические оссификаты иногда приходится дифференцировать от остеогенной саркомы. Клинико-рентгенологические признаки, позволяющие подозревать саркому, могут усугубляться быстро наступающим рецидивом со стремительным ростом оссификата.
Паратиреоидная остеодистрофия является эндокринным заболеванием. Гормон околощитовидных желез действует на всю костную систему, поэтому наряду с челюстными изменениям подвергаются все кости. Идет интенсивная перестройка костей, и вновь образующиеся костные структуры не успевают созревать, что рентгенологически выражается в остеопорозе. Эти изменения и характеризуют паратиреоидную остеодистрофию.
263
ъ
Кроме того, в костях могут возникать образования, не отличи мые по структуре от гигантоклеточной опухоли или кисты. В по добных случаях важно оценить микроскопическую картину в свете общих клинико-рентгенологических данных: исключить или, напротив, обнаружить генерализованные изменения ске лета.
<
При дифференциальной диагностике опухолей и опухолеподобных процессов лицевого скелета у детей клинический диаг ноз не может быть установлен без микроскопического анализа тканевого материала, полученного путем инцизионной биопсии. Наш опыт показывает, что сходство клинико-рентгенологиче ских симптомов многих опухолевых и опухолеподобных процес сов в детском возрасте заставляет проводить клиническую диаг ностику только на основании совокупности данных клиниче ского, рентгенологического и микроскопического исследований.
4
РЕАБИЛИТАЦИЯ ДЕТЕЙ, ОПЕРИРОВАННЫХ ПО ПОВОДУ ОНКОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ
4.1. ПРИНЦИПЫ РЕАБИЛИТАЦИИДЕТЕЙ
Реабилитация детей, оперированных по поводу опухоли или опухолеподобного процесса, проводится методом диспансеризации. При систематическом клиническом наблюдении и лечении диспансеризация позволяет решить следующие задачи:
1) выявить продолжающийся рост опухоли и опухолеподобный процесс, или рецидив заболевания;
2)при злокачественных опухолях выявить регионарные и отдаленные метастазы;
3)провестиортодонтическое лечение;
4)осуществить протезирование зубных рядов или челюстное протезирование;
5)устранить послеоперационный дефект мягких тканей или кости методами восстановительной хирургии.
Диспансерное обеспечение детей должно проводиться в том лечебном учреждении, в котором ребенок был оперирован и где хранится первичная документация. В редких случаях после удаления ограниченных доброкачественных новообразований мягких тканей или альвеолярного отростка ребенка направляют для наблюдения или ортодонтического лечения по месту жительства. Клиники кафедр детской стоматологии должны выполнять роль центров, в которых проводится диспансеризация онкологических больных после удаления доброкачественных новообразований.
В детских стоматологических учреждениях проводится лишь диагностика злокачественной опухоли. Как правило, такие дети находятся на лечении и под диспансерным наблюдением в онкологических центрах.
Частота обследования зависит от характера и степени распространенности новообразования, возраста ребенка, объема оперативного вмешательства. Так, при обширных сосудистых новообразованиях лечение можно проводить в несколько этапов на протяжении нескольких лет, а между этапами лечения выполнять корригирующие пластические операции.
Многие доброкачественные опухоли и опухолеподобные
..процессы склонны к рецидивам или продолжающемуся росту. Например, все сосудистые новообразования мягких тканей
265
растут вместе с ребенком и с возрастом могут появляться новые очаги гемангиомы или лимфангиомы. Как показывает наш опыт, цементомы и цементодисплазии способны к неограниченному росту и распространению в костях лицевого скелета и нередко переходят на кости основания черепа (возможно, так проявляются мультицентрический рост новообразования в про-
цессе роста скелета).
После удаления злокачественных новообразований требуется тщательное и систематическое обследование детей. Метастазирование костных злокачественных опухолей происходит, как правило, на ранних стадиях развития опухоли гематогенным и лимфогенным путем. Метастазы могут быть выявлены в регионарных и отдаленных лимфатических узлах, а также в легких и различных отделах скелета, чаще в области позвоночника, ребер. Приводим одно из наших наблюдений.
Больная А., 4 лет, поступила в клинику в 1965 г. Диагноз: эпулис альвеолярного отростка нижней челюсти. Новообразование размером 2X3 см было удалено вместе с тремя молочными зубами и их зачатками. Гистологическое заключение: ангиоматозный эпулис.
Через 8 мес после операции ребенка привезли в клинику с жалобами на острые боли в животе. Внешне ребенок выглядел удовлетворительно. Снижения массы тела не отмечено. Кожные покровы бледные. При пальпации в брюшной полости выявлены множественные крупные, плотные болезненные новообразования, что расценено как метастазы в лимфатический аппарат брыжейки. Местно в послеоперационной области патологии не об-нафужено. Лимфатические узлы шеи, надключичной и подмышечной обла-ст'и не пальпировались.
С подозрением на наличие метастазов опухоли в брюшную полость ребенок вместе с гистологическими препаратами направлен в онкологический институт. Повторное исследование препаратов: ангиосаркома нижней челюсти, метастазы опухоли в лимфатические узлы брыжейки. Проведена лучевая и химиотерапия. Через год после операции девочка умерла.
В ортодонтическом лечении нуждаются многие онкологические больные. Обширные мягкотканные опухоли (особенно лимфангиомы) вызывают вторичную деформацию лицевого скеле-т.а. При локализации их в мягких тканях щеки, губ, языка сильно деформируется нижняя челюсть, нарушается физиологический прикус. Ортодонтические мероприятия начинают одновременно с лечением новообразования и продолжают до излечения лимфангиомы или до возрастной остановки роста челюстных
костей.
Удаление костных доброкачественных опухолей или опухолеподобных новообразований, как правило, приводит к появлению дефекта зубного ряда или челюстной кости. Дефекты верхней челюсти замещаются съемным челюстным аппаратом, а зубного ряда — съемными протезами. По мере роста ребенка меняют конструкцию и методы фиксации протезов. В детском возрасте послеоперационный протез имеет две функции: восполняет дефект и предупреждает развитие вторичной деформации оперированной и противоположной челюсти в период роста лицевого скелета. Таким образом, послеоперационный
протез одновременно является функционально действующим ортодонтическим аппаратом (рис. 70).
Послеоперационные дефекты или рубцовую деформацию мягких тканей (например, после лечения гемангиом) устраняют пластическими операциями (рис. 71, 72). Требования к пластическим операциям в детском возрасте такие же, как у взрослых, но особое внимание обращают на характер послеоперационных рубцов. Нехватка мягких тканей, их натяжение, грубые рубцы вызывают вторичную деформацию растущих костей лица.
В нашей клинике накоплен большой опыт костнопластических восстановительных операций на нижней челюсти. В связи с этим мы считаем целесообразным поделиться имеющимися данными.
4.2. КОСТНАЯ ПЛАСТИКА НИЖНЕЙ ЧЕЛЮСТИ КАК МЕТОД РЕАБИЛИТАЦИИ ДЕТЕЙ ПОСЛЕ УДАЛЕНИЯ КОСТНЫХ НОВООБРАЗОВАНИЙ
После успешного удаления костного новообразования челюстных костей ребенка нельзя считать здоровым, так как удаление любого костного новообразования связано с образованием дефекта растущей кости. Успешно леченного ребенка с онкологическим заболеванием переводят в другую группу больных,— детей с дефектами челюстных костей, которым необходимодлительноекомплексноелечение.
В этом разделе обобщен наш многолетний опыт использования костнопластического материала при восстановительных операциях нижней челюсти после удаления опухолей и опухолеподобныхобразований удетей.
Детский хирург-стоматолог и ортодонт используют большой арсенал средств для восстановления формы и функции поврежденных отделов челюстно-лицевой области после удаления новообразований. В активе хирургии и ортодонтии пластический метод: реплантация, аутотрансплантация и аллотранспланта-ция костной ткани, использование костно-пластмассовых эндопротезов, неагрессивных металлов и протезов сложных конструкций из полимеров. Все это можно объединить в емкое по-
нятие «реконструктивная хирургия челюстно-лицевой области». Показаниями к костной пластике нижней челюсти у ребенка
являются послеоперационные дефекты с нарушением непрерывностикости.
При наличии костного дефекта в процессе роста лицевого скелета оставшаяся часть нижней челюсти как бы распрямляется под действием жевательных мышц и теряет свойственный ей изгиб в подбородочном отделе. Кроме того, вторично деформируется верхняя челюсть за счет развития зубоальвео-лярного удлинения в месте, противоположном дефекту нижней челюсти. Альвеолярный отросток растет вниз до соприкоснове-
267
266

70.
(продолжение)
г — съемный
70.
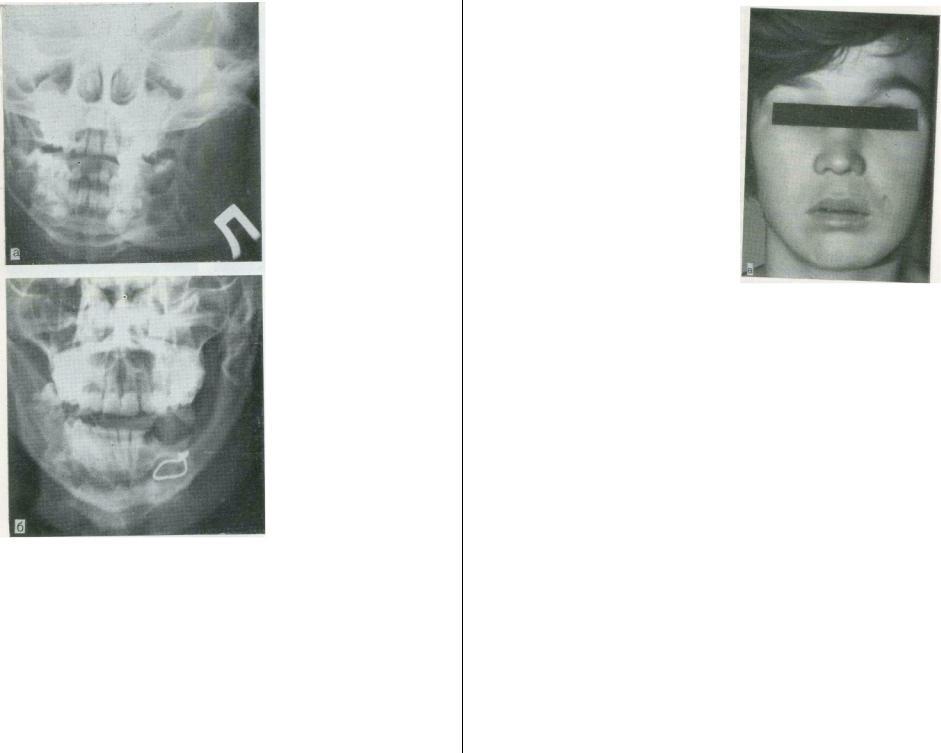
Реабилитация больного с гигантоклеточной опухолью после резекции верхнейчелюсти.
а — томограмма костей лица больного К., 13 лет, до операции; б — больной после резекции: в — послеоперационный дефект.
полый
пластмассовый Функциональный аппарат восполняющий дефект кости и зубного ряда.
ния с мягкими тканями дна рта. Если реконструктивное вмешательство не проводится в течение несколнышх лет, то на стороне дефекта нижней челюсти меняет свойе положение и деформируется
скуловая кость.
Помимо |
костных деформаций лицевого оскелета, развиваются стойкая дисфункция жевательных и |
|||||
мимических |
мышц, атрофия мягких тканей лица и шеи в областей рубца, устранить которые после отсроченной |
|||||
костной |
пластинки оказывается невозможным. Нарушаются функции жеваЫ'ия и артикуляция звуков речи. |
|||||
Изменение |
внешнего облика Дребенка вырабатывает у него чувство собственной неполноценнности, что |
|||||
|
приводит к патологической реакции поведения в деэтском коллективе. Эти |
|||||
|
обстоятельства способствуют расширению показаний и реконструктивным |
|||||
|
операциям на нижней 'челюсти в детском возрасте. Наш опыт |
|||||
|
подтверждает, что костгная пластика нижней челюсти должна быть |
|||||
|
проведена ребеШку независимо от возраста. |
|
||||
|
С 1954 по 1963 г. в клинике кафедры хирургической стоматологии |
|||||
|
ММСИ |
детям |
проведено |
5 |
восстанОовительных |
операций |
|
аутотрансплантатом (ребром во всю птолщу или гребнем подвздошной |
|||||
|
кости). Основной причиной маалого числа таких операций было |
|||||
|
несогласие родителей на дополнительную тяжелую операцию, |
|||||
|
проводившуюся под местНной анестезией, поскольку в то время в |
|||||
|
практике хирургичесиких стоматологических клиник (даже ведущих) |
|||||
|
общее обезбо-оливание не применялось, а также не было опыта |
|||||
|
использования и возможностей полученияконсервированной аллокости. |
|||||
|
После организации кафедры детской стооматологии с 1964 по 1986 г., |
|||||
|
т. е. в течение 22 |
лет, по поводу заболеваний и повреждений нижней |
||||
челюсти нами произведеено детям 186 ал-•лопластических операций с применением кхостных аллотранс-
269

|
71. Реабилитация больного с об- |
|||||
|
ширной кавернозной гемангио-мой |
|||||
|
лица. |
|
|
|
|
|
|
а — больной В., 1 год 1 мес, в процессе |
|||||
|
лечения; б — через год после лечения |
|||||
|
гемангиомы. |
|
|
|
|
|
|
плантатов, из них 86 после- |
|||||
|
удалении опухолей и опухо- |
|||||
|
леподобных |
|
образований |
|||
|
нижней |
|
челюсти. |
Ауто- |
||
|
трансплантация |
кости |
не |
|||
|
проводилась. |
|
|
|
||
Хорошим |
заменителем, |
|
|
|||
аутокости оказалась консер |
вированная аллокость, кото |
|||||
рая неограниченно |
расширя |
|
|
|
|
|
ет возможности костно- |
пла- |
|
|
|
|
|
|
стических |
восстановитель |
|
|||
|
ных операций. Клинически и |
|
||||
|
экспериментально установ |
|
||||
|
лено, что пересаженная ал |
|
||||
|
локость всегда рассасывает |
|
||||
|
ся, замещаясь |
новой кост |
|
|||
|
ной тканью. |
Интенсивность |
|
|||
|
процесса зависит от свойств |
|
||||
|
пересаживаемой |
|
|
|||
|
условий, в которые она по |
|
||||
|
падает, и общей реакции ор |
|
||||
|
ганизма |
на аллотрансплан- |
|
|||
|
тацию. Активная перестрой |
|
||||
|
ка костной ткани при явном |
|
||||
|
преобладании процессов ко- |
|
||||
|
стеобразования над резорб |
|
||||
|
цией обеспечивает успешный |
|
||||
|
исход |
при |
использовании |
|
||
|
аллотрансплантатов |
для костной |
||||
пластики у детей [Волков М. В., Бизер В. А., 1969]. В детском |
||||||
возрасте аллотрансплантаты перестраиваются |
медленнее, чем |
|||||
аутотрансплантаты, и не рассасываются до появления новооб разованнойкости (регенерат).
Об использовании аллокости в детской стоматологической клинике сообщается в ряде работ отечественных авторов [Плотников Н. А., Колесов А. А., 1964; Колесов А. А. и др., 1968; Колесов А. А. и др., 1975; Сысолятин П. Г, 1976; Плотников Н. А., 1979; Соловьев М. М. и др., 1979].
Относительно сроков проведения костной пластики нет единого мнения. В нашей клинике пластику называют первичной или одномоментной, если ее проводят сразу после удаления опухоли, отсроченной — через 1 год и более после удаления опухоли, вторичной, или повторной, — после первичной или от-
270
72. Реабилитация больного Д. с лимфангиомой языка, дна полости рта и шеи.
а — до операции; б — через 6 лет в процессе хирургического и ортодонтического лечения.
сроченной операции, которая была безуспешной вследствие отторжения или рассасывания ранее пересаженного трансплантата. ткани,,
Первичная, или од номоментная, костная п л а с т и к а нижнейчелюсти имеет преимущества перед от сроченной, ибо при ней ребе нок избавлен от дополнитель-
ной травмы— повторной |
one- |
-Ш: |
] |
рации. |
|
Воспринимающее ложе трансплантата имеет достаточное количество хорошо васкуляризованных мягких тканей, способствующих приживлению и перестройке аллотрансплантата. Создаются благоприятные условия для раннего протезирования, а следовательно, и функциональной нагрузки. Все это сокращает сроки перестройки трансплантата и лечения больного. Первичная костная пластика в детском возрасте показана после резекции нижней челюсти по поводу доброкачественных опухолей и опухолеподобных образований, т. е. в тех случаях, когда отсутствует опасность рецидива опухоли и имеется достаточно мягких тканей и слизистой оболочки рта для свободного (без натяжения) укрытия трансплантата. При недостатке мягких тканей и особенно слизистой оболочки рта лучше выполнить отсроченную костную пластику.
271

При значительном дефиците мягких тканей после удаления обширных доброкачественных или злокачественных опухолей для создания ложа трансплантата приходится использовать филатовский стебель.
Отсроченная костная пластика проводится после удаления обширных доброкачественных новообразований, иссечение которых связано с образованием дефицита слизистой оболочки рта, и злокачественных опухолей. В отдельных случаях отсроченная костная пластика проводилась детям, направленным в клинику из других лечебных учреждений, где была произведена резекция нижней челюсти без замещения дефекта кости трансплантатом.
При отсроченной костной пластике биологические условия для приживления трансплантата менее благоприятны. Трансплантат помещают в рубцовый массив между склерозирован-ными концами фрагментов челюсти. Если при одномоментной пластике неизбежно возникает сообщение ложа трансплантата с полостью рта, то при отсроченной такое сообщение крайне нежелательно.
Оптимальные сроки для отсроченной костной пластики следующие: 1) после удаления доброкачественных опухолей — через 3—4 мес, в период наиболее активных репаративных процессов, когда еще нет грубых Рубцовых изменений в мягких тканях и склерозирования концевых фрагментов челюсти; 2) после удаления злокачественных опухолей — не ранее 1,5— 2 лет (в отсутствие рецидива и метастазов). При необходимости подготовки воспринимающего ложа для трансплантата за счет местных тканей или филатовского стебля указанные сроки следует увеличить.
Вторичная (повторная) костная пластика
•осуществляется в тех случаях, когда ранее произведена первичная или отсроченная костная пластика, закончившаяся отторжением трансплантата или его рассасыванием. После отторжения трансплантата пластика показана через 6—8 мес, когда снижается иммунологическая активность, вызванная
•трансплантацией аллокости. При вторичном (повторном) замещении дефектов нижнечелюстной кости у детей создаются
•особенно тяжелые условия, существенно влияющие на исход
•операции.
При первичной, отсроченной и вторичной костной пластике дефектов нижней челюсти у детей аллотрансплантат выполняет следующие функции: 1) анатомическую — восстанавливает непрерывность нижней челюсти и ее форму, что улучшает
•функцию жевательного аппарата и эстетический вид больного; 2) механическую — удерживает костные фрагменты в правильном анатомо-физиологическом взаимоотношении, предупреждая деформацию прикуса и костей всего лицевого скелета; 3) биологическую — стимулирует остеопластические процессы, способствуя более быстрой консолидации его с воспри-
272
нимающим ложем, а также образованию регенерата в области дефекта.
В период с 1964 по 1986 г. костная пластика дефектов нижней челюсти после удаления доброкачественных опухолей и опухолеподобных процессов произведена у 81 ребенка, злокачественных— у 5 детей: по поводу фиброзной дисплазии — у 13, гигантоклеточной опухоли — у 30, фибром — у 21, амелобластомы (адамантиномы)—у 3, миксомы — у 2, обширных костных кист — у 4, ангиофибромы — у одного, костной формы гемангиомы — у 4, гемангиоэндотелиомы — у 4, саркомы — у 5 детей.
По возрасту больные распределялись следующим образом: от 1 года до 4 лет—11, от 4 до 7 лет — 9, от 7 до 12 лет — 39, от 12 до 15 лет — 27 детей. Большинство больных были в возрасте 7— 12 и 12—15 лет, что совпадает с наиболее высокой частотой костных опухолей в детском возрасте.
Первичная костная пластика произведена 68 детям, отсроченная— 18, вторичная — 9 (из них у одного 3 раза, у одного— дважды). Всего выполнено 98 трансплантаций.
В качестве пластического материала использовали 29 лиофилизированных трансплантатов, полученных в лаборатории консервации тканей МОНИКИ, 51 трансплантат, консервированный методом глубокого замораживания, заготовленный нами и полученный в лаборатории консервации тканей ЦИТО, 27 трансплантатов, консервированных другими методами (в слабых растворах формалина и полиэфирных смолах), один костнопластмассовый эндопротез (рис. 73). При замещении дефектов нижней челюсти использовано 37 ортотопических трансплататов, 58
— кортикальной кости, 2 — гребня подвздошной кости и один костно-пластмассовый эндопротез.
4.2.1.Особенностикостнойпластикиудетей
Вреконструктивной хирургии челюстно-лицевой области у •детей особое значение имеют выбор вида пластического материала,
размеры трансплантируемой ткани, расположение алло- |трансплантата в костной ране, способы его фиксации, иммобилизация челюстных костей, а также реабилитация при диспансерном наблюдении в возрасте до 15 лет.
I Анализ отдаленных результатов лечения 186 детей на проггяжении 22 лет, которым реконструктивные операции на нижней челюсти с применением аллотрансплантатов были выполнены по поводу различных патологических процессов, позволяет выделить некоторые особенности костной пластики в детском возрасте.
Как известно, наилучшие условия для формирования репаэативного регенерата создаются при аллотрансплантации коЬтной ткани одинакового анатомического строения с костью реципиента [Надеин А. П., 1969; Плотников! Н. А., 1979]. В этом
Г18—901 |
273 |

73. Реабилитация больной после резекции нижней челюсти по поводу оссифицирующей фибромы левой ветви с одномоментным замещением дефекта костно-пластмассовымэндопротезом.
а — ортопантомограмма больной К-, 12 лет, до операции; б— через 30 дней после операции; в, г
— больная через 3 года после операции.
плане костные ортотопические трансплантаты более приемлемы для замещения дефектов нижней челюсти. Однако значительные различия в детском возрасте таких параметров нижней челюсти, как мыщелковый отросток, ветвь и угол челюсти, не позволяют использовать этот вид трансплантата у детей младшего возраста. Необходимость уменьшать размеры такого трансплантата приводит к обнажению губчатого вещества, нарушению его архитектоники, следствием чего является активная резорбция аллотрансплантата, часто без построения полноценного репаративного регенерата.
Анализ нашего клинического материала показал, что ортотопические аллотрансплантаты целесообразно использовать
274
при костной пластике обширных дефектов нижней челюсти у детей старше 7 лет, а при пластике подбородочного отдела — в любом возрасте. При дефектах любой другой локализации, независимо от возраста ребенка, могут быть успешно применены не только ортотопические, но и кортикальные трансплантаты, смоделированные по форме замещаемого дефекта.
Экспериментальное обоснование достоинств неортотопиче-ских аллотрансплантатов, которые приобретают анатомическое строение, характерное для костной ткани реципиента, дано А. П. Надеиным (1969).
Аллотрансплантаты губчатого строения для замещения дефектов нижней челюсти в детском возрасте применять нецелесообразно, так как они быстро резорбируют без построения регенерата.
Вторая важная особенность костной пластики у детей — размер аллотрансплантата. В связи с возрастными изменениями строения челюстных костей и окружающих тканей, их непрерывным и неравномерным ростом, сопровождающимся интенсивной дифференцировкой тканей, размер используемого аллотрансплантата должен значительно превышать размеры дефекта. Это необходимо для создания гиперкоррекции размеров нижней челюсти в области восстанавливаемого участка, благодаря которой в последующие периоды роста ребенка обеспечивается равномерное развитие здоровой ее половины и постепенное выравнивание оперированной. Чем в более раннем возрасте ребенку производится костная пластика нижней челюсти, тем больших размеров должен быть аллотрансплантатг У всех оперированных нами больных костная пластика произ-'
Л О Л
18
275

.водилась с использованием аллотрансплантата больших размеров, а эффект выравнивания длины челюсти проявлялся в течение 2—3 лет (рис. 74, 75).
Особенности анатомического строения нижнечелюстной ко--сти (тонкий и мало минерализованный слой кости, наличие в "теле челюсти зачатков постоянных зубов) предопределяют единственно возможный способ расположения трансплантата в костной ране
— «внакладку».
Из-за малых размеров челюсти ребенка площадь воспринимающего ложа на концах костных фрагментов редко составляет 1x1 см. Чаще приходится формировать воспринимающее ложе болееэкономно.
Способы фиксации трансплантата в ране в детском возрасте также имеют особенности. Фиксация трансплантата в костной ране производится чаще одинарным, реже двойным швом кости, проволочной лигатурой марки 1Х18Т9Ю, диаметр которой не
более 0,6 мм.
Особенности строения молочного и сменного прикуса (тре-мы и диастемы, наличие зубов с резорбирующимися или несформированными корнями) существенно затрудняют иммобилизацию челюстей. Как показал наш опыт, в период молочного и сменного прикуса прочную иммобилизацию костных фрагментов челюсти обеспечивают назубные капповые аппараты из рластмассы с зацепными петлями. Для иммобилизации челюстей после 98 костных пластик по поводу опухолей использовались назубные шины: каппы с зацепными петлями — у 71, аппарат Рудько —у 9, проволочные шины с зацепными петлями— у 8, шина типа Ванкевич в сочетании с пращевидной повязкой— у 10
детей.
Накостные аппараты у детей практически неприменимы, поскольку травмируют зоны роста кости и зачатки зубов. Кроме того, постоянное давление крючков накостных аппаратов на мало минерализованную костную ткань приводит к появлению вокруг них очагов деструкции, в результате чего возникает патологическая подвижность фрагментов челюсти и аллотран-
еплантата.
Ортодонтическое лечение после костной пластики необходимо проводить до окончания роста костей лицевого скелета. Это возможно только при диспансерном наблюдении хирурга и ортодонта за ребенком до достижения им 15 лет. При необходимости лечение продолжают и вболеестаршемвозрасте.
Предоперационная подготовка ребенка к костной пластике— один из факторов, определяющих исход лечения. Наиболее подробное описание предоперационной подготовки к рекон- структивно-восстановительной операции опорно-двигательного аппарата ребенка приводят М. Д. Дмитриев и соавт. (1974).
Специфика челюстно-лицевой области в возрастном аспекте, особенности местных изменений при свежих и старых дефектах нижней челюсти потребовали разработки системы об-
74.
Реабилитация больной после резекции по поводу фиброзной дисплазии нижней челюсти и первичной костной пластики аналогичным аллотрансплантатом. а— больная М., 5 лет, до операции; б-через 23 года после операции (лечилась у ортодонта, протезирована); в — рентгенограмма тон же больной через 4А года после операции.
щих и специальных мероприятий, которые мы считаем необходимыми при подготовке ребенка к первичной, отсроченной и вторичной костной пластикенижнейчелюсти.
Общая подготовка ребенка предусматривает:
1) тщательный анализ анамнеза, определение давности перенесенныхзаболеваний;
277
276
тер-
278
75.
Реабилитация больной после резекции нижней челюсти по поводупервичной(примордиальной) нагноившейся кисты нижней челюсти с.пер-вичной костной пластикой аналогичным алло-трансплантатом.
а — рентгенограмма больной в возрасте 6 лет до операции; б — через 20 лет после операции;
2)выделение группы заболеваний, при которых проведение костной пластики нецелесообразно (активные формы туберкулеза, сахарный диабет, системные костные заболевания, болезни крови, хронические заболевания паренхиматозных органов
встадии декомпенсации);
3)выявление заболеваний, требующих обязательного лечения в предоперационном периоде (воспалительные заболевания ЛОР-органов, острые и хронические заболевания верхних дыхательных путей, гиповитаминозы, анемии
и др.).
В связи с анатомической и функциональной незрелостью ряда органов и систем (ЦНС, паренхиматозные органы,
морегуляция, водно-солевой баланс
и т. д.) при |
подготовке к операции |
||||
необходимо |
учитывать высокую |
||||
чувствительность ребенка к |
|
||||
воздействию |
внешней и |
|
|||
внутренней |
среды. |
Чем моложе |
|||
ребенок, |
тем ярче |
проявляются эти |
|||
особенности. |
В |
противном случае |
|||
в послеоперационном периоде |
|
||||
общие симптомы любого |
|
||||
заболевания |
начинают преобладать |
||||
над местными, что сказывается на |
|||||
исходе костной пластики. Общие |
|||||
санационные |
мероприятия |
|
|||
желательно |
проводить не позднее |
||||
чем за 1—2 мес |
до костной |
|
|||
пластики. |
Это осуществимо при |
||||
планировании |
отсроченной |
и |
|||
вторичной |
|
пластики. Однако при |
|||
первичной пластике, когда |
|
||||
операцию' |
нельзя откладывать |
из-за |
|||
интенсивного |
роста |
75. (продолжение) |
|||
доброкачественной |
опухоли или |
||||
опухолеподобного |
процесса,вы- |
||||
•
полнить указанные мероприятия
в полном объеме не представляется возможным. В таких случаях санацию осуществляют во время специальной подготовки и в послеоперационном периоде.
В зависимости от того, будет ли пластика первичной, отсроченной или вторичной, специальная предоперационная подготовка различна по продолжительности и объему мероприятий.
К специальным мероприятиям, проводимым независимо от вида костной пластики, относятся:
1) санация рта: лечение кариеса зубов, его осложнений, снятие зубных отложений, удаление молочных зубов с резор-
бированными корнями, лечение заболеваний и травматических ' повреждений слизистой оболочки не менее чем за 3—4 нед до
первичной костной пластики;
2) клиническое и рентгенологическое исследование костей лицевого скелета и нижней челюсти для определения протяженности будущего или имеющегося дефекта;
3)изготовление контрольных гипсовых моделей, по которым также можно определить величину дефекта, степень деформации челюстей, зубных рядов, положение зубов и установить степень требуемой «гиперкоррекции» трансплантата;
4)фотографирование больного до операции, что позволяет проследить динамику восстановления контуров лица;
5)выбор способа фиксации трансплантата в костной ране;
279
6)выбор конструкции иммобилизирующего аппарата и его изготовление;
7)подбор аллотрансплантата по структуре ткани, виду и размеру.
До проведения отсроченной и вторичной костной пластики обязательны обследование и ортодонтическое лечение. Последнее должно предшествовать хирургическому и не может быть перенесено на послеоперационный период.
Конструкцию ортодонтического аппарата выбирают в зависимости от результатов рентгенологического исследования и контрольных моделей челюстей.
Совместная работа хирурга, ортодонта и терапевта-стомато- лога— обязательное условие на всех этапах проведения ребенку костной пластики: в предоперационном, послеоперационном периодах и в дальнейшем.
Планируя лечение, детей с послеоперационными дефектами и деформациями нижней челюсти после удаления опухолей можно разделить на три группы.
1. Дети, которым костная пластика проводится одновременно с удалением опухоли нижней челюсти. Этих детей готовит к операции группа в составе хирурга-стоматолога, ортодонта, терапевта-стоматолога, педиатра, анестезиолога и по показаниям других специалистов. Время подготовки не более 3—4 нед, иногда меньше, что зависит от темпов роста опухоли, давности ее обнаружения, общего состояния ребенка.
2. Дети, которым по показаниям костная пластика не планируется как одномоментная. С момента выписки их из лечебного учреждения этих больных должен лечить ортодонт. Ребенку изготовляют функциональный ортодонтический аппарат, удерживающий фрагмент или фрагменты челюсти в правильном анатомическом положении до проведения реконструктив-но- восстановительной операции и предупреждающий вторичную деформацию челюстей. В зависимости от характера проведенного ранее лечения период диспансерного наблюдения до операции продолжается от 4—8 мес до 1,5 года. В остальном объем предоперационной подготовки не отличается от такового в первой группе.
3. Дети, которым после удаления опухоли не проводились костная пластика и ортодонтическое лечение. Длительное время перед операцией они должны подвергаться ортодонтиче-скому лечению для нормализации соотношения зубных рядов и прикуса. Результат лечения зависит от времени, прошедшего после удаления опухоли нижней челюсти, возраста больного и состояния прикуса. Сроки костной пластики у таких больных планируются строго индивидуально и зависят от результатов ортодонтического лечения. В дальнейшем подготовка ведется так же, как в первой группе.
К первичной костной пластике все 68 детей были подготовлены по данной схеме.
Из 18 детей, которым выполнена отсроченная костная пластика, 4 оперированным в нашей клинике и 2 оперированным в-других клиниках в течение всего периода подготовки к .операт-ции проводилось ортодонтическое лечение. Десяти детям, которые обращались в нашу клинику через 2—3 года и более после удаления опухоли нижней челюсти, ортодонтическое лечение раньше не проводилось, в результате чего были выявлены значительные изменения костных фрагментов и вторичная деформация верхней челюсти. У них обнаружены уменьшение размеров дефекта за счет рубцов, деформация прикуса, аномалии положения зубов, обнажение корня зуба, расположенного-по краю дефекта, с резорбцией альвеолы зуба, значительное изменение внешнего вида. Ортодонтическое лечение в предоперационном периоде полного эффекта не дало.
Из 9 детей, которым проведена вторичная костная пластика, 7 детей, ранее лечившихся в нашей клинике, в период до-повторной операции систематически получали ортодонтическое лечение.
Лечение после реконструктивно-восстановительных операций предусматривает:
1)послеоперационную терапию и профилактику инфекции;
2)иммобилизацию челюстей, наблюдение за послеопера-
ционной раной;
3)клинико-рентгенологический контроль за репаративной регенерацией и качеством формирования регенерата;
4)ортодонтическое лечение и рациональное протезирование;
5)диспансерное наблюдение до окончания роста костей лицевого скелета с постоянной ортодонтической коррекцией прикуса.
Всем больным после костной пластики на 12—14 дней назначали курс антибактериальной, десенсибилизирующей, общеукрепляющей терапии и при необходимости повторяли его.
Окончательную иммобилизацию челюстей проводили на второй день после операции и продолжали 50—56 дней, т. е. до> наступления прочной консолидации фрагментов с трансплантатом, что контролировали серией рентгенограмм. Особенности-детского возраста исключают возможность сокращения сроков-, иммобилизации, так как недостаточная минерализация костной ткани, даже при условии более быстрого образования костной мозоли, чем у взрослых, под влиянием функциональной нагрузки может быть причиной неполного формирования регенерата или его резорбции.
В течение всего послеоперационного периода проводилитщательный уход за полостью рта (многократное орошение полости рта слабыми растворами антисептиков), контролировали степень фиксации иммобилизующих аппаратов. После снятия швов назначали охранительный режим.
После снятия иммобилизующей аппаратуры всем детям изготавливали шины типа Ванкевич или ее модификации, в ре-
28В
280
