
zadat-fkh
.pdf
2.7 Для превращения цианида аммония в мочевину при Т = 35 °С были найдены следующие периоды полураспада при различных исходных концентрациях:
С, моль/л |
0,20 |
0,10 |
0,05 |
t1/2, ч |
9,45 |
19,15 |
37,03 |
Какого порядка эта |
реакция? |
|
|
2.8 Пользуясь зависимостью между временем полураспада и давлением, определить порядокдля реакцииконверсиипараводородавортоводород.
Р×10-5,н/м2 |
0,067 |
0,133 |
0,267 |
0,533 |
t, с |
648 |
450 |
318 |
222 |
2.9 Исследовалась кинетика каталитического распада аммиака на простые вещества. Время полураспада зависит от начального давления аммиака
так: |
|
|
0,267 |
Р×10-5,н/м2 |
0,067 |
0,133 |
|
t, с |
648 |
450 |
318 |
Определить порядок реакции и константу скорости.
2.10 Определить порядок реакции
СН3СООСН3 + NaОН 'С2Н4 + Н2 + СО
по изменению давления в ходе реакции. Найти среднее значение константы скорости.
Р×10-3 н/м2 (общее) |
|
41,6 |
|
54,5 |
|
63,7 |
|
|
74,2 |
|
||
t, мин |
|
|
|
0 |
|
6,5 |
|
13,0 |
|
|
19,9 |
|
2.11 Определить константу скорости и порядок реакции |
|
|
|
|||||||||
N2О5 'N2О4 + 1/2 О2 |
|
|
|
|
|
|
|
|
||||
t |
0 |
|
184 |
319 |
526 |
867 |
1198 |
1877 |
3144 |
|||
а |
2,33 |
|
2,08 |
1,91 |
1,68 |
1,36 |
1,11 |
0,72 |
0,34 |
|||
где а – концентрация N2О5, моль/л.
2.12 Определить порядок стадии, определяющей скорость пиролиза В2Н6 из данных по скорости увеличения давления в зависимости от исходной
концентрации В2Н6. |
|
|
||||
о |
|
× |
2 |
2,153 |
0,433 |
|
С(В2Н6 |
10 ,моль/л) |
|
|
|||
∆ |
Р/ |
∆ × |
4 |
|
7,4 |
0,73 |
|
t 10 ,моль/л час |
|
|
|||
2.13 Определить порядок реакции
СН3СООСН3 + NaОН 'С2Н4 + Н2 + СО
по изменению давления в ходе реакции. Найти константу скорости.
t, мин |
0 |
6,5 |
13,0 |
19,9 |
Р, мм. рт ст |
312 |
408 |
488 |
562 |
81
2.14 Для реакции 2 NО + 2 Н2 ' N2 + 2 Н2О
если исходные газы взяты в эквивалентных количествах при Р = 0,454×105 Па тоихдавлениеуменьшаетсявдвоеза102 секунд, еслижеисходное Р = 0,384×105 Па, то уменьшаетсявдвоеза140секунд.Найтипорядокреакции.
2.15Было найдено, что в некоторой реакции при изменении начальной концентрации с 0,502 до 1,007 кмоль/м3период полураспада уменьшается от 51 до 26 секунд. Каков порядок этой реакции и чему равна константа скорости?
2.16При разложении азотного ангидрида в ССl4 при 30 ˚С исходная концентрация N2О5, равная 84,85 см3/л через 8717 секунд. Каков порядок реакции?
2.17Два вещества вступают в реакцию. Каков порядок реакции, если за периоды времени, прошедшие от начала реакции: 5, 15, 30 минут, количество прореагировавших веществ составило: 19,8; 46,7; 77 %?
2.18Начальная концентрация реагирующего вещества уменьшилась за 10 минут вдвое. Начальная концентрация в 5 раз большая того же вещества, уменьшилась вдвое за 24 секунды. Определить порядок реакции.
2.19По мере течения реакции между эквивалентными количествами СО и
Cl2 согласно уравнению СО + Cl2 → СОCl2 наблюдалось следующее уменьшение общего давления:
t, мин |
0 |
5 |
10 |
15 |
21 |
|
|
|
|
|
|
Р×10-5 Па |
0,965 |
0,900 |
0,829 |
0,779 |
0,735 |
Определить порядок реакции, константу скорости.
2.20 В некоторой реакции при изменении начальной концентрации с 0,502 до 1,007 моль/л период полураспада уменьшился от 51 до 26 секунд. Какой порядок реакции и чему равна константа скорости?
Задача 3
3.1Реакциятермическогоразложениягазообразнойокисиэтиленапри478,5 оСпротекает по 1 порядку. Период полураспада при этой температуре равен 363 мин. Энергия активацииравна217 кДж/моль. Определитьконстантускоростиреакциипри450°С.
3.2Константа скорости реакции 1 порядка при 303 К 2,2·10-3 мин-1, а при 308,2 К 4,1·10-3 мин-1. Вычислить энергию активации и время, в течение которого при 313,2 К разложится 99,99 % вещества.
82
3.3Константа скорости омыления уксусноэтилового эфира едким натром при 282,6 К равна 2,37, а при 287,6 К равна 3,204. При какой температуре константа скоростиравна4?
3.4Двереакцииодинаковогопорядкаимеют равныепредэкспоненциальныемножители, ноихэнергииактивацииразличаютсяна10 ккал/моль. Рассчитайтеотношенияихконстант при600К.
3.5 Константаскорости инверсии тростниковогосахарапри25 °Сравна9,67·10 -3, апри 40°С равна73,4·10-3 мин-1.Определитьконстантускоростиэтойреакциипри 35°С.
3.6Константыскоростиреакции2 порядкапри328,2 и298,2 Ксоответственноравны1·10-2 и1·10-3мин-1·моль-1·л. Вычислитьскоростьэтойреакциипри342,2 Квначальныймомент реакции,если начальные концентрацииобоих веществодинаковы и равны 0,01моль/л.
3.7Муравьиная кислота разлагается на диоксид углерода и водород. Константа скорости при 140 °С равна 5,5·10 - 4, а при 185 °С – 9,2·10 -3. Вычислить энергиюактивациииконстантускоростипри150°С.
3.8Разложениенекотороговещества пореакции1 порядкаимеетэнергиюактивации231 кДж./моль. При300 Кразложениеидетсоскоростью95 % вчас. Вычислитьтемпературу, прикоторойэтовеществоразлагаетсясоскоростью0,1% вминуту.
3.9Время половинного распада вещества в реакции первого порядка при 323,2 К составляет 100 мин, а при 353,2 К 15 минут. Вычислить температурный коэффициент константы скорости этой реакции.
3.10Следующие значения для К скорости реакции первого порядка были
определены при |
разложении |
ацетондикарбоновой |
кислоты в одном |
|||||
растворе: |
|
|
|
|
|
|
||
|
t °С |
|
0 |
|
20 |
40 |
|
60 |
|
К · 106 |
|
2,46 |
|
47,5 |
576 |
|
5480 |
Определить графически энергию активации.
3.11 Константа скорости омыления уксусноэтилового эфира едким натром равна 2,37 при 9,4 °С, а при 14,4 °С – 3,204. Вычислить, при какой температуре константаскоростибудетравна15.
3.12 Вычислить энергию активации реакции, если |
при Т1 = 456,2 К, |
К1 = 0,942·10-6, а при Т2 = 700, К2 = 0,310·10-2. Найти К3 при Т = 923 К и |
|
вычислить, сколько вещества прореагирует через 17 |
мин, если С0 = 2,38 |
к/моль м3. Реакция первого порядка. |
|
83

3.13 Для некоторой реакции 1 порядка период полураспада при 378,5 К равен 363 мин. Энергия активации равна 2,184·105 Дж/моль. Определите, сколько времени потребуется для разложения 75 % исходного вещества при 450 К.
3.14 Вычислить |
энергию |
активации реакции |
H2 + Br2 '2 HBr, |
если |
при |
|||||
Т1 = 574,5 К К1 = 0,0856; при Т2 = 497,2 К |
К2 = 0,00036. Найти К3 при Т3 = 483,2 и |
|||||||||
определить,скольковещества |
прореагировало |
кмоментувремени τ = 60 минут, если |
||||||||
С0А = С0В = 0,03 кмоль/м3. Порядок реакции считать по молекулярности. |
|
|||||||||
3.15 Вычислить |
энергию |
активацию реакции |
2NО 'N2 + O2, |
если |
при |
|||||
Т1 = 1525 К |
К1 = 47059; приТ2=1251 К К2 = 1073. НайтиК3 приТ3 = 1423 ивычислить, |
|||||||||
сколько вещества прореагирует к τ =45 мин, если С0=2,83 кмоль/м3. Реакция 2 |
||||||||||
порядка. |
|
|
|
|
|
|
|
|
|
|
3.16 Дана зависимость константы скорости разложения N2O5 от температуры: |
||||||||||
|
Т |
273 |
298 |
308 |
|
318 |
|
328 |
338 |
|
|
К, сек-1 |
7,67·10-7 3,46·10-5 1,46·10-4 |
4,98·10-4 |
1,50·10-3 |
4,87·10-3 |
|||||
Найти графически энергию активацию, константу скорости при 323 оС и предэкспоненциальный множитель.
3.17 В растворе, содержащем 0,1 кмоль этилацетата и 0,1 кмоль NaOH при 283,2 К в течение 15 минут омыляется 10 % эфира, а при 298,2 К за тот же промежуток времени 20 %. Реакция второго порядка. Сколько эфира омыляется в течение 5 минут при 313,2 К?
3.18 Константа скорости реакции |
разложения |
органической кислоты при |
|
20 оС 4,75·10-4, |
а при 40 оС |
5,76·10-3 |
мин-1. Определить период |
полупревращения |
при 30 оС, если эта реакция первого порядка. |
||
3.19Для реакции 2 порядка при СА0 = СВ0 = 0,1 кмоль/м3 и Т=300,2 К время прохождения наполовину равно 200 мин, а при 320,2 К 40 мин. Вычислить время прохождения реакции на 99 % при 330 К и СА0 = СВ0 = 0,01 кмоль/м3.
3.20Во сколько раз возрастет скорость реакции при повышении температуры от 25 до 100 °С, если энергия активации равна 30 ккал/моль.
|
|
|
|
|
|
|
|
|
|
Задача 4 |
|
|
4.1 |
|
Описать |
|
кинетическое |
поведение |
каждого из |
веществ реакции |
|||||
|
|
|
K1 |
|
K3 |
|
|
|
||||
A |
|
|
|
|
2B+C |
|
|
|
2D |
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
K2 |
|
K4 |
|
|
|
||||
4.2 |
|
Описать |
|
|
кинетику |
реакции |
при |
помощи системы |
||||
дифференциальныхуравнений
84
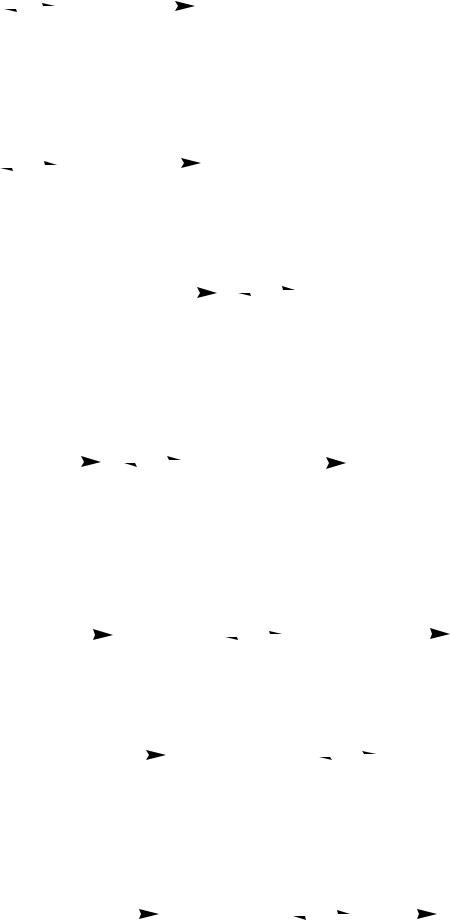
2A+B |
|
K1 |
2D A+C |
K2 |
3P |
|
|
|
|
|
|||
|
K-1 |
|
||||
|
|
|
|
|
||
4.3 Описатькинетикуреакцииприпомощисистемыдифференциальныхуравнений
|
|
K1 |
|
|
K2 |
||
A+B |
|
|
|
C |
2A+2C |
|
D |
|
|
|
|
||||
|
K-1 |
||||||
|
|
|
|
|
|
||
4.4 Описатькинетикуреакцииприпомощисистемыдифференциальныхуравнений
|
K |
|
|
K2 |
||
2A+B |
1 |
3P |
|
|
|
D |
|
|
|
|
|||
|
|
|
|
|||
|
|
|
|
K3 |
||
4.5 Описатькинетикуреакцииприпомощисистемыдифференциальныхуравнений
|
|
K |
|
|
K2 |
|
K |
|
||
. |
A |
1 |
2P |
|
|
|
C |
2A |
3 |
D |
|
|
|
|
|
||||||
|
|
|
|
|
||||||
|
|
|
|
|
K-2 |
|
|
|
||
4.6 Описатькинетикуреакцииприпомощисистемыдифференциальныхуравнений
|
|
K1 |
|
|
|
K2 |
|
|
K4 |
|
. |
A+B |
|
P |
P+2B |
|
|
|
R 1/2R+2P |
|
C |
|
|
|
|
|||||||
|
|
K3 |
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
4.7 Описатькинетикуреакцииприпомощисистемыдифференциальныхуравнений
|
|
K1 |
|
|
|
K2 |
||
. |
A+2B |
|
P |
1/2A+P |
|
|
|
C |
|
|
|
||||||
|
|
|
|
|||||
|
|
|
|
|
|
K3 |
||
4.8 Описатькинетикуреакцииприпомощисистемыдифференциальныхуравнений
. |
2A |
K1 |
P |
A+1/2B |
|
K2 |
|
C |
K3 |
2D |
|
|
|
|
|
||||||
|
|
K4 |
|
|
||||||
|
|
|
|
|
|
|
|
|
|
85

4.9 Описатькинетикуреакцииприпомощисистемыдифференциальныхуравнений
|
|
K |
|
|
|
K2 |
||
. |
A+B |
1 |
P |
A+2P |
|
|
|
C |
|
|
|
|
|||||
|
|
|
|
|||||
|
|
|
|
|
|
K3 |
||
4.10 Описатькинетикуреакцииприпомощисистемыдифференциальныхуравнений
. 1/2A+B |
|
K1 |
|
P+C |
A+3P |
K2 |
C+2D |
|
|
|
|
||||
|
K3 |
|
|
||||
|
|
|
|
|
|
|
4.11 Описатькинетикуреакцииприпомощисистемыдифференциальныхуравнений
|
|
K2 |
|
|
K1 |
||||
. A+B |
|
|
|
C |
2A+1/2C |
|
|
|
D |
|
|
|
|
||||||
|
|
|
|
|
|||||
|
|
K3 |
|
|
K4 |
||||
4.12 Описатькинетикуреакцииприпомощисистемыдифференциальныхуравнений
|
|
K |
|
K |
2 |
|
|
K3 |
||
A |
1 |
|
B |
|
C |
1/2A+C |
|
2D |
||
|
|
|
|
|
|
|||||
|
K |
|
|
|||||||
|
-1 |
|
|
|
|
|
|
|
||
4.13 Описатькинетикуреакцииприпомощисистемыдифференциальныхуравнений
|
K1 |
|
|
|
K2 |
|
|
K |
|
. 2A+B |
|
C |
|
A+2D |
|
H |
1/2C+D |
3 |
P |
|
|
|
|
||||||
|
K-1 |
|
|
|
|
|
|
||
4.14 Описатькинетикуреакцииприпомощисистемыдифференциальныхуравнений
. A+2B |
|
K1 |
2C |
K2 |
D |
|
|
|
|
|
|||
|
K-1 |
|
||||
|
|
|
|
|
||
86
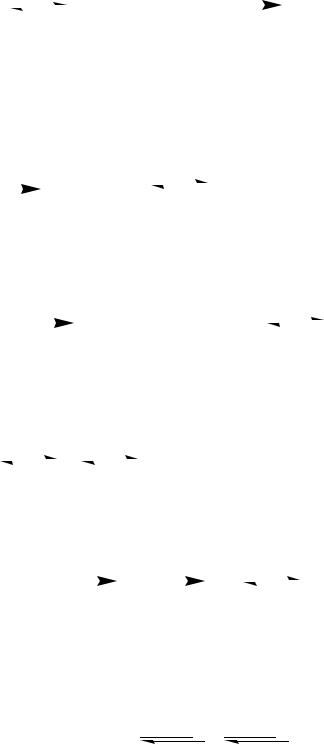
4.15 Описатькинетикуреакцииприпомощисистемыдифференциальныхуравнений
. A+C |
|
K1 |
|
B+D |
1/2A |
K2 |
2B |
|
|
|
|
|
|
||||
|
K-1 |
|
|
|||||
|
|
|
|
|
|
|
||
4.16 Описатькинетикуреакцииприпомощисистемыдифференциальныхуравнений
|
K1 |
|
|
|
K2 |
||
. A |
B |
2A+C |
|
|
|
B+2D |
|
|
|
|
|
||||
|
|||||||
|
|
|
|
|
K3 |
||
4.17 Описатькинетикуреакцииприпомощисистемыдифференциальныхуравнений
|
K1 |
|
|
|
K2 |
||
.2A+K |
|
AK |
AK+2B |
|
|
|
C+K |
|
|
|
|||||
|
|
|
|
||||
|
|
|
|
|
K3 |
||
4.18 Описатькинетикуреакцииприпомощисистемыдифференциальныхуравнений
|
|
K1 |
|
K |
||||
. 2A |
|
|
|
B |
3 |
|
C |
|
|
|
|
|
|||||
|
|
|
|
|
||||
|
|
K2 |
|
|
|
|
||
4.19 Описатькинетикуреакцииприпомощисистемыдифференциальныхуравнений
|
K |
|
K |
|
|
K3 |
||
. 3A |
1 |
B |
2 |
2C |
|
|
|
D |
|
|
|
|
|
||||
|
|
|||||||
|
|
|
|
|
||||
|
|
|
|
|
|
K4 |
||
4.20 Описать кинетику реакции при помощи системы дифференциальных уравнений
1/2A+B K1  C K3
C K3  2D
2D
K2 K4
Задача 5
87

5.1 Определить концентрации веществ А, В, С последовательной реакции
A |
K1 |
B |
K2 |
C |
через 2 часа от начала реакции. Исходная концентрация |
|
|
вещества А 1 моль/л. Определить время |
достижения максимальной концентрации |
||||||||
веществаВ, t , если К = 0,4 час-1 ; К |
= 0,3 час-1. |
|
|||||||
|
|
max |
1 |
2 |
|
|
|
||
5.2 В реакционном |
сосуде |
протекает |
последовательно |
реакция первогопорядка |
|||||
A |
K1 |
B |
K2 |
C, гдеК |
= 0,5 час-1; К |
= 0,2 час-1; С° = 2моль/л. Определить |
|||
|
|
|
|||||||
|
|
|
|
|
1 |
|
|
2 |
А |
максимальный выход вещества В. Как изменится время достижения максимальной концентрации вещества В, если К1 останется без изменений, а К2 увеличится в 2
раза?
5.3 Впоследовательнойреакциипервогопорядка
A |
K1 |
B |
K2 |
C |
|
|
К1=0,5час-1; К2 = 0,1 час-1; С°А= 2 моль/л.
Определить концентрации всех веществ через 5 часов от начала реакции. Определите время, закотороепрореагируетполовинавеществаА.
5.4 Для реакции изомеризации β-оксикротонового эфира в ацетоуксусный эфир при 25 ˚С концентрация исходного вещества была взята 0,366 моль/л. Через 71,8 часа концентрация его стала 0,277 моль/л. Найти константы скорости прямой и обратной реакции, если конечная, не изменяющаяся более, концентрация стала
0,078 моль/л.
5. 5.При превращении эфира (1) в изомер эфир (2) через 215,8 часа концентрация эфира (1) изменилась с 0,366 моль/л до 0,174 моль/л. Равновесная концентрация эфира(1) равна 0,078 моль/л. Найтиконстантыскоростипрямойиобратнойреакции.
5.6 Константы скорости прямой и обратной реакций равны 40,3·10-4 час-1 и 10,9·10-4 час-1. РавновеснаяконцентрациявеществаАравна0,078 моль/л.
Сколько % вещества А прореагирует через 383 часа, если исходная концентрация быларавна0,366 моль/л?
5.7 Превращение γ-оксимасляной кислоты в γ-лактон является обратимой мономолекулярной реакцией. В результате опытов былиполученыследующие данные:
t,мин |
21 |
50 |
100 |
120 |
160 |
200 |
∞ |
Х,моль |
2,41 |
4,96 |
8,11 |
8,9 |
10,35 |
11,55 |
13,28 |
лактона |
|
|
|
|
|
|
|
88

Начальноеколичествокислотыа= 18,23 моль. Рассчитать константыскоростипрямойи обратнойреакциииКравновесия.
5.8 Дляобратимойреакции
K1
A
 B
B
K2
С°А = 2 моль/л. Через 10 минут после начала реакции концентрация вещества А
уменьшилась на 25 %. Определить концентрацию вещества А через 30 минут от началареакции, если (К1/К2)= 3,5.
5.9 В системе осуществляется реакция A |
K1 |
B |
|
K2 |
C. |
|
|
|
|
||||
Рассчитать |
максимальную концентрацию вещества В и время её достижения, |
|||||
если К = 5,1·10-8 час-1; К = 2,5·10-8 час-1; С° |
= 0,25моль/л. |
|||||
1 |
2 |
|
А |
|
|
|
5.10 Вобратимойреакции
K1
A
 B
B
K2
через 30 минут от начала реакции вещества А осталось 80 %, а равновесное его количество составило 40 % от первоначального. Найти константы скорости прямой и обратнойреакции.
5.11 ОпределитьконцентрациивеществаА, В, Споследовательнойреакциичерез2 часаотначалареакции
A |
K1 |
B |
|
K2 |
C |
|
|
|
|||
Исходная концентрация |
вещества А 1 моль/л. Определить время достижения |
||||
максимальнойконцентрациивещества(τmax), еслиК1 = 0,4 час-1; К2 = 0,3 час-1.
5.12 .В реакционном сосуде протекает последовательно реакция первогопорядка,
К1 = 0,5час-1; К2=0,2час-1; С°А = 2моль/л.
A |
K1 |
B |
K2 |
C |
|
|
Определить максимальный выход вещества В. Как изменится время достижения максимальной концентрации вещества В, если К1 останется без изменений, а К2
увеличитсяв2раза?
89

5.13 Впоследовательнойреакциипервогопорядка
A |
K1 |
B |
K2 |
C |
|
|
К1 = 0,5 час-1; К2 = 0,1 час-1; С°А= 3 моль/л. Определить концентрации всех
веществ через 5 часов от начала реакции. Определить время, за которое прореагирует половинавеществаА.
5.14 Для |
реакции |
изомеризации β-оксикротонового |
|
эфира |
в |
ацетоуксусный эфир при 25 ˚С концентрация исходного вещества |
была взята |
||||
0,366 моль/л. Через 71,8 часа концентрация его стала 0,277 |
моль/л. Найти |
||||
константы |
скорости |
прямой и обратной реакции, если |
конечная, |
не |
|
изменяющаяся более, |
концентрациястала0,078 моль/л. |
|
|
|
|
5.15При превращении эфира (1) в изомер эфир (2) через 215,8 часа концентрация эфира (1) изменилась с 0,366 моль/л до 0,174 моль/л. Равновесная концентрация эфира (1) равна 0,078 моль/л. Найтиконстантыскоростипрямойи обратной реакции.
5.16Определить концентрации вещества А, В, С последовательной реакции через 2 часаотначалареакции
A |
K1 |
B |
K2 |
C |
|
|
Исходная концентрация вещества А 1 моль/л. Определить время достижения
|
максимальнойконцентрациивещества(τ |
), еслиК |
1 |
= 0,4час-1; К |
= 0,3час-1. |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
max |
|
2 |
|
|
||||
5.17 |
Превращение |
γ-оксимасляной кислоты в γ-лактон |
является |
обратимой |
|||||||||||||||
|
мономолекулярной реакцией. В результате опытов былиполученыследующиеданные: |
||||||||||||||||||
t,мин |
|
|
21 |
|
50 |
100 |
120 |
|
160 |
200 |
|
∞ |
|
||||||
Х,моль |
|
|
2,41 |
|
4,96 |
8,11 |
8,9 |
|
10,35 |
11,55 |
|
13,28 |
|
||||||
лактона |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
||||||||||||||
Начальноеколичествокислотыа= 18,23 моль. Рассчитать |
константыскорости прямой и |
||||||||||||||||||
обратнойреакциииКравновесия. |
|
|
|
|
|
|
|
|
|
||||||||||
5.18 Дляобратимойреакции |
|
|
|
|
|
|
|
|
|
|
|||||||||
A |
|
|
K1 |
B |
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
K2 |
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
С°А = 2 моль/л. Через 10 минут после начала реакции концентрация вещества А
уменьшилась на 25%. Определить концентрацию вещества А через 30 минут от началарешении, если (К1/К2)= 3,5.
90
