
zadat-fkh
.pdf5.19Определить стандартную теплоту образования этана, пользуясь энергиями связей.
5.20Определить стандартную теплоту сгорания изобутана, пользуясь энергиями связей.
Задача 6
6.1Вычислить тепловой эффект разложения 50 г карбоната кальция
СаСО3 = СаО +СО2 при 298 К: а) при постоянном давлении б) при постоянном объеме (используя справочные данные) .
6.2В топке сгорает каменный уголь, содержащий 65 % С. В топочных газах
содержится 13 % (мол.) СО2 и 1 % СО, остальное - азот и кислород. Определить теплоту сгорания 1 кг угля, если известно, что теплота
образования СО2 составляет -393,5 кДж/моль, теплота образования СО
-110,5 кДж/моль.
6.3 Используя таблицы стандартных величин, рассчитать тепловой эффект
реакции 2Н2 + СО = CH3OH(газ) при 298 К и Р = 1,033·105 Па; при: а) постоянном давлении, б) постоянном объеме.
6.4 При растворении 32 г CuSO4 в 80 г Н2О выделяется 13,2 кДж, а при растворении 59 г СuSO4·5Н2О в том же количестве воды поглощается 2,34 кДж. Определить молярную теплоту гидратации сернокислой меди.
6.5 Вычислить тепловой эффект реакции 2N2+6Н2О(ж) = 4NH3+302 при 298К при: а) постоянном давлении; б) постоянном объеме
6.6Теплоты нейтрализации соляной, уксусной и масляной кислот едким натром соответственно равны: -55,9; -56,07; -57,74 кДж/моль. Какова теплота диссоциации уксусной и масляной кислот, если они в водном растворе практически не диссоциируют?
6.7Вычислить тепловой эффект реакции при 298 К: а) при постоянном
давлении, б) при постоянном объеме 2Н2+СО = СН3ОН(ж). Воспользоваться необходимыми данными из справочника.
6.8Теплоты нейтрализации растворов NaОH и NH4OH соляной кислотой соответственно равны -55,9 кДж/моль и -51,34 кДж/моль. Какова теплота диссоциации NH4OH, если он в растворе практически не диссоциирует?
6.9Вычислить тепловой эффект реакции при 298 К, используя справочные данные: а) при постоянном давлении, б) при постоянном объеме
2N2О + 6Н2О = 4NH3 + 4О2
11
6.10 Используя таблицы стандартных величин, рассчитать тепловой эффект
реакции CО2 + Н2 = СО + Н2О(газ), при: а) постоянном давлении, б) постоянном объеме.
6.11 Рассчитать теплоту реакции
NH3 + 5/4О2 = NO + 3/2 Н2O, если
NO = 1/2N2 + 1/2О2 ; ∆Н= -90,37 кДж/моль.
Для водорода ∆Нсгор= -285,85 кДж/моль,
для аммиака ∆Нобр= - 46,19 кДж/моль. |
|
|
6.12 Вычислить стандартную теплоту образования |
C2H5NО2(ж), |
если |
его теплота сгорания при Т=298 К и Р=1,0133·105 Н/м2 |
равна |
|
- 981,852·103Дж/моль. Продукты сгорания СО2(газ), Н2О(ж), N2 .
С(гр)+O2 = СО2(г) -393,795·10 Дж/моль, H2+1/2О2=Н2О(ж) -286,043·10 Дж/моль.
6.13 Рассчитать стандартную теплоту образования CH4N2O(тв), если при Т=298К и Р=1,0133·105 Н/м2 его теплота сгорания ∆Нсг = -634,749·103
Дж/моль. Продукты сгорания: СО2(газ), Н2О(ж), N2 .
Сгр+О2 = СО2(газ) -393,795 ·103 Дж/моль; Н2+1/2O2 = Н2О(ж) -286,043·103 Дж/моль.
6.14 Используя табличные данные, вычислить, тепловой эффект реакции при Т= 298 К и Р= 1,0133·105 Па: а) при постоянном давлении, б) при постоянном объеме. Mg(OH)2 = MgO + Н2О(газ)
6.15 Определить тепловой эффект получения 1 кг акриловой кислоты С2Н2+СО+H2O(ж) = CH2CHCOOH(ж), если стандартная теплота образования СН2СНСООН равна -384,37 кДж/моль. Определите также тепловой эффект этой реакции при постоянном объеме.
6.16Определить тепловой эффект реакции С2Н2+СО+Н2Ож = СН2СНСООНж при стандартном давлении и 298 К, если теплота сгорания акриловой кислоты равна - 1368,03 кДж/моль. Определите также тепловой эффект реакции при постоянном объеме.
6.17Вычислите тепловой эффект реакции при 298 К и постоянном давлении СаС2 + 2Н2О = Са(ОН)2+С2Н2. Для расчета данные возьмите из справочника.
6.18 Вычислить тепловой эффект реакции C2Н2+2H2Ож =CН3СООН +Н2 при 298К: а) при Р = const, б) при V= const. Необходимые данные взять из справочника.
6.19 Вычислить тепловой эффект реакции С2Н6=С2Н4+Н2 при 298 К: 12
а) при P = const, б) при V = const. Необходимые данные взять из справочника.
6.20 Вычислить тепловой эффект реакции S(ромб) + 2Н2Ож = SO2 + 2Н2 при 298 К: а) при P = const б) V = const. Тепловые эффекты образования веществ
при стандартных условиях возьмите из справочника
Задача 7 7.1 Молярная теплота сгорания графита при 290 К равна -394,5 кДж/моль, а
молярная теплота сгорания алмаза -395,4 кДж/моль. Срграф = 0,710, Сралм = 0,505 Дж/(г·К). Рассчитать молярную теплоту перехода графита в алмаз при 700 К.
7.2 Определить энтальпию плавления льда при –10 °С из следующих данных:
Ср(Н2Отв) = 37,6 Дж/(моль·К), Ср(Н2Ож) = 75,3 Дж/(моль·К),
∆Нплав.(Н2О) = 6,3 кДж/моль при 0 °С.
7.3 Теплота затвердевания кристаллогидрата СаС12·6Н2О при 290 0С составляет -170,3 Дж/г, а при 160 °С равна 0. Какова удельная теплоемкость этого соединения в жидком состоянии, если удельная теплоемкость в твердом состоянии составляет 1,443 Дж/(г·К).
7.4 Вычислить теплоту образования 100 г SО3 исходя из реакции 2 SO2 + О2 = 2SО3 при 500К, пользуясь справочными данными.
7.5Теплоты образования FeO, СО и СО2 равны: - 266,5; -110,5; - 393,3 кДж/моль при 298 К и 1 атм. Определить количество тепла, которое выделится при восстановлении 100 кг FeO оксидом углерода СО при 1200 К. При необходимости использовать справочные данные.
7.6Выразить зависимость теплового эффекта реакции от температуры
СН3СОН(газ) + Н2 = С2Н5ОН(газ). Вычислить тепловой эффект реакции при 450 К (воспользоваться таблицами стандартных величин).
7.7 Вычислить тепловой эффект реакции при 600 К при: а) V = const, б) P = const, пользуясь таблицами стандартных величин
4НС1+ О2 = 2Н2О + 2С12.
7.8 Для реакции 4NO + 6Н2О(газ) = 4NН3 + 5О2 выразить зависимость ∆H = f(T). Вычислить тепловой эффект реакции при Т = 500 К и V = const.
7.9Вычислить тепловой эффект реакции 2Н2 + СО = СН3ОН при 1000 К, пользуясь таблицами стандартных величин.
7.10Вычислить тепловой эффект реакции при P = const при 800 К, пользуясь
таблицами стандартных величин. 4NO + 6Н2О(газ) = 4NН3 + 5О2.
13
7.11Вычислить теплоту реакции СН4 + 1/2О2 = СН3ОН(газ) при 500 К, пользуясь таблицами стандартных величин.
7.12Вычислить, пользуясь табличными данными, при 500 К теплоту реакции
3Н2 + SO2 = Н2S + 2Н2О(г).
7.13Вычислить при 900 К теплоту реакции используя табличные данные СН3СНО + Н2 = С2Н5ОН.
7.14Вычислить теплоту реакции при 600 К 2СО2 = 2СО+О2, используя табличные данные.
7.15Вычислить тепловой эффект реакции при 700 К: при а) V = const,
б) P = const, пользуясь таблицами стандартных величин СО + С12 = СОС12(газ).
7.16 |
Вычислить тепловой |
эффект реакции при 700 К при: а) P = const, |
б) V = const, при 700 К, пользуясь таблицами стандартных величин. |
||
Са(ОН)2 = СаО + Н2О(газ). |
|
|
7.17 |
Вычислить тепловой эффект реакции при 800 К при: а) V =сonst, |
|
б) P = const для реакции |
СН3СНО + Н2 = С2Н5ОН. |
|
7.18 Вычислить тепловой эффект реакции C6Н6+ 3Н2 = С6Н12 при 700 К:
а) при P = const, б) при V = const. Необходимые данные взять из справочника.
7.19Вычислить тепловой эффект реакции при 400 К для реакции 2Н2 + СО = СНЗОН(газ).
7.20Выразить зависимость теплового эффекта реакции от Т
СО2 + 4Н2 = СН4 + 2Н2О. Вычислить тепловой эффект реакции при 400 К (воспользоваться таблицами стандартных величин).
Задача 8
8.1Существует ли максимум на кривой зависимости ∆Н=ƒ(Т) для реакции
2С + 2Н2 → С2Н4?
8.2Получить зависимость ∆Н=ƒ(Т) из справочных данных для реакции
Н2 + Cl2 → 2НCl. Определить, проходит ли она через максимум.
8.3 Нарисовать зависимость ∆Н=ƒ(Т), Срнач =ƒ(Т), Сркон =ƒ(Т). Ответ обосновать.
14

8.4 Нарисовать зависимость ∆Ср =ƒ(Т) и ∆Н=ƒ(Т), если:
8.5 Нарисовать зависимость ∆Н=ƒ(Т), ∆Ср =ƒ(Т). Ответ обосновать.
8.6 Используя зависимость Ср =ƒ(Т), определить проходит ли зависимость ∆Н=ƒ(Т) через максимум в интервале от 298 до 1000 К для реакции
2N2 + 6Н2О(газ) → 4NН3 + ЗО2.
8.7 Выразить ∆Ср =ƒ(Т) для реакции СО + 3Н2 → СН4 + Н2О (газ), проанализировать полученное выражение и схематично изобразить зависимость
∆Н=ƒ(Т) в интервале от 100 до 1000 К.
15

8.8 Дана зависимость ∆Н=ƒ(Т). Изобразить зависимость ∆Ср =ƒ(Т) в интервале температур от Т1 до Т2, если СРнач =ƒ(Т), СРкон =ƒ(Т). Ответ обос-
новать.
8.9 Выразить ∆Ср =ƒ(Т) для реакции Н2 + Cl2 → 2НCl.
Существует ли минимум на зависимости ∆Н=ƒ(Т)? Если существует, то при какой температуре?
8.10 Дана зависимость ∆Н=ƒ(Т). Изобразить зависимости СРнач =ƒ(Т), СРкон =ƒ(Т), ∆Ср =ƒ(Т). Ответ обосновать.
8.11Представить схематично ход зависимости ∆Н=ƒ(Т) реакции в интервале температур от 300 до 1000 К. 2Н2 + СО → СН3ОН.
8.12Выразить ∆Ср =ƒ(Т) для реакции 2SО2 + О2 = 2SО3 (газ)
Существует ли минимум на зависимости ∆Н=ƒ(Т)?
8.13 Нарисовать зависимости ∆Н=ƒ(Т), СРнач =ƒ(Т), СРкон =ƒ(Т). Ответ обосновать.
16
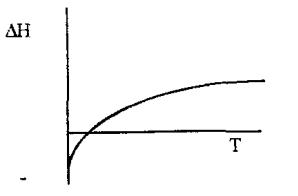
8.14 Дана зависимость ∆Н=ƒ(Т). Построить зависимость СРнач =ƒ(Т), СРкон =ƒ(Т). Ответ обосновать.
8.15Получить зависимость ∆Н=ƒ(Т) из справочных данных для реакции SО2 + Cl2 → SО2Cl2 . Определить проходит ли она через максимум.
8.16Получить зависимость ∆Н=ƒ(Т), из справочных данных для реакции 2СО2 → 2СО + О2. Проходит ли зависимость ∆Н=ƒ(Т) через максимум?
8.17Получить зависимость ∆Н=ƒ(Т), из справочных данных для реакции СО + Cl2 → СОCl2. Проходит ли зависимость ∆Н=ƒ(Т) через максимум?
8.18Получить зависимость ∆Н=ƒ(Т), из справочных данных для реакции С2Н6 → С2Н4 + Н2. Проходит ли зависимость ∆Н=ƒ(Т) через максимум?
8.19Выразить зависимость теплового эффекта реакции от Т для реакции
С2Н5ОН (ж) → С2Н4 + Н2О (ж). Вычислить тепловой эффект реакции при разложении 1кг спирта при 350 °С.
8.20 Получить зависимость ∆Н=ƒ(Т) из справочных данных для реакции
С6Н6 (газ) + 3Н2 → С6Н12 (газ). Проходит ли зависимость ∆Н=ƒ(Т) через максимум?
2. ВТОРОЕ НАЧАЛО ТЕРМОДИНАМИКИ
|
Задача 1 |
|
|
1.1 2 л аргона под давлением |
19,6·104 Н/м2 |
нагревают |
до тех пор, |
пока объем не увеличится |
до 12 л. Каково изменение энтропии, если |
||
Т1 = 373 К? |
|
|
|
1.2 Молярная теплоемкость газообразного метана выражается уравнением
Ср = |
17,518·103 + 60,69 Т Дж/(кмоль·К). |
|
Энтропия |
СН4 при 298 К |
равна 167,73 Дж/(моль·К). Определить |
энтропию 1·10-3 м3 метана при 800 |
оС и Р = 1,01·103 Н/м2. |
|
|
|
17 |
1.31 г льда, взятого при 273 К, прибавлен к 10 г воды, взятой при температуре кипения. Какова конечная температура и чему равно изменение энтропии? Теплота плавления льда равна 334,7 Дж/г, удельная теплоемкость воды равна 4,184 Дж/(г·К).
1.4Определить изменение энтропии при нагревании 1 моль серебра от 298 до 498 К. Необходимые данные взять из справочника.
1.5 |
В |
термически изолированный сосуд, содержащий 1,5 кг воды при 323 |
|||
К вносят 1 кг снега при 264 К. Как возрастет |
энтропия, если ∆Нпл = 334,6 |
||||
Дж/г, |
Сртв.(н2о) = 2,024 |
Дж/(г ·К), |
Срж(н2о) = 4,184 Дж/(г·К). |
||
1.6 |
Найти изменение |
энтропии |
при превращении 100 г воды, взятой при |
||
0 оС |
|
в пар при 120 оС. Удельная теплота |
испарения воды при 100 оС |
||
равна 2,2 кДж/г. Удельная теплоемкость воды равна 4,2 Дж/(г·К). Удельная теплоемкость пара при постоянном давлении равна 1,9 Дж/(г·К).
1.7 Как изменится энтропия С6Н6, если 20 кг его нагреть от 278,7 до 400 К |
||
Тпл = 278,7 К |
Ствр = 1,486 Дж/(г·К) |
|
Тн.т.кип = 353,31 К |
Сжр = 1,842 Дж/(г·К) |
|
∆Нпл = 9,836 кДж/моль |
Сгазр= 1,046 Дж/(г·К) |
|
∆Нисп = 30,77 кДж/моль. |
|
|
1.8 Найти изменение энтропии |
при нагревании 20 |
г КВr от 25 до |
227 оС. Необходимые данные взять из справочника.
1.9 Найти изменение энтропии в процессе затвердевания 1 кг переохлажденного бензола при Т = 268,2 К, если при Т = 278,2 К
∆Нпл = 9,836 кДж/моль, Сртв = 123,6 Дж/(моль·К), Срж = 127,3 Дж/(моль·К).
1.10 200 г Sn с исходной температурой 100 oC и 100 г Н2О с исходной температурой 25 оС погружены вместе в калориметр.
Ср(Sn) = 25,5 Дж/(моль·К), Ср(Н2О) = 75,3 Дж/(моль·К). Найдите: а)
конечную температуру системы, б) изменение энтропии для олова, для Н2О и для Sn и Н2О вместе.
1.11 Вычислить ∆S при смешении 700 м3 СН4 при Т = 268 К |
и 900 м3 С2Н6 |
|
при Т = 288 |
К, если Ро(СН4) = Ро(С2Н6) = Рсмеси = 1,8 · 105 |
Н/м2 , |
Ср (СН4) = |
35,589 Дж/(моль· К), Ср (С2Н6) = 52,756 Дж/(моль· К). |
|
1.12 Найти изменение энтропии при изменении температуры от 280 до 350 К
для 20 кг Вr2, если Ткип = 332,2 К, |
Срж = 0,461 Дж/(г·К), |
|
18 |
∆Нисп = 30,7 кДж/моль, |
Срг = 0,225 Дж/(г·К). |
1.13Вычислить молярную энтропию СО при 598 К и 2 атм., если
Sо298 (СО) = 197,55 Дж/(моль·К).
1.14Найти возрастание энтропии в изохорическом процессе смешения 5 м3
Н2О при 388 К и 6 м3 О2 при 310 К, Рнач = 1 атм.
1.1512 кг кислорода охлаждают от 290 до 233 К, одновременно повышается давление от 1 до 60 атм. Как изменится энтропия?
1.16Рассчитайте изменение энтропии при нагревании 58,82 кг В2О3 от 298 до 700 К. Зависимость молярной теплоемкости от температуры выражается
уравнением Ср = 36, 5525 + 106,345·10-3 Т, Дж/(моль·К).
1.17 280 г азота при 373 К расширяются в вакуум, занимая втрое больший объем. Вычислить изменение энтропии, считая азот идеальным газом.
1.18 Определить изменение энтропии при смешении 1 моль N2 и 2 моль О2, если исходные температуры и давления одинаковы, конечное давление смеси равно исходному давлению, а исходные объемы различны: V(N2) = 1 л, V(02) = 2 л.
1.19 |
Зависимость молярной |
теплоемкости |
газообразного |
аммиака |
от |
|||
температуры выражается уравнением Ср = 29,80 |
+ |
25,48·10-3 Т Дж/(моль·К). |
||||||
S°298 = 99,15 Дж/(моль·К). Определить энтропию |
1·10-3 |
м3 |
аммиака |
при |
||||
500 К и Р = 1,01·105 Н/м2. |
|
|
|
|
|
|
|
|
1.20 |
При 298 К смешали 2 моль О2 и 1 моль N2. Рисх (О2) = Р исx (N2) = Рсмеси |
|||||||
= 1,0133·105 Па. Парциальные давления газов в смеси составляют |
|
|||||||
Р(О2) = 0,668·105, Р(N2) = 0,334·105 Па, соответственно. |
Вычислить ∆G, ∆S |
|||||||
и ∆Н смешения. |
|
|
|
|
|
|
|
|
1.21 Вычислить молярную энтропию СО2 |
при |
598 К |
и |
2 атм., |
|
|||
если |
Sо298 (СО2) = 213,66 Дж/(моль·К). |
|
|
|
|
|
|
|
1.22 |
Рассчитать изменение энтропии при нагревании 1 кг КСl от 298 |
до |
||||||
500 К. Необходимые данные взять из справочника. |
|
|
|
|
||||
|
|
Задача 2 |
|
|
|
|
|
|
2.1 Вычислить ∆S смешения 200 м3 СН4 |
при Т = 298 К |
и 300 м3 Nе при |
||||||
Т = |
283 К, если Р(СН4) = РNe = Рсмеси = 3,1·105 Па, |
|
|
|
|
|||
Ср(СН4) = 35,589 Дж/(моль·К), |
Ср (Ne) = 20,935 Дж/(моль·К). |
|
|
|||||
19
2.2 |
Найти изменение |
энтропии для процесса перехода 20 г газа О2 из |
||||
состояния |
при |
Р = 1,013·105 |
Па и Т = 298 К в |
состояние при |
||
Р = 1,33·102 Па и Т = 250 К. |
|
|
||||
2.3 |
Найти |
возрастание |
энтропии |
при смешении 7 м3 |
He при 275 К и |
|
5 м3 О2 при 350 |
К. Процесс проходит при Р = соnst . |
|
||||
2.4 Определить изменение энтропии при смешении 1 кмоль аргона, взятого при температуре 293 К и давлении 1,01·105 Па, с 2 кмоль азота, взятыми при температуре 323 К и давлении 1,01·105 Па. Рсмеси = 1,01·105 Па. Принять Аr и N2 идеальными газами.
2.5 Найти изменение энтропии для перехода 1 моля газа азота из состояния
(Р = 1,013·105 Па, Т = 298 К) в состояние (Р = 13,3·102 Па, Т = 350 К).
2.6Смешаны 2·10-3 м3 гелия и 2·10-3 м3 аргона при 300 К и Р = 1 атм. После смешения газовая смесь нагрета до 600 К при постоянном объеме. Найти общее возрастание энтропии (теплоемкость рассчитать по классической теории).
2.7Определить изменение энтропии в процессе разделения 2 моль воздуха
при 298 К и давлении 1 атм на чистые азот и кислород. Состав воздуха: 21 моль % О2 и 79 моль % N2.
2.8 Рассчитать изменение энтропии |
в процессе смешения 27 кг воды при |
|
260 К и 20 кг метанола при 298 К. |
|
|
Тпл (Н2О) = 273,2 К; |
Ср(СН3ОНж) = 81,60 Дж/(моль·К); |
|
∆Нпл (Н2О) = 6,138 кДж/моль; |
Ср (Н2Ож) = 4,184 |
Дж/(г·К); |
|
Ср (Н2Отв) = 0,570 |
Дж/(г·К). |
2.9 Найти ∆S при смешении 500 м3 |
Н2О (газ) при Т = 388 К и 600 м3 О2 |
|
при Т = 378 К, если Р(Н2О) = Р(О2) = Робщ = 1,1·105 Н/м2, |
|
|
Ср (Н2О) = 34,572 Дж/(моль ·К), Ср(О2) = 29,309 Дж/(моль· К).
2.10 Рассчитать энтропию С2Н5ОН (газ) при 351,2 К и 0,05 атм.
∆Нисп = 40950 Дж/моль, Т кип = 351,2 К, Sо(С2Н5ОНж) (298,2К) = 160,67
Дж/(моль ·К).
2.11 В термически изолированный сосуд, содержащий 5 кг воды при 303 К, вносят 1 кг снега при 263 К. Как возрастет энтропия, если теплота плавления снега 334,6 Дж/г, теплоемкость жидкой воды 4,184 Дж/(г·К), теплоемкость снега 2,024 Дж/(г·К).
20
