
- •Биохимия животных Электронный дидактический комплекс (эдк)
- •Физическая химия вода
- •Активная реакция водных растворов
- •Ионное произведение воды. Водородный показатель
- •Методы определения рН среды
- •Роль активной реакции среды в биологических процессах
- •Буферные pacтворы, состав, механизм действия
- •Буферная емкость
- •Биологическое значение буферных систем
- •Коллоидная химия
- •Классификация дисперсных систем
- •Поверхностные явления
- •Адсорбция
- •Коллоидные растворы (золи) Методы получения
- •Строение коллоидных частиц
- •Коагуляция. Седиментация. Пептизация
- •Молекулярно-кинетические свойства коллоидных растворов
- •Осмотическое давление
- •Биологическое значение явления осмоса
- •Механизмы, участвующие в сохранении изоосмии:
- •Оптические свойства коллоидных систем
- •Растворы высокомолекулярных соединений
- •Свободная и связанная вода в коллоидных pacтвopax
- •Свойства растворов вмс
- •Денатурация
- •2. Белки; биологическая роль Аминокислоты
- •Содержание белков в организме и тканях
- •Методы выделения белков
- •Методы фракционирования и очистки белков
- •Физико-химические свойства белков
- •Аминокислоты
- •Ациклические аминокислоты
- •Структура белковой молекулы
- •Классификация белков
- •Химия сложных белков
- •3. Нуклеиновые кислоты
- •Нуклеотиды и нуклеозиды
- •Структура днк
- •Рибонуклеиновые кислоты
- •4. Ферменты
- •Биосинтез и клеточная локализация ферментов
- •Химическая природа ферментов
- •Строение ферментов
- •Активный центр фермента
- •Регуляция активности ферментов
- •Механизм действия ферментов
- •Основные свойства ферментов
- •2. Зависимость активности ферментов от рН среды.
- •Факторы, определяющие активность ферментов
- •Активирование и ингибирование ферментов
- •Типы ингибирования
- •Классификация и номенклатура ферментов
- •Применение ферментов.
- •Использование иммобилизованных ферментов для производства биологических соединений
- •Иммуноферментный анализ и его использование в ветеринарии
- •5. Химия витаминов
- •Классификация и номенклатура витаминов
- •I. Жирорастворимые витамины
- •II. Витамины, растворимые в воде
- •Витамин d, антирахитический, кальциферол
- •Витамин e, антистерильный, токоферолы
- •Витамин к, антигеморрагический (филлохинон)
- •Витамин q (убихинон)
- •Водорастворимые витамины
- •Витамин b1, антиневритный, тиамин
- •Витамин b2, рибофлавин
- •Витамин b3, пантотеновая кислота
- •Витамин b5, pp, никотинамид, ниацин, антипеллагрический
- •Витамин b6, адермин, пиридоксол
- •Витамин b12, кобаламин, антианемический
- •Фолиевая кислота
- •Витамин с (аскорбиновая кислота)
- •Биотин, витамин h
- •6. Гормоны
- •Гормоны гипофиза
- •Поджелудочная железа
- •Гормоны щитовидной железы
- •Гормоны надпочечников
- •Гормоны коры надпочечников
- •Гормоны половых желез
- •Гормоны тимуса (вилочковой железы)
- •Гормоны местного действия
- •7. Обмен веществ и энергии
- •Основные этапы обмена веществ
- •Биологическое окисление
- •Окислительное фосфорилирование
- •Токсичность кислорода
- •8. Химия и обмен углеводов
- •Моносахариды
- •Производные моносахаридов.
- •Полисахариды (гликаны)
- •Гетерополисахариды (гетерогликаны)
- •Обмен углеводов
- •Катаболизм глюкозы
- •Гликогенолиз
- •Биосинтез углеводов
- •Биосинтез гликогена (гликогенез)
- •Регуляция углеводного обмена.
- •9. Химия и обмен липидов
- •Химическое строение нейтральных жиров
- •Жирные кислоты.
- •Нейтральные гликолипиды
- •Фосфолипиды (фосфатиды)
- •Сфинголипиды
- •Двойной липидный слой мембран
- •Обмен липидов
- •Переваривание липидов в желудочно-кишечном тракте
- •Промежуточный обмен липидов
- •Энергетический баланс β-окисления жирных кислот
- •Метаболизм ацетил-коэнзима а
- •Пути образования кетоновых тел
- •Биосинтез липидов
- •Метаболизм стеринов и стеридов
- •Липосомы
- •10. Обмен белков
- •Биологическая ценность белков
- •Нормы белка в питании животных
- •Белковые резервы организма
- •Обмен простых белков
- •Переваривание белков в желудочно-кишечном тракте моногастричных животных
- •Переваривание белков в кишечнике.
- •Особенности переваривания белков у жвачных животных
- •Дезаминирование аминокислот
- •Трансаминирование – непрямой путь дезаминирования аминокислот
- •Декарбоксилирование аминокислот
- •Окислительное расщепление аминокислот
- •Особенности обмена отдельных аминокислот
- •11. Биосинтез белка
- •Генетический код
- •Этапы синтеза белка
- •Мультиферментный механизм синтеза белка
- •12.Обмен нуклеиновых кислот Переваривание нуклеиновых кислот в желудочно-кишечном тракте
- •Промежуточный обмен нуклеиновых кислот Распад нуклеиновых кислот в тканях
- •Пиримидиновые основания
- •Биосинтез нуклеиновых кислот
- •Рекомбинантные молекулы и проблемы генной инженерии
- •Клонирование животных
- •Метод молекулярной гибридизации
- •Принцип метода
- •Способы гибридизации
- •Метод блоттинга по Саузерну
- •Полимеразная цепная реакция (пцр)
- •Необходимые приборы и реактивы
- •13. Обмен воды и солей
- •Вода, ее содержание и роль в организме
- •Потребность животного организма в минеральных веществах, их поступление и выделение
- •Микроэлементы
- •14. Биохимия крови
- •Физико-химические свойства крови
- •Буферные системы крови
- •Плазма крови и ее химический состав
- •Белки плазмы и сыворотки крови
- •Небелковые азотистые вещества крови
- •Форменные элементы крови
- •15. Биохимия мышечной ткани
- •Механизм сокращения мышцы
- •Азотистые экстрактивные вещества мышц
- •Минеральные вещества
- •Окоченение мышц
- •16. Биохимия молока и молокообразования
- •17. Биохимия почек и мочи
- •Патологические компоненты мочи
- •Особенности мочи птиц
- •18. Биохимия кожи и шерсти
- •19. Биохимия яйца
- •Биосинтез компонентов яйца
- •Предметный указатель
- •Приложения
- •Рекомендуемая литература
- •Тесты для проверки биохимических
- •Глава 8. Химия обмена углеводов
- •24. Сложноэфирные связи в молекулах триацилглицеролов подвергаются ферментативному гидролизу при участии:
- •Глава 11. Синтез белка
- •Глава 12. Обмен нуклеиновых кислот
- •Глава 13. Биохимия почек и мочи
Генетический код
Второй нуклеотид кодона

Этапы синтеза белка
В процесс синтеза белка включается около 300 типов макромолекул – белков и нуклеиновых кислот, из них около 100 участвуют в активировании аминокислот и переносе их на рибосомы, свыше 60 – в составе рибосом, свыше 10 белковых факторов участвуют в процессах трансляции. Синтез идет в направлении от свободного аминного конца к свободному карбоксильному концу: NH2 → СООН (Рис. 11.2).
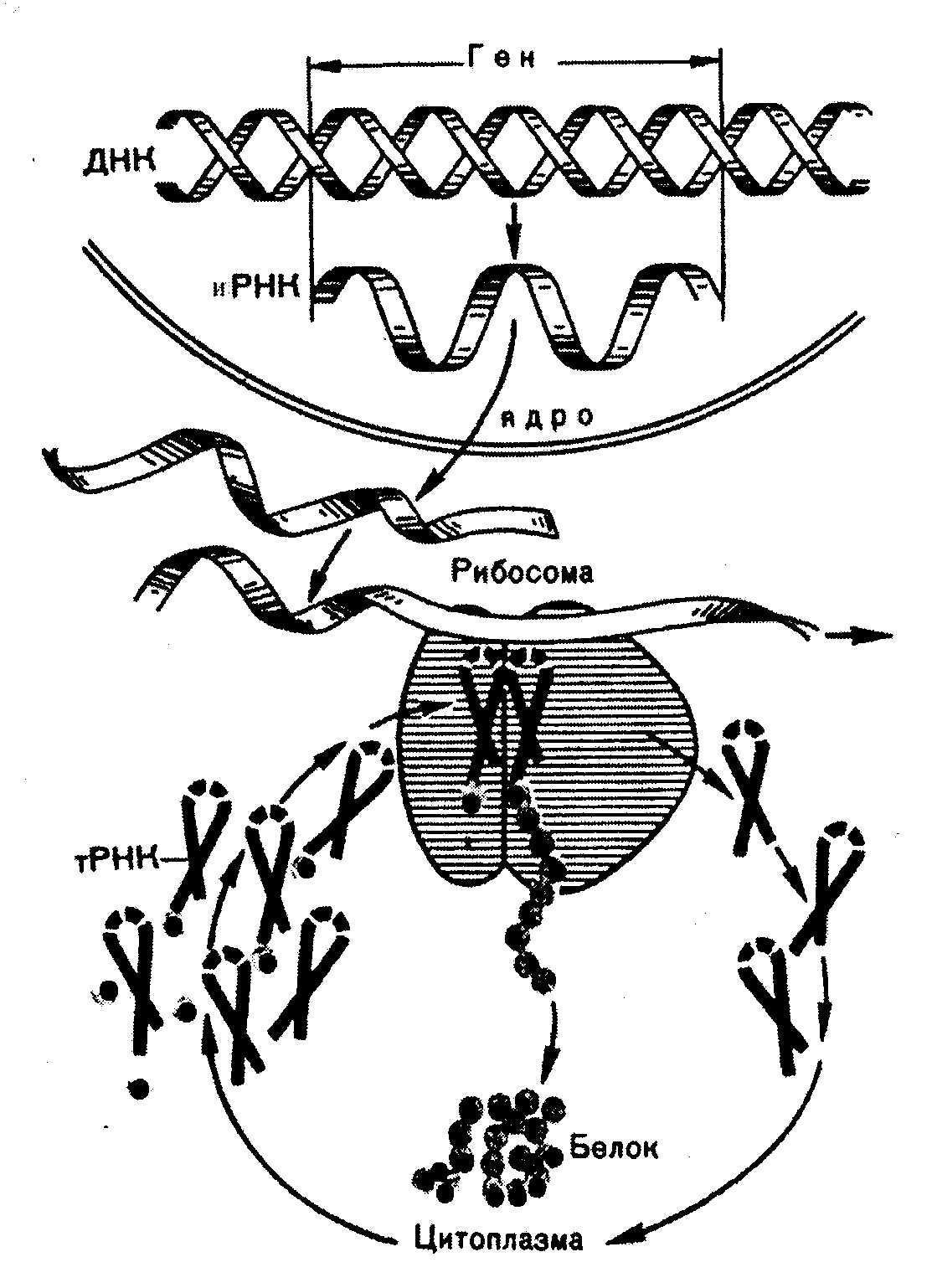
Рис. 11.2. Принципиальная схема биосинтеза белка (по А.С. Спирину).
Активирование аминокислот происходит в цитоплазме при помощи ферментов аминоацил-т-РНК-синтетаз с участием АТФ, в результате образуется аминоацил-т-РНК:

Активированная аминокислота переносится к месту синтеза белка – к полирибосомному комплексу. Следующий этап биосинтеза белка – трансляция – происходит в рибосоме и имеет 3 стадии: инициацию, элонгацию, терминацию.
Инициация трансляции обеспечивается специальными белками, их около 10, начальный участок содержит метионин, то есть начало синтеза обусловлено кодоном формил-метионина (начальный метионин). При этом антикодон (мет-т-РНК) ЦАЦ соединяется с кодоном АУГ и-РНК, образуется инициативный комплекс – к 40 S рибосомной части присоединяется мет-тРНК, затем 60 S субчастица рибосомы(рис.11.3.).
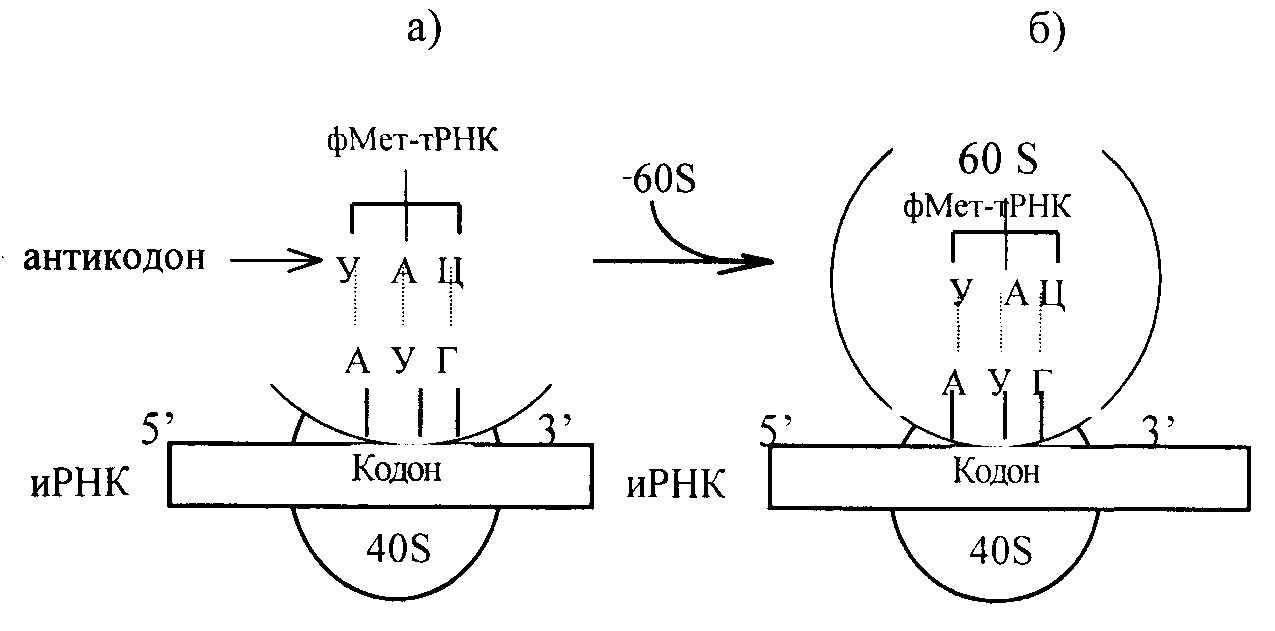
Рис.11.3. Схематическое изображение взаимодействия формилметионил-т-РНК и иРНК с 40S субчастицей рибосомы (а) и транслирующей 80 S рибосомы (б).
После образования комплекса 80 S рибосома + и-РНК, начинается элонгация, то есть удлинение полипептидной цепи. В рибосоме образуется пептидная связь между аминокислотами за счет энергии ГТФ. После присоединения очередной аминокислоты происходит движение рибосомы вдоль цепи и-РНК с 5' к 3' концу на 3 нуклеотида (один ко дон) для каждой аминокислоты.
Терминация трансляции осуществляется с участием трех белковых факторов. Последний терминирующий кодон обуславливает отделение и-РНК от 80S и 80S рибосома распадается на составные субчастицы 60 и 40 S, которые поступают в клеточный пул и используются для образования и-РНК – рибосомного комплекса. Одна и-РНК транслируется не одной рибосомой, а одновременно многими рибосомами (полирибосомы, полисомы), что значительно ускоряет синтез белка (рис. 11.2.).
Постсинтетическая модификация белков происходит в несколько этапов: в начале удаляется сигнальный пептид (из 15-30 аминокислотных остатков) – специфическая протеаза отщепляет начальный N - концевой метионин. Таким образом, отщепляется часть молекулы у проферментов (пепсиноген, проинсулин и т.д.). Затем происходит химическая модификация ферментных белков -ковалентное присоединение простетической группы к молекуле белка, например, присоединение пиридоксальсульфата к белковой части аминотрансфераз; гликозилирование – присоединение олигосахаридных остатков в гликопротеинах; гидроксилирование пролина, лизина, метилирование лизина и глутамата, ацетилирование N-концевых аминокислот, фосфорилирование серина, треонина, тирозина и т.д. Укладка белковой молекулы -образование вторичной, третичной и четвертичной структур так же происходит после синтеза – образования первичной структуры белковой молекулы.
