
- •Биохимия животных Электронный дидактический комплекс (эдк)
- •Физическая химия вода
- •Активная реакция водных растворов
- •Ионное произведение воды. Водородный показатель
- •Методы определения рН среды
- •Роль активной реакции среды в биологических процессах
- •Буферные pacтворы, состав, механизм действия
- •Буферная емкость
- •Биологическое значение буферных систем
- •Коллоидная химия
- •Классификация дисперсных систем
- •Поверхностные явления
- •Адсорбция
- •Коллоидные растворы (золи) Методы получения
- •Строение коллоидных частиц
- •Коагуляция. Седиментация. Пептизация
- •Молекулярно-кинетические свойства коллоидных растворов
- •Осмотическое давление
- •Биологическое значение явления осмоса
- •Механизмы, участвующие в сохранении изоосмии:
- •Оптические свойства коллоидных систем
- •Растворы высокомолекулярных соединений
- •Свободная и связанная вода в коллоидных pacтвopax
- •Свойства растворов вмс
- •Денатурация
- •2. Белки; биологическая роль Аминокислоты
- •Содержание белков в организме и тканях
- •Методы выделения белков
- •Методы фракционирования и очистки белков
- •Физико-химические свойства белков
- •Аминокислоты
- •Ациклические аминокислоты
- •Структура белковой молекулы
- •Классификация белков
- •Химия сложных белков
- •3. Нуклеиновые кислоты
- •Нуклеотиды и нуклеозиды
- •Структура днк
- •Рибонуклеиновые кислоты
- •4. Ферменты
- •Биосинтез и клеточная локализация ферментов
- •Химическая природа ферментов
- •Строение ферментов
- •Активный центр фермента
- •Регуляция активности ферментов
- •Механизм действия ферментов
- •Основные свойства ферментов
- •2. Зависимость активности ферментов от рН среды.
- •Факторы, определяющие активность ферментов
- •Активирование и ингибирование ферментов
- •Типы ингибирования
- •Классификация и номенклатура ферментов
- •Применение ферментов.
- •Использование иммобилизованных ферментов для производства биологических соединений
- •Иммуноферментный анализ и его использование в ветеринарии
- •5. Химия витаминов
- •Классификация и номенклатура витаминов
- •I. Жирорастворимые витамины
- •II. Витамины, растворимые в воде
- •Витамин d, антирахитический, кальциферол
- •Витамин e, антистерильный, токоферолы
- •Витамин к, антигеморрагический (филлохинон)
- •Витамин q (убихинон)
- •Водорастворимые витамины
- •Витамин b1, антиневритный, тиамин
- •Витамин b2, рибофлавин
- •Витамин b3, пантотеновая кислота
- •Витамин b5, pp, никотинамид, ниацин, антипеллагрический
- •Витамин b6, адермин, пиридоксол
- •Витамин b12, кобаламин, антианемический
- •Фолиевая кислота
- •Витамин с (аскорбиновая кислота)
- •Биотин, витамин h
- •6. Гормоны
- •Гормоны гипофиза
- •Поджелудочная железа
- •Гормоны щитовидной железы
- •Гормоны надпочечников
- •Гормоны коры надпочечников
- •Гормоны половых желез
- •Гормоны тимуса (вилочковой железы)
- •Гормоны местного действия
- •7. Обмен веществ и энергии
- •Основные этапы обмена веществ
- •Биологическое окисление
- •Окислительное фосфорилирование
- •Токсичность кислорода
- •8. Химия и обмен углеводов
- •Моносахариды
- •Производные моносахаридов.
- •Полисахариды (гликаны)
- •Гетерополисахариды (гетерогликаны)
- •Обмен углеводов
- •Катаболизм глюкозы
- •Гликогенолиз
- •Биосинтез углеводов
- •Биосинтез гликогена (гликогенез)
- •Регуляция углеводного обмена.
- •9. Химия и обмен липидов
- •Химическое строение нейтральных жиров
- •Жирные кислоты.
- •Нейтральные гликолипиды
- •Фосфолипиды (фосфатиды)
- •Сфинголипиды
- •Двойной липидный слой мембран
- •Обмен липидов
- •Переваривание липидов в желудочно-кишечном тракте
- •Промежуточный обмен липидов
- •Энергетический баланс β-окисления жирных кислот
- •Метаболизм ацетил-коэнзима а
- •Пути образования кетоновых тел
- •Биосинтез липидов
- •Метаболизм стеринов и стеридов
- •Липосомы
- •10. Обмен белков
- •Биологическая ценность белков
- •Нормы белка в питании животных
- •Белковые резервы организма
- •Обмен простых белков
- •Переваривание белков в желудочно-кишечном тракте моногастричных животных
- •Переваривание белков в кишечнике.
- •Особенности переваривания белков у жвачных животных
- •Дезаминирование аминокислот
- •Трансаминирование – непрямой путь дезаминирования аминокислот
- •Декарбоксилирование аминокислот
- •Окислительное расщепление аминокислот
- •Особенности обмена отдельных аминокислот
- •11. Биосинтез белка
- •Генетический код
- •Этапы синтеза белка
- •Мультиферментный механизм синтеза белка
- •12.Обмен нуклеиновых кислот Переваривание нуклеиновых кислот в желудочно-кишечном тракте
- •Промежуточный обмен нуклеиновых кислот Распад нуклеиновых кислот в тканях
- •Пиримидиновые основания
- •Биосинтез нуклеиновых кислот
- •Рекомбинантные молекулы и проблемы генной инженерии
- •Клонирование животных
- •Метод молекулярной гибридизации
- •Принцип метода
- •Способы гибридизации
- •Метод блоттинга по Саузерну
- •Полимеразная цепная реакция (пцр)
- •Необходимые приборы и реактивы
- •13. Обмен воды и солей
- •Вода, ее содержание и роль в организме
- •Потребность животного организма в минеральных веществах, их поступление и выделение
- •Микроэлементы
- •14. Биохимия крови
- •Физико-химические свойства крови
- •Буферные системы крови
- •Плазма крови и ее химический состав
- •Белки плазмы и сыворотки крови
- •Небелковые азотистые вещества крови
- •Форменные элементы крови
- •15. Биохимия мышечной ткани
- •Механизм сокращения мышцы
- •Азотистые экстрактивные вещества мышц
- •Минеральные вещества
- •Окоченение мышц
- •16. Биохимия молока и молокообразования
- •17. Биохимия почек и мочи
- •Патологические компоненты мочи
- •Особенности мочи птиц
- •18. Биохимия кожи и шерсти
- •19. Биохимия яйца
- •Биосинтез компонентов яйца
- •Предметный указатель
- •Приложения
- •Рекомендуемая литература
- •Тесты для проверки биохимических
- •Глава 8. Химия обмена углеводов
- •24. Сложноэфирные связи в молекулах триацилглицеролов подвергаются ферментативному гидролизу при участии:
- •Глава 11. Синтез белка
- •Глава 12. Обмен нуклеиновых кислот
- •Глава 13. Биохимия почек и мочи
Классификация и номенклатура ферментов
Рациональная номенклатура ферментов составляется путем прибавления к латинскому корню названия субстрата, на который действует фермент, или к названию процесса, катализируемого ферментом, окончания "аза".
Например, фермент, воздействующий на крахмал (amylum), называется амилаза; мочевину (urea) – уреаза; фенолы – фенолаза и т.д.
Кроме рационального названия сохранились ранее появившиеся термины: пепсин, трипсин.
В 1961 г. принята новая международная классификация, в основу которой принят тип катализируемой реакции.
В настоящее время известно около 3000 различных ферментов. Классификацию их проводят по типу их действия. Различают 6 классов ферментов:
1 .Оксидоредуктазы – окислительно-восстановительные
ферменты; катализируют биологическое окисление.
2.Трансферазы – катализируют реакции переноса различных химических групп от одной молекулы (донора) к другой молекуле (акцептору).
3. Гидролазы – осуществляют химические превращения веществ с участием молекулы воды.
4. Лиазы – отщепляют от субстратов ту или иную группу негидролитическим путем.
5. Изомеразы – осуществляют изомерные превращения соединений.
6. Лигазы (синтетазы) – катализируют реакции синтеза, сопровождающиеся отщеплением фосфорной кислоты от АТФ или другого трифосфата.
I класс. Оксидоредуктазы – это ферменты окислительно-восстановительных реакций, лежащих в основе биологического окисления. Название ферментов составляется по следующей форме: название субстрата (донора), от которого отщепляются атомы водорода (электроны), название акцептора, на который переносятся атомы водорода и оканчивается названием "оксидоредуктаза": например, лактат: НАД-оксидоредуктаза.
Различают следующие подклассы:
1) аэробные дегидрогеназы, которые переносят электроны и протоны водорода с окисляемого субстрата на кислород:
H2S
+ O2
![]() S
окисленная + H2O2
S
окисленная + H2O2
сероводород
к ним относятся ферменты оксидазы;
2) анаэробные дегидрогеназы переносят электроны и протоны водорода с окисляемого на другой субстрат. К ним относятся пиридинзависимые и флавинзависимые дегидрогеназы. Например, окисление молочной кислоты происходит под действием лактатдегидрогеназы, при этом НАД восстанавливается в НАДН2:
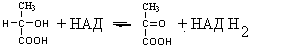
молочная кислота пировиноградная кислота
Окисление янтарной кислоты происходит под действием сукцинатдегидоогеназы, при этом ФАД восстанавливается в ФАДН2.
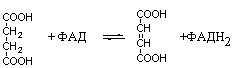
янтарная кислота фумаровая кислота
3) электронтранспортазы – переносчики электронов. К ним относятся цитохромные ферменты, цитохромоксидазы дыхательной цепи митохондрий
4) пероксидаза и каталаза. Пероксидаза катализирует окисление субстрата перекисью водорода. Например, под действием пероксидазы сероводород окисляется с участием перекиси водорода:
H
 2
S
+ H2O2
S
окисленная
+
2H2O
2
S
+ H2O2
S
окисленная
+
2H2O
Каталаза в организме животных разрушает перекись водорода на воду и молекулярный кислород:
2
 H2O2
2H2O
+ O2
H2O2
2H2O
+ O2
Каталаза обезвреживает действие перекиси и является источником молекулярного кислорода в тканях.
II класс. Трансферазы – катализируют реакции переноса атомов и групп атомов, включают следующие подклассы:
1) Аминоферазы – ферменты, переносящие аминогруппы с одного вещества на другое. Коферментом является производное витамина B6 (пиридоксин): например, глутаминовая кислота отдает аминную группу на пируват, в результате синтезируется аланин и образуется а-кетоглутаровая кислота.
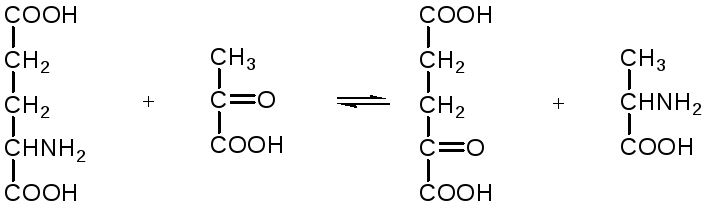
глутаминовая пируват α - кетоглутаровая аланин
кислота кислота
Пиридоксин – фермент, осуществляющий эту реакцию, называется 1-глутамил:пируватаминотрансфераза или по старой номенклатуре – аминофераза.
2) Ацилтрансферазы – ускоряют перенос ацилов (остатков карбоновых кислот) на аминокислоты, спирты и другие соединения. Например, синтез ацетилхолина осуществляется с участием фермента холинацетилтрансферазы:
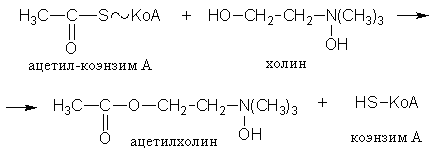
3) Фосфотрансферазы – ферменты, ускоряющие реакцию переноса остатка фосфорной кислоты. Донором фосфатных остатков чаще всего является АТФ. Например, гексокиназа ускоряет перенос остатка фосфорной кислоты на глюкозу:
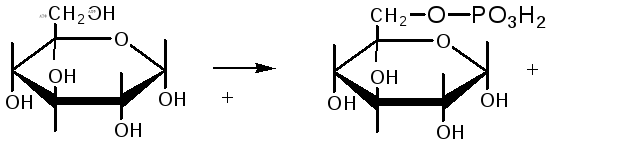
α-D -глюкоза глюкозо-6-фосфат
4) Метилферазы - ферменты, переносящие метильную группу с одного соединения на другое: например, при синтезе креатина донором метильной группы является метионин.
5) Глюкозилтрансферазы - переносчики глюкозидных
остатков:
1 1(C6H12O6)
+ УДФ - глюкоза (n+1)
(C6H12O6)
+ УДФ
1(C6H12O6)
+ УДФ - глюкоза (n+1)
(C6H12O6)
+ УДФ
к ним относятся гликогенсинтазы, глюкозилтрансферазы, фосфорибозилтрансферазы и т.д.
6) Алкилтрансферазы – переносчики спиртовых остатков. К ним относятся холинтрансфераза, фосфатилдиэтаноламин-трансфераза и др.
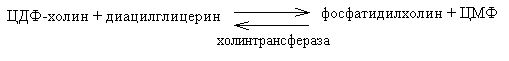
III класс. Гидролазы - разрывают внутримолекулярные связи путем присоединения элементов воды:
R - R1
+ HOH
R
- H
+ R1
- ОН
- R1
+ HOH
R
- H
+ R1
- ОН
К ним относятся следующие подклассы:
1) Эстеразы - ферменты, гидролизирующие эфирные связи по схеме:
R 1-0-R2+
HOH
R1-H+
R2-OH
1-0-R2+
HOH
R1-H+
R2-OH
Например, фосфодиэстеразы - гидролизуют фосфорные эфиры:
Д иацилглицерин
3-фосфорная кислота +HOH
диацилглицерин + H3PO4.
иацилглицерин
3-фосфорная кислота +HOH
диацилглицерин + H3PO4.
К этому подклассу относятся: фосфатазы (кислая, щелочная), глюкозо-6-глюкозо-1-фосфатаза, РНК-аза и др.
Карбоксиэстеразы – гидролизуют сложные эфирные связи:
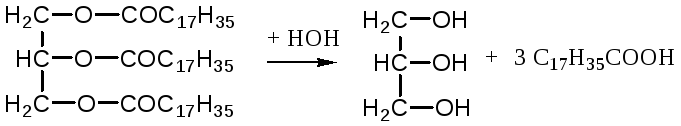
тристеарин глицерин стеариновая
кислота
К этим ферментам относятся липазы, лецитиназы, простые эстеразы и т.д.
Сульфоэстеразы – гидролизуют сернокислые эфиры по следующей схеме:
![]()
фенолсерная кислота фенол серная кислота
2) Гликозидазы – гидролизуют гликозидные связи, к ним относятся α- и β-амилазы, мальтаза, лактаза, сахараза.
3) Пептидазы. Различают эндопептидазы – пепсин, трипсин, хемотрипсин; экзопептидазы – аминопептидаза, карбоксипептидаза, дипептидазы, трипептидазы.
Пептидазы гидролизуют пептидные связи по следующей реакции:
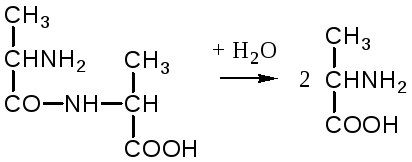
аланилаланин аланин
В результате гидролиза образуется две молекулы аланина.
4) Амидазы – ферменты, гидролизующие амидные связи пуриновых и пиримидиновых оснований, амидов аминокислот и
аргинина. Примеры:
а )
Аденин +H2O
гипоксантин + NH3
)
Аденин +H2O
гипоксантин + NH3
пуриндезаминаза
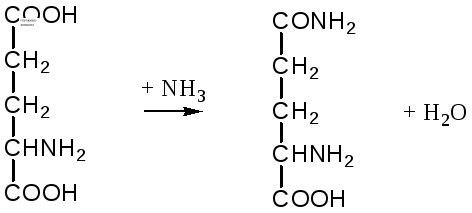
глутаминовая глутамин
кислота
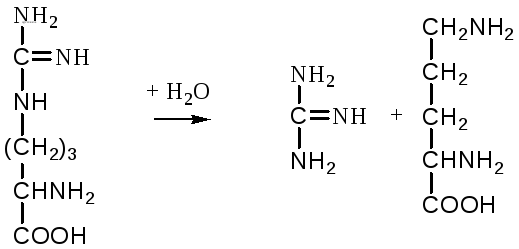
аргинин мочевина орнитин
5) Полифосфатазы - гидролизуют фосфорноангидридные связи:
АТФаза
А ТФ
+H2O
АДФ + H3PO4
ТФ
+H2O
АДФ + H3PO4
К этой группе относятся Na+, K+, Mg2+-ATФaзa, и др.
IV класс. Лиазы – ферменты, расщепляющие связи без Участия воды, разрывая при этом C-C связи, C-N связи, C-O связи. К ним относятся ферменты альдолаза, декарбоксилаза и другие. Например, альдолаза разрывает C-C связи гексозы (1,6 -дифосфофруктозы) с образованием двух триоз, фосфодиоксиацетона и фосфоглицеринового альдегида:
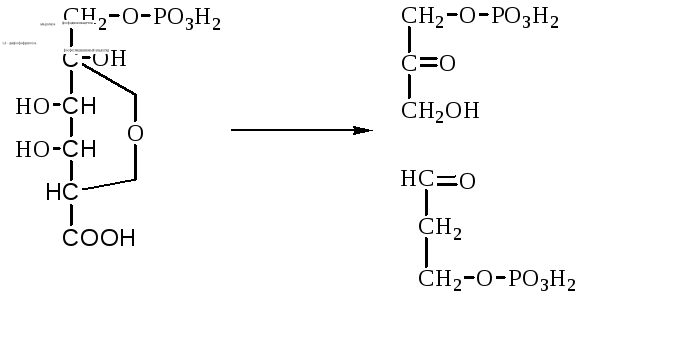
V класс. Изомеразы: катализируют изомеризацию, изомерные превращения молекул, например, молекулы глюкозы во фруктозу. Мутазы изменяют местоположение различных групп или атомов в молекуле. К ним относятся: фосфоглицеромутаза, фосфоглюкомутаза, фосфофруктомутаза и т.д. Например, фосфодиоксиацетон под действием изомеразы превращается в фосфоглицериновый альдегид:
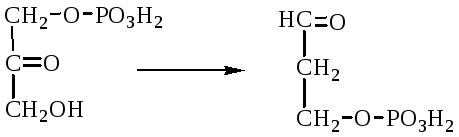
фосфодиоксиацетон фосфоглицериновый альдегид
VI класс. Лигазы (синтетазы) – ферменты, катализирующие присоединение молекул друг к другу. Например:
а минокислота
+ тРНК аминоацил-тРНК
минокислота
+ тРНК аминоацил-тРНК
Сюда относятся ферменты: ДНК-полимеразы, РНК-полимеразы, ферменты, катализирующие синтез белков и т.д.
