
- •Биохимия животных Электронный дидактический комплекс (эдк)
- •Физическая химия вода
- •Активная реакция водных растворов
- •Ионное произведение воды. Водородный показатель
- •Методы определения рН среды
- •Роль активной реакции среды в биологических процессах
- •Буферные pacтворы, состав, механизм действия
- •Буферная емкость
- •Биологическое значение буферных систем
- •Коллоидная химия
- •Классификация дисперсных систем
- •Поверхностные явления
- •Адсорбция
- •Коллоидные растворы (золи) Методы получения
- •Строение коллоидных частиц
- •Коагуляция. Седиментация. Пептизация
- •Молекулярно-кинетические свойства коллоидных растворов
- •Осмотическое давление
- •Биологическое значение явления осмоса
- •Механизмы, участвующие в сохранении изоосмии:
- •Оптические свойства коллоидных систем
- •Растворы высокомолекулярных соединений
- •Свободная и связанная вода в коллоидных pacтвopax
- •Свойства растворов вмс
- •Денатурация
- •2. Белки; биологическая роль Аминокислоты
- •Содержание белков в организме и тканях
- •Методы выделения белков
- •Методы фракционирования и очистки белков
- •Физико-химические свойства белков
- •Аминокислоты
- •Ациклические аминокислоты
- •Структура белковой молекулы
- •Классификация белков
- •Химия сложных белков
- •3. Нуклеиновые кислоты
- •Нуклеотиды и нуклеозиды
- •Структура днк
- •Рибонуклеиновые кислоты
- •4. Ферменты
- •Биосинтез и клеточная локализация ферментов
- •Химическая природа ферментов
- •Строение ферментов
- •Активный центр фермента
- •Регуляция активности ферментов
- •Механизм действия ферментов
- •Основные свойства ферментов
- •2. Зависимость активности ферментов от рН среды.
- •Факторы, определяющие активность ферментов
- •Активирование и ингибирование ферментов
- •Типы ингибирования
- •Классификация и номенклатура ферментов
- •Применение ферментов.
- •Использование иммобилизованных ферментов для производства биологических соединений
- •Иммуноферментный анализ и его использование в ветеринарии
- •5. Химия витаминов
- •Классификация и номенклатура витаминов
- •I. Жирорастворимые витамины
- •II. Витамины, растворимые в воде
- •Витамин d, антирахитический, кальциферол
- •Витамин e, антистерильный, токоферолы
- •Витамин к, антигеморрагический (филлохинон)
- •Витамин q (убихинон)
- •Водорастворимые витамины
- •Витамин b1, антиневритный, тиамин
- •Витамин b2, рибофлавин
- •Витамин b3, пантотеновая кислота
- •Витамин b5, pp, никотинамид, ниацин, антипеллагрический
- •Витамин b6, адермин, пиридоксол
- •Витамин b12, кобаламин, антианемический
- •Фолиевая кислота
- •Витамин с (аскорбиновая кислота)
- •Биотин, витамин h
- •6. Гормоны
- •Гормоны гипофиза
- •Поджелудочная железа
- •Гормоны щитовидной железы
- •Гормоны надпочечников
- •Гормоны коры надпочечников
- •Гормоны половых желез
- •Гормоны тимуса (вилочковой железы)
- •Гормоны местного действия
- •7. Обмен веществ и энергии
- •Основные этапы обмена веществ
- •Биологическое окисление
- •Окислительное фосфорилирование
- •Токсичность кислорода
- •8. Химия и обмен углеводов
- •Моносахариды
- •Производные моносахаридов.
- •Полисахариды (гликаны)
- •Гетерополисахариды (гетерогликаны)
- •Обмен углеводов
- •Катаболизм глюкозы
- •Гликогенолиз
- •Биосинтез углеводов
- •Биосинтез гликогена (гликогенез)
- •Регуляция углеводного обмена.
- •9. Химия и обмен липидов
- •Химическое строение нейтральных жиров
- •Жирные кислоты.
- •Нейтральные гликолипиды
- •Фосфолипиды (фосфатиды)
- •Сфинголипиды
- •Двойной липидный слой мембран
- •Обмен липидов
- •Переваривание липидов в желудочно-кишечном тракте
- •Промежуточный обмен липидов
- •Энергетический баланс β-окисления жирных кислот
- •Метаболизм ацетил-коэнзима а
- •Пути образования кетоновых тел
- •Биосинтез липидов
- •Метаболизм стеринов и стеридов
- •Липосомы
- •10. Обмен белков
- •Биологическая ценность белков
- •Нормы белка в питании животных
- •Белковые резервы организма
- •Обмен простых белков
- •Переваривание белков в желудочно-кишечном тракте моногастричных животных
- •Переваривание белков в кишечнике.
- •Особенности переваривания белков у жвачных животных
- •Дезаминирование аминокислот
- •Трансаминирование – непрямой путь дезаминирования аминокислот
- •Декарбоксилирование аминокислот
- •Окислительное расщепление аминокислот
- •Особенности обмена отдельных аминокислот
- •11. Биосинтез белка
- •Генетический код
- •Этапы синтеза белка
- •Мультиферментный механизм синтеза белка
- •12.Обмен нуклеиновых кислот Переваривание нуклеиновых кислот в желудочно-кишечном тракте
- •Промежуточный обмен нуклеиновых кислот Распад нуклеиновых кислот в тканях
- •Пиримидиновые основания
- •Биосинтез нуклеиновых кислот
- •Рекомбинантные молекулы и проблемы генной инженерии
- •Клонирование животных
- •Метод молекулярной гибридизации
- •Принцип метода
- •Способы гибридизации
- •Метод блоттинга по Саузерну
- •Полимеразная цепная реакция (пцр)
- •Необходимые приборы и реактивы
- •13. Обмен воды и солей
- •Вода, ее содержание и роль в организме
- •Потребность животного организма в минеральных веществах, их поступление и выделение
- •Микроэлементы
- •14. Биохимия крови
- •Физико-химические свойства крови
- •Буферные системы крови
- •Плазма крови и ее химический состав
- •Белки плазмы и сыворотки крови
- •Небелковые азотистые вещества крови
- •Форменные элементы крови
- •15. Биохимия мышечной ткани
- •Механизм сокращения мышцы
- •Азотистые экстрактивные вещества мышц
- •Минеральные вещества
- •Окоченение мышц
- •16. Биохимия молока и молокообразования
- •17. Биохимия почек и мочи
- •Патологические компоненты мочи
- •Особенности мочи птиц
- •18. Биохимия кожи и шерсти
- •19. Биохимия яйца
- •Биосинтез компонентов яйца
- •Предметный указатель
- •Приложения
- •Рекомендуемая литература
- •Тесты для проверки биохимических
- •Глава 8. Химия обмена углеводов
- •24. Сложноэфирные связи в молекулах триацилглицеролов подвергаются ферментативному гидролизу при участии:
- •Глава 11. Синтез белка
- •Глава 12. Обмен нуклеиновых кислот
- •Глава 13. Биохимия почек и мочи
Переваривание белков в кишечнике.
Высокомолекулярные полипептиды, образовавшиеся в желудке под действием пепсина, и нативные белки в двенадцатиперстной кишке подвергаются действию ферментов поджелудочной железы – трипсина, химотрипсина, карбоксипептидазы, аминопептидазы.
Трипсин – выделяется в виде трипсиногена. Трипсиноген под действием энтеропептидазы (открыт в лаборатории Павлова И.П.) превращается в активную форму – трипсин, при этом освобождается активный центр фермента. М.м. 26700, трипсин активен при рН 7,8-8,2. Он расщепляет примерно 1/3 пептидных связей в молекуле белка. Продукты гидролиза – низкомолекулярные полипептиды, дипептиды, свободные аминокислоты.
Химотрипсин – М.м. 25000, оптимум рН 7,2-8,0; выделяется в виде профермента химотрипсиногена,который превращается в химотрипсин многоступенчато (α, β, γ, δ и т.д.). Он гидролизует белки и высокомолекулярные пептиды, так же как и трипсин, но более глубоко. При этом гидролизуются до 50 % пептидных связей. Легче разрываются связи карбоксильных групп тирозина, фенилаланина, триптофана и метионина. Низкомолекулярные пептиды расщепляются под действием пептидаз. Карбоксипептидаза расщепляет полипептиды с конца цепи со свободной карбоксильной группой, а аминопептидазы – со свободного N- конца. Ди- и трипептидазы вырабатываются в клетках кишечной стенки и гидролиз пептидных связей под действием этих ферментов происходит или непосредственно у кишечной стенки или же в клетках кишечной стенки, поэтому этот процесс называют пристеночным перевариванием.
Фермент коллагеназа гидролизует коллагены костной ткани, эластаза – эластины связок. Распад белков идет до образования аминокислот, которые затем всасываются с участием переносчиков, то есть всасывание аминокислот – активный процесс.
Биохимические процессы в толстом отделе кишечника
Толстый отдел кишечника (слепая, ободочная кишки и др.) представляют важный участок желудочно-кишечного тракта, в его соке содержатся карбонаты, создаются условия для микробиологических процессов. Клетчатка и другие углевод подвергаются бактериальному гидролизу и сбраживанию, а белки и аминокислоты - гниению, что приводит к образованию различных ядовитых для организма продуктов.
У лошадей, кроликов и других травоядных животных преобладают различные виды брожения. У свиней, собак, кошек – процессы гниения. В толстом отделе кишечника микроорганизмами синтезируются водорастворимые витамины (B1, B2, B3, B5, Вб, B12 и т.д.).
Одним из путей превращения аминокислот является их декарбоксилирование, которое сопровождается выделением CO2 и образованием аминов и диаминов. Реакция происходит под действием фермента декарбоксилазы.
Тирозин декарбоксилируется с образованием тирамина, орнитин – путресцина, лизин – кадаверина, гистидин – гистамина.
Из тирозина образуются крезол, фенол, из триптофана – скатол, индол; все они имеют неприятный запах.
Фенол, крезол, скатоксил, индоксил обезвреживаются в результате взаимодействия этих веществ с "активной" формой серной кислоты (З-фосфоаденозин-5-фосфосульфат, ФАФС).
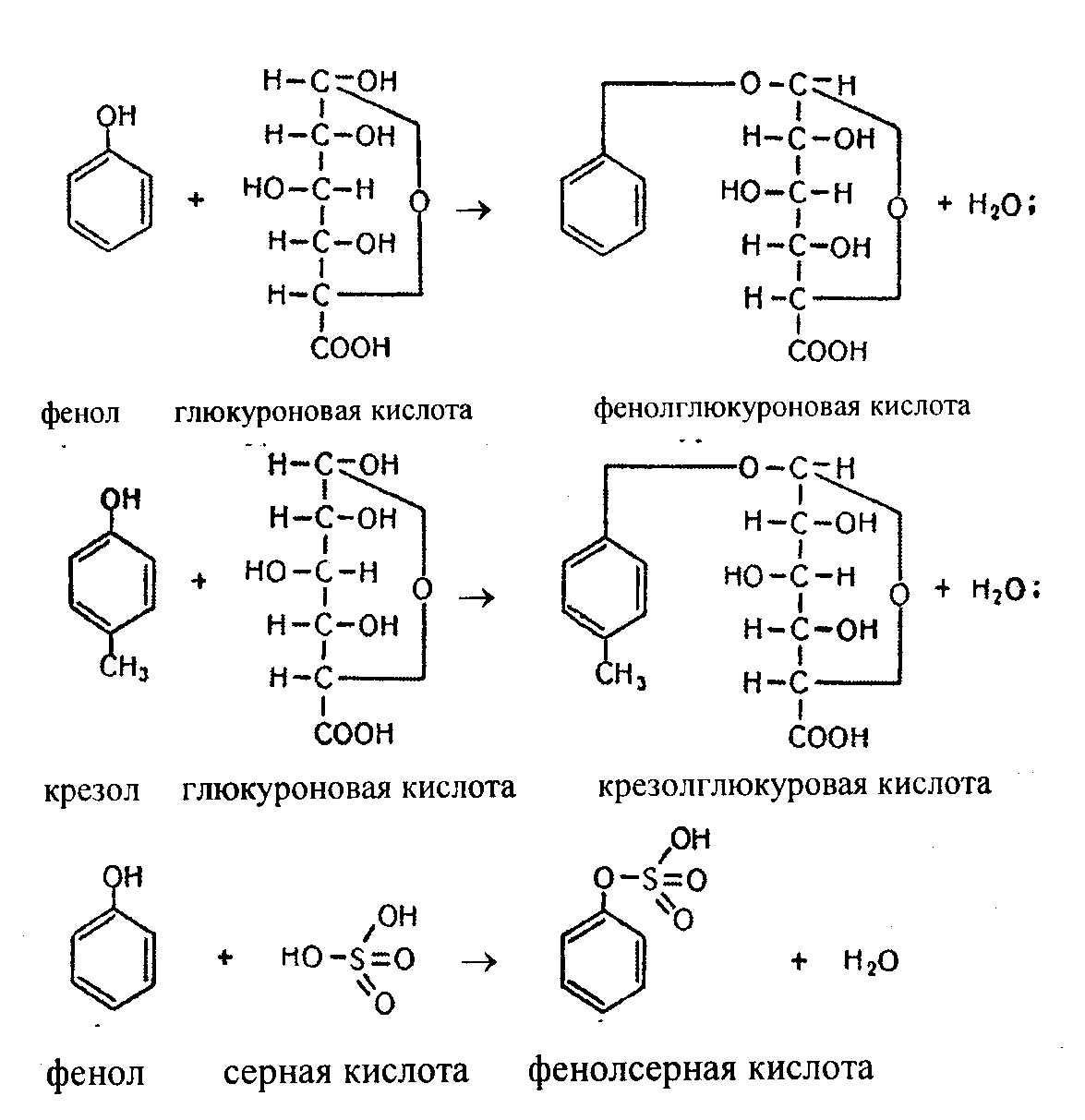
Кроме того, эти вещества обезвреживаются при связывании их с глюкуроновой кислотой, образуя при этом парные соединения. Реакция катализируется ферментом УДФ-глюкуронил-
трансферазой (УДФ-ГК). Ниже представлены химическое строение ФАФС и УДФГК.


Они всасываются из кишечника в кровь и выделяются с мочой. Путресцин и кадаверин называют трупными ядами, так как они образуются при разложении трупов.
Образующиеся в кишечнике амины и диамины обладают сильным действием на сосуды и, как следствие, – на кровяное давление (тирамин, гистамин). Сероводород (H2S), метилмеркаптан (CH3SH) и другие серосодержащие соединения образуются из цистеина, метионина.
Под влиянием ферментов гнилостных бактерий происходит окисление аминокислот и образуются ядовитые продукты распада фенилаланина, тирозина, триптофана.
В результате образуются фенолсерная кислота, крезолсерная кислота, фенолглюкуроновая, крезолглюкуроновая кислоты. Индол (как и скатол) предварительно подвергается окислению в индоксил (соответственно скатоксил), который взаимодействует непосредственно в ферментативной реакции с ФАФС или УДФГК. Так, индоксил образует эфиры серной кислоты, затем калиевую соль, которая выделяется с мочой (животный индикан):
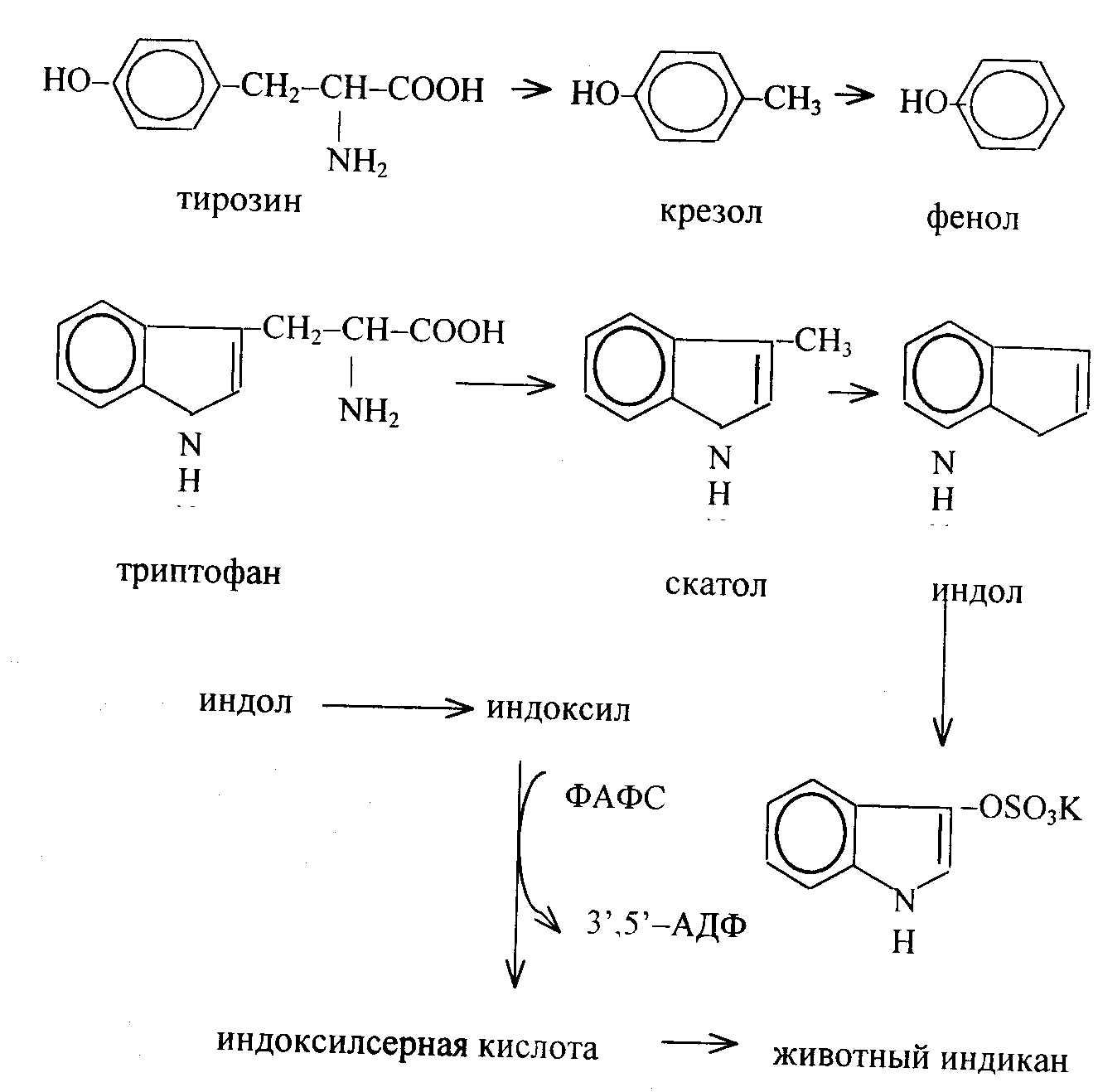
Индол и скатол обезвреживаются преимущественно путем синтеза сульфопроизводных, а количество индикана в моче является постоянной величиной у здоровых животных. Увеличение индикана в моче наблюдается при воспалении мышц, обширных травмах и при избытке триптофана в рационе животных.
Избыточное содержание фенилаланина в рационе, или ее недоступность ферментам тонкого отдела кишечника, приводит к тому, что фенилаланин окисляется бактериальными ферментами в толстом отделе кишечника и превращается в бензойную кислоту. У млекопитающих бензойная кислота обезвреживается в печени и почках путем взаимодействия с глицином, в результате образуется гиппуровая кислота. У птиц обезвреживание бензойной кислоты происходит в реакции с орнитином, в результате образуется орнитуровая кислота.
