
- •Биохимия животных Электронный дидактический комплекс (эдк)
- •Физическая химия вода
- •Активная реакция водных растворов
- •Ионное произведение воды. Водородный показатель
- •Методы определения рН среды
- •Роль активной реакции среды в биологических процессах
- •Буферные pacтворы, состав, механизм действия
- •Буферная емкость
- •Биологическое значение буферных систем
- •Коллоидная химия
- •Классификация дисперсных систем
- •Поверхностные явления
- •Адсорбция
- •Коллоидные растворы (золи) Методы получения
- •Строение коллоидных частиц
- •Коагуляция. Седиментация. Пептизация
- •Молекулярно-кинетические свойства коллоидных растворов
- •Осмотическое давление
- •Биологическое значение явления осмоса
- •Механизмы, участвующие в сохранении изоосмии:
- •Оптические свойства коллоидных систем
- •Растворы высокомолекулярных соединений
- •Свободная и связанная вода в коллоидных pacтвopax
- •Свойства растворов вмс
- •Денатурация
- •2. Белки; биологическая роль Аминокислоты
- •Содержание белков в организме и тканях
- •Методы выделения белков
- •Методы фракционирования и очистки белков
- •Физико-химические свойства белков
- •Аминокислоты
- •Ациклические аминокислоты
- •Структура белковой молекулы
- •Классификация белков
- •Химия сложных белков
- •3. Нуклеиновые кислоты
- •Нуклеотиды и нуклеозиды
- •Структура днк
- •Рибонуклеиновые кислоты
- •4. Ферменты
- •Биосинтез и клеточная локализация ферментов
- •Химическая природа ферментов
- •Строение ферментов
- •Активный центр фермента
- •Регуляция активности ферментов
- •Механизм действия ферментов
- •Основные свойства ферментов
- •2. Зависимость активности ферментов от рН среды.
- •Факторы, определяющие активность ферментов
- •Активирование и ингибирование ферментов
- •Типы ингибирования
- •Классификация и номенклатура ферментов
- •Применение ферментов.
- •Использование иммобилизованных ферментов для производства биологических соединений
- •Иммуноферментный анализ и его использование в ветеринарии
- •5. Химия витаминов
- •Классификация и номенклатура витаминов
- •I. Жирорастворимые витамины
- •II. Витамины, растворимые в воде
- •Витамин d, антирахитический, кальциферол
- •Витамин e, антистерильный, токоферолы
- •Витамин к, антигеморрагический (филлохинон)
- •Витамин q (убихинон)
- •Водорастворимые витамины
- •Витамин b1, антиневритный, тиамин
- •Витамин b2, рибофлавин
- •Витамин b3, пантотеновая кислота
- •Витамин b5, pp, никотинамид, ниацин, антипеллагрический
- •Витамин b6, адермин, пиридоксол
- •Витамин b12, кобаламин, антианемический
- •Фолиевая кислота
- •Витамин с (аскорбиновая кислота)
- •Биотин, витамин h
- •6. Гормоны
- •Гормоны гипофиза
- •Поджелудочная железа
- •Гормоны щитовидной железы
- •Гормоны надпочечников
- •Гормоны коры надпочечников
- •Гормоны половых желез
- •Гормоны тимуса (вилочковой железы)
- •Гормоны местного действия
- •7. Обмен веществ и энергии
- •Основные этапы обмена веществ
- •Биологическое окисление
- •Окислительное фосфорилирование
- •Токсичность кислорода
- •8. Химия и обмен углеводов
- •Моносахариды
- •Производные моносахаридов.
- •Полисахариды (гликаны)
- •Гетерополисахариды (гетерогликаны)
- •Обмен углеводов
- •Катаболизм глюкозы
- •Гликогенолиз
- •Биосинтез углеводов
- •Биосинтез гликогена (гликогенез)
- •Регуляция углеводного обмена.
- •9. Химия и обмен липидов
- •Химическое строение нейтральных жиров
- •Жирные кислоты.
- •Нейтральные гликолипиды
- •Фосфолипиды (фосфатиды)
- •Сфинголипиды
- •Двойной липидный слой мембран
- •Обмен липидов
- •Переваривание липидов в желудочно-кишечном тракте
- •Промежуточный обмен липидов
- •Энергетический баланс β-окисления жирных кислот
- •Метаболизм ацетил-коэнзима а
- •Пути образования кетоновых тел
- •Биосинтез липидов
- •Метаболизм стеринов и стеридов
- •Липосомы
- •10. Обмен белков
- •Биологическая ценность белков
- •Нормы белка в питании животных
- •Белковые резервы организма
- •Обмен простых белков
- •Переваривание белков в желудочно-кишечном тракте моногастричных животных
- •Переваривание белков в кишечнике.
- •Особенности переваривания белков у жвачных животных
- •Дезаминирование аминокислот
- •Трансаминирование – непрямой путь дезаминирования аминокислот
- •Декарбоксилирование аминокислот
- •Окислительное расщепление аминокислот
- •Особенности обмена отдельных аминокислот
- •11. Биосинтез белка
- •Генетический код
- •Этапы синтеза белка
- •Мультиферментный механизм синтеза белка
- •12.Обмен нуклеиновых кислот Переваривание нуклеиновых кислот в желудочно-кишечном тракте
- •Промежуточный обмен нуклеиновых кислот Распад нуклеиновых кислот в тканях
- •Пиримидиновые основания
- •Биосинтез нуклеиновых кислот
- •Рекомбинантные молекулы и проблемы генной инженерии
- •Клонирование животных
- •Метод молекулярной гибридизации
- •Принцип метода
- •Способы гибридизации
- •Метод блоттинга по Саузерну
- •Полимеразная цепная реакция (пцр)
- •Необходимые приборы и реактивы
- •13. Обмен воды и солей
- •Вода, ее содержание и роль в организме
- •Потребность животного организма в минеральных веществах, их поступление и выделение
- •Микроэлементы
- •14. Биохимия крови
- •Физико-химические свойства крови
- •Буферные системы крови
- •Плазма крови и ее химический состав
- •Белки плазмы и сыворотки крови
- •Небелковые азотистые вещества крови
- •Форменные элементы крови
- •15. Биохимия мышечной ткани
- •Механизм сокращения мышцы
- •Азотистые экстрактивные вещества мышц
- •Минеральные вещества
- •Окоченение мышц
- •16. Биохимия молока и молокообразования
- •17. Биохимия почек и мочи
- •Патологические компоненты мочи
- •Особенности мочи птиц
- •18. Биохимия кожи и шерсти
- •19. Биохимия яйца
- •Биосинтез компонентов яйца
- •Предметный указатель
- •Приложения
- •Рекомендуемая литература
- •Тесты для проверки биохимических
- •Глава 8. Химия обмена углеводов
- •24. Сложноэфирные связи в молекулах триацилглицеролов подвергаются ферментативному гидролизу при участии:
- •Глава 11. Синтез белка
- •Глава 12. Обмен нуклеиновых кислот
- •Глава 13. Биохимия почек и мочи
Применение ферментов.
Ферменты получили широкое применение в животноводстве и ветеринарии или в виде свободных ферментных препаратов или же в виде иммобилизованных ферментов. Иммобилизацию ферментов производят путем прикрепления к структурам, не растворимым в воде. Иммобилизованные ферменты легко отделяются от реакционной среды, что позволяет вести процесс непрерывно. Носителем фермента могут быть селикагель, окись алюминия, активированный уголь, полисахариды, иониты, органические полимеры. Связывание фермента может осуществляться методом ковалентного связывания, электростатического связывания, сополимеризации или же фермент может быть включен в полимер, инкапсулирован, включен в липосомы. Для связывания фермента важно при этом сохранение активного центра фермента. В качестве мостика часто используют глутаровый альдегид, бромистый циан (CNBr). Молекулу фермента можно заключить в капсулы, ограниченные мембраной, фиксировать в полимерах, при этом наиболее удобным является полимеризация в полиэтиленгликоле (ПЭГ), в полиакриламиде (ПААГ). Сейчас добились функционирования фермента в течение одного месяца при 60-700C. Использоваться иммобилизованные ферменты могут для аналитических целей, для получения биологических продуктов или же для лечения (в медицине, ветеринарии).
1. Применение в аналитических целях. Существует два типа устройств с иммобилизованными ферментами, применяемые в аналитических целях – ферментные электроды и автоматические
анализаторы.
Ферментный электрод – это датчик, способный генерировать электрический потенциал в результате реакции, катализируемый иммобилизованным ферментом. Разработаны ферментные электроды для определения глюкозы, мочевины, аминокислот, спирта, пенициллина и ряда других веществ.
Например, глюкозочувствительный ферментный электрод содержит иммобилизованную глюкозооксидазу, которая катализирует удаление протонов водорода из раствора со скоростью, зависящей от концентрации в среде глюкозы:
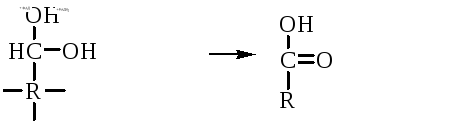
то есть, окисление альдегидов происходит путем дегидрирования. Альдегиды существуют в водных растворах в форме гидратов:
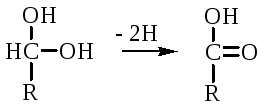
атом водорода затем переходит через пленку к платиновому электроду, меняет потенциал (рН), что и регистрируется прибором. По этому принципу разработан прибор для определения сахара в крови. Прибор напоминает авторучку, где имеется пластинка для нанесения пробы крови (каплю) и экран, указывающий содержание глюкозы в процентах в пробе. Результат получается через 30 секунд после нанесения пробы. В приборе иммобилизованный фермент реагирует с глюкозой, электрический ток (потенциал) показывает на экране процент глюкозы.
По этому же принципу сейчас пользуются индикаторной бумагой, например, для определения глюкозы в моче больных сахарным диабетом: на индикаторную бумагу наносится капля мочи, и, если в ней содержится глюкоза, то под действием иммобилизованного фермента глюкоза окисляется в глюконовую кислоту, что в свою очередь изменяет рН. Показатель очень удобен для контроля состояния больных и назначения лечения.
Разрабатываются подобные приборы для определения холестерина в крови (показатель атеросклероза) и других соединений.
2. Применение ферментов с лечебной целью. Для этого выпускаются ферментные препараты или свободные, или же иммобилизованные. Ферментные препараты, применяемые преимущественно при гнойно-некротических процессах: трипсин, химотрипсин, химопсин, террилитин (Asp.terricola), РНК-аза, ДНК-аза, коллагеназа, аспераза, лизоамидаза (бактериальный фермент), профезим, карипазин (из папайи), лекозим. Ферментные препараты, улучшающие процессы пищеварения: пепсин, сок желудочный, пепсидал, аболин, панкреатин, ораза, сализим, нигедаза (липолитический фермент).
Для применения в ветеринарии выпускаются иммобилизованные ферменты: фермсорб – сополимер метакриловой кислоты и триэтиленгликоль – диметакрилата с сорбированными на нем литическими ферментами. Происходит лизис клеточной оболочки и сорбции полимерной матрицей патогенных микроорганизмов. При диарее телят различной этиологии препарат дают внутрь с кипяченой водой 3 раза в день. Полиферм – сополимер метакриловой кислоты и триэтиленгликоль диметакриловой кислоты с сорбированными в нем протеолитическими ферментами.
При лечении желудочно-кишечных болезней молодняка успешно применяют протеолитические ферменты – пепсин, амилосубтилин, протосубтилин, иммобилизованные ферменты профезим, иммозим. Лизосубтилин – универсальный протеолитический фермент производится у нас в стране в больших объемах.
Лизоцим, гликозидаза, коллитин – бактериолитические ферменты, применяют при желудочно-кишечных заболеваниях молодняка сельскохозяйственных животных.
Фермент гиалуронидаза (лидаза) разрушает гиалуроновую кислоту, тем самым улучшает проницаемость тканей.
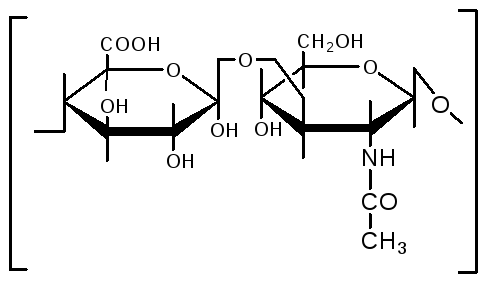
Гиалуроновая кислота
Полимер из глюкуроновой кислоты + ацетилгюкозамина является межклеточным веществом, содержится в структуре кожи, связок, регулирует поступление различных соединений, питательных веществ.
Ферменты – ДНК-аза, РНК-аза применяются для разложения слизистой массы дыхательных путей – для ингаляции, виде салфетки, пропитанной ферментами гиалуронидазой, ДНК-азой, РНК-азой.
3. Применение ферментных препаратов в кормлении животных. В настоящее время в кормлении животных и кормопроизводстве широкое распространение находят ферментные препараты, с помощью которых можно существенно улучшить переваримость и усвоение организмом питательных веществ корма, а также ускорить процессы пищеварения. Для этой цели промышленность выпускает различные ферментные препараты бактерий и грибков. Их получают путем глубинного (Г) или поверхностного (II) культивирования, затем высушивают путём распылительной сушки. Благодаря этому активность фермента повышается по сравнению с исходной в 3, 10, 15 раз, что обозначается как 3х, 10x, 15х.
Широкое применение получили ферментные препараты амилосубтилин и протосубтилин, полученные выращиванием специальных штаммов Bacillus subtilis.
Амилосубтилин ГЗх содержит альфа-амилазу, протеазы, бета-глюказу. Стандартизируется по альфа-амилазной активности.
Протосубтилин ГЗх, содержит те же ферменты, но стандартизируется по нейтральной протеазе.
Различные штаммы Aspergillus awamori служат продуцентами для глюкаваморина, пектаварина, ксилаваморина.
Глюкаваморин П10х содержит альфа-амилазу декстриназу, мальтазу, глюкоамилазу, кислую протеазу, гемицеллюлазу, стандартизируется по декстриназе.
Пектаваморин ГЗх содержит полигалактуроназу, полиметилгалактуроназу, пектинэстеразу, кислую протеазу, стандартизируется по общей пектолитической активности.
Ксилаваморин ГЗх содержит гемицеллюлазу и пектиназу, стандартизируется по гемицеллюлазной активности.
Из культуры Aspergillus oryzae получают препарат амилоризин П10х, который содержит альфа-амилазу, декстриназу, мальтазу, протеазу, стандартизируется по альфа-амилазе.
Кроме того, производят ферментные препараты пектофоетидин ГЗх, пектоклостридин, пектонигрин и т.д.
Добавление указанных ферментных препаратов в корм животных значительно улучшает переваримость грубых кормов, усвоение питательных веществ и увеличение продуктивности.
