
- •Биохимия животных Электронный дидактический комплекс (эдк)
- •Физическая химия вода
- •Активная реакция водных растворов
- •Ионное произведение воды. Водородный показатель
- •Методы определения рН среды
- •Роль активной реакции среды в биологических процессах
- •Буферные pacтворы, состав, механизм действия
- •Буферная емкость
- •Биологическое значение буферных систем
- •Коллоидная химия
- •Классификация дисперсных систем
- •Поверхностные явления
- •Адсорбция
- •Коллоидные растворы (золи) Методы получения
- •Строение коллоидных частиц
- •Коагуляция. Седиментация. Пептизация
- •Молекулярно-кинетические свойства коллоидных растворов
- •Осмотическое давление
- •Биологическое значение явления осмоса
- •Механизмы, участвующие в сохранении изоосмии:
- •Оптические свойства коллоидных систем
- •Растворы высокомолекулярных соединений
- •Свободная и связанная вода в коллоидных pacтвopax
- •Свойства растворов вмс
- •Денатурация
- •2. Белки; биологическая роль Аминокислоты
- •Содержание белков в организме и тканях
- •Методы выделения белков
- •Методы фракционирования и очистки белков
- •Физико-химические свойства белков
- •Аминокислоты
- •Ациклические аминокислоты
- •Структура белковой молекулы
- •Классификация белков
- •Химия сложных белков
- •3. Нуклеиновые кислоты
- •Нуклеотиды и нуклеозиды
- •Структура днк
- •Рибонуклеиновые кислоты
- •4. Ферменты
- •Биосинтез и клеточная локализация ферментов
- •Химическая природа ферментов
- •Строение ферментов
- •Активный центр фермента
- •Регуляция активности ферментов
- •Механизм действия ферментов
- •Основные свойства ферментов
- •2. Зависимость активности ферментов от рН среды.
- •Факторы, определяющие активность ферментов
- •Активирование и ингибирование ферментов
- •Типы ингибирования
- •Классификация и номенклатура ферментов
- •Применение ферментов.
- •Использование иммобилизованных ферментов для производства биологических соединений
- •Иммуноферментный анализ и его использование в ветеринарии
- •5. Химия витаминов
- •Классификация и номенклатура витаминов
- •I. Жирорастворимые витамины
- •II. Витамины, растворимые в воде
- •Витамин d, антирахитический, кальциферол
- •Витамин e, антистерильный, токоферолы
- •Витамин к, антигеморрагический (филлохинон)
- •Витамин q (убихинон)
- •Водорастворимые витамины
- •Витамин b1, антиневритный, тиамин
- •Витамин b2, рибофлавин
- •Витамин b3, пантотеновая кислота
- •Витамин b5, pp, никотинамид, ниацин, антипеллагрический
- •Витамин b6, адермин, пиридоксол
- •Витамин b12, кобаламин, антианемический
- •Фолиевая кислота
- •Витамин с (аскорбиновая кислота)
- •Биотин, витамин h
- •6. Гормоны
- •Гормоны гипофиза
- •Поджелудочная железа
- •Гормоны щитовидной железы
- •Гормоны надпочечников
- •Гормоны коры надпочечников
- •Гормоны половых желез
- •Гормоны тимуса (вилочковой железы)
- •Гормоны местного действия
- •7. Обмен веществ и энергии
- •Основные этапы обмена веществ
- •Биологическое окисление
- •Окислительное фосфорилирование
- •Токсичность кислорода
- •8. Химия и обмен углеводов
- •Моносахариды
- •Производные моносахаридов.
- •Полисахариды (гликаны)
- •Гетерополисахариды (гетерогликаны)
- •Обмен углеводов
- •Катаболизм глюкозы
- •Гликогенолиз
- •Биосинтез углеводов
- •Биосинтез гликогена (гликогенез)
- •Регуляция углеводного обмена.
- •9. Химия и обмен липидов
- •Химическое строение нейтральных жиров
- •Жирные кислоты.
- •Нейтральные гликолипиды
- •Фосфолипиды (фосфатиды)
- •Сфинголипиды
- •Двойной липидный слой мембран
- •Обмен липидов
- •Переваривание липидов в желудочно-кишечном тракте
- •Промежуточный обмен липидов
- •Энергетический баланс β-окисления жирных кислот
- •Метаболизм ацетил-коэнзима а
- •Пути образования кетоновых тел
- •Биосинтез липидов
- •Метаболизм стеринов и стеридов
- •Липосомы
- •10. Обмен белков
- •Биологическая ценность белков
- •Нормы белка в питании животных
- •Белковые резервы организма
- •Обмен простых белков
- •Переваривание белков в желудочно-кишечном тракте моногастричных животных
- •Переваривание белков в кишечнике.
- •Особенности переваривания белков у жвачных животных
- •Дезаминирование аминокислот
- •Трансаминирование – непрямой путь дезаминирования аминокислот
- •Декарбоксилирование аминокислот
- •Окислительное расщепление аминокислот
- •Особенности обмена отдельных аминокислот
- •11. Биосинтез белка
- •Генетический код
- •Этапы синтеза белка
- •Мультиферментный механизм синтеза белка
- •12.Обмен нуклеиновых кислот Переваривание нуклеиновых кислот в желудочно-кишечном тракте
- •Промежуточный обмен нуклеиновых кислот Распад нуклеиновых кислот в тканях
- •Пиримидиновые основания
- •Биосинтез нуклеиновых кислот
- •Рекомбинантные молекулы и проблемы генной инженерии
- •Клонирование животных
- •Метод молекулярной гибридизации
- •Принцип метода
- •Способы гибридизации
- •Метод блоттинга по Саузерну
- •Полимеразная цепная реакция (пцр)
- •Необходимые приборы и реактивы
- •13. Обмен воды и солей
- •Вода, ее содержание и роль в организме
- •Потребность животного организма в минеральных веществах, их поступление и выделение
- •Микроэлементы
- •14. Биохимия крови
- •Физико-химические свойства крови
- •Буферные системы крови
- •Плазма крови и ее химический состав
- •Белки плазмы и сыворотки крови
- •Небелковые азотистые вещества крови
- •Форменные элементы крови
- •15. Биохимия мышечной ткани
- •Механизм сокращения мышцы
- •Азотистые экстрактивные вещества мышц
- •Минеральные вещества
- •Окоченение мышц
- •16. Биохимия молока и молокообразования
- •17. Биохимия почек и мочи
- •Патологические компоненты мочи
- •Особенности мочи птиц
- •18. Биохимия кожи и шерсти
- •19. Биохимия яйца
- •Биосинтез компонентов яйца
- •Предметный указатель
- •Приложения
- •Рекомендуемая литература
- •Тесты для проверки биохимических
- •Глава 8. Химия обмена углеводов
- •24. Сложноэфирные связи в молекулах триацилглицеролов подвергаются ферментативному гидролизу при участии:
- •Глава 11. Синтез белка
- •Глава 12. Обмен нуклеиновых кислот
- •Глава 13. Биохимия почек и мочи
Использование иммобилизованных ферментов для производства биологических соединений
Иммобилизованные ферменты широко применяются для производства различных продуктов и лекарственных препаратов. Иммобилизованный фермент впервые в промышленном масштабе был использован для разделения рацемических смесей D- и L-аминокислот (Япония, 1969 г.). Сейчас реализовано получение L-аспарагиновой кислоты, L-тирозина, L-триптофана и других аминокислот путем присоединения к аминокислотам остатка уксусной кислоты (ацил) и воздействия аминоацилазой, которая гидролизует только ацил L-аминокислот.
В промышленном масштабе получают инвертный сахар (смесь глюкозы и фруктозы, возникающая в результате гидролиза сахарозы) с помощью иммобилизованной β-фруктофуранозидазы (сахаразы). Этот фермент очень устойчив и за десять лет непрерывной работы одного из реакторов его активность снизилась всего на 10%.
С помощью иммобилизованного фермента глюкозоизомеразы в больших объемах получают из кукурузного крахмала смесь глюкозы и фруктозы. Этот фермент глюкозу превращает во фруктозу. Такие установки функционируют в США (с 1972 г.), ФРГ, Дании, Голландии. В нашей стране изомеризацию глюкозы в фруктозу ведут в реакторе с помощью глюкозоизомеразы из Actinomyces olivocinereus, иммобилизованной на силохроме. Глюкозо-фруктозная смесь является очень важным продуктом для больных сахарным диабетом.
Иммобилизованные ферменты широко применяются для синтеза аминокислот. Так, в 1974 г. в Японии начат промышленный синтез L-аспарагиновой кислоты с участием фермента аспартат-аммиаклиазы, иммобилизованный на фенол-формальдегидной смоле. Фермент осуществляет образование L-аспарагиновой кислоты из аммония и фумаровой кислоты. L-триптофан синтезируют из индола и серина при помощи фермента триптофан-синтетазы, L-тирозина с участием иммобилизованной тирозин-фенол-лиазы.
Иммобилизованные ферменты применяются для производства антибиотиков и гормональных препаратов.
Для производства некоторых продуктов удобнее пользоваться не иммобилизованными ферментами, а иммобилизованными микробными клетками – продуцентами ферментов. Так, этанол получают из глюкозы с помощью иммобилизованных в полиакриламидном геле клеток Saccharomyces cerevisiae. Первый в мире промышленный реактор проточного типа объемом в одну тонну по синтезу L-аспарагиновой кислоты из фумарата аммония был запущен в Японии (1973 г.). В нем использованы иммобилизованные в полиакриламидном геле клетки кишечной палочки (Esherichia coli), содержащие аспартат-аммиак-лиазу:
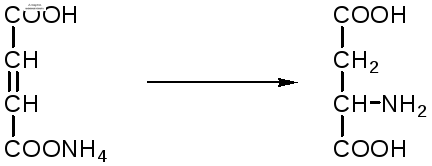
фумарат аспарагиновая
аммония кислота
Реактор давал около 2000 кг L-аспарагиновой кислоты в сутки при 95%-ном уровне превращения в нее введенного фумарата аммония. При подкислении элюата до рН 2,8 и охлаждении до 15оC аспарагиновая кислота выделялась в виде кристаллов. Иммобилизованные клетки E.coli сохраняли активность фермента в течение четырех месяцев, в то время как интактные клетки только в течение 10 дней.
L-изолейцин синтезируют из треонина и глюкозы при посредстве иммобилизованных клеток Serratia marcescens с выходом до 4 г/л элюата с колонки реактора. Таким же образом получают незаменимую аминокислоту L- лизин:
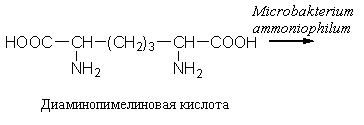
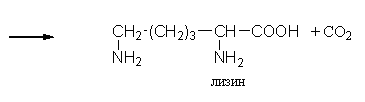
При помощи иммобилизованных клеток Corynobacterium glutamicum производят L-глутаминовую кислоту из глюкозы; E coli – L-триптофан из индола, Streptococus faecalis – L-орнитин из L-аргинина. С помощью иммобилизованных микроорганизмов синтезируют L-формы аминокислот – аланина, фенилаланина, метионина, треонина. Таким образом, производство L-аминокислот для питания человека и выращивания сельскохозяйственных животных и птиц осуществляется в основном в реакторах с иммобилизованными клетками.
Отработаны способы получения яблочной кислоты из фумаровой, пропионовой, уксусной и пировиноградной кислот из глюкозы, лактозы или лактата натрия в проточной системе с клетками пропионовокислых бактерий, иммобилизованными в полиакриламидный гель.
Иммобилизованные ферменты широко применяют для производства различных гормональных препаратов.
Производится в больших масштабах аспартам – метиловый эфир аспартил-фенилаланина:
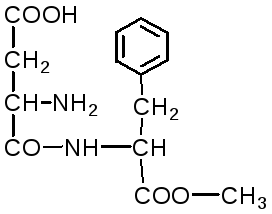
Аспартам
Аспартам в 300 раз слаще сахара, безвреден, в организме расщепляется на аспарагиновую кислоту и фенилаланин, используется для детского питания, добавляется в диетическую кока-колу. Ферменты, синтезирующие аспарагиновую кислоту и фенилаланин, получены генно-инженерным методом.
