
- •1. Зависимость термодинамических функций от температуры
- •2. Фазовое равновесие в однокомпонентных системах
- •Зависимость теплоты фазового перехода от температуры описывается уравнением:
- •С учетом уравнения (21) уравнение (17) в интегральной форме принимает вид
- •3. Закон распределения. Экстракция Закон распределения выражается уравнением
- •4. Термодинамика растворов неэлектролитов
- •Для бинарного раствора парциальные давления компонентов AиBопределяются законом Рауля
- •Отсюда следует
- •Химический потенциал. Активность. Коэффициент активности
- •Коллигативные свойства растворов
- •5. Растворы сильных электролитов
- •6. Химическая кинетика сложных реакций
- •Для мономолекулярных обратимых реакций типа а в дифференциальная форма кинетического уравнения имеет вид
- •Считая концентрации n2o* и о.Стационарными, найти выражение для скорости распадаN2o.
- •7. Поверхностные явления. Адсорбция
- •Адсорбция на границе жидкость – газ
- •Содержание
- •2. Фазовое равновесие в однокомпонентных системах
- •4. Термодинамика растворов неэлектролитов
6. Химическая кинетика сложных реакций
При кинетическом изучении сложных реакций применяют принцип независимости(являющийся одним из постулатов химической кинетики):
если в системе протекают несколько реакций, то каждая из них подчиняется основному закону химической кинетики и протекает независимо от других химических реакций.
Константа скорости элементарной химической стадии не зависит от протекания в реакционной системе других элементарных стадий. Из этого постулата следует, что скорость реакции по одному из веществ ее участников - равна алгебраической сумме скоростей тех элементарных стадий, в которых это вещество принимает участие.
Для мономолекулярных обратимых реакций типа а в дифференциальная форма кинетического уравнения имеет вид
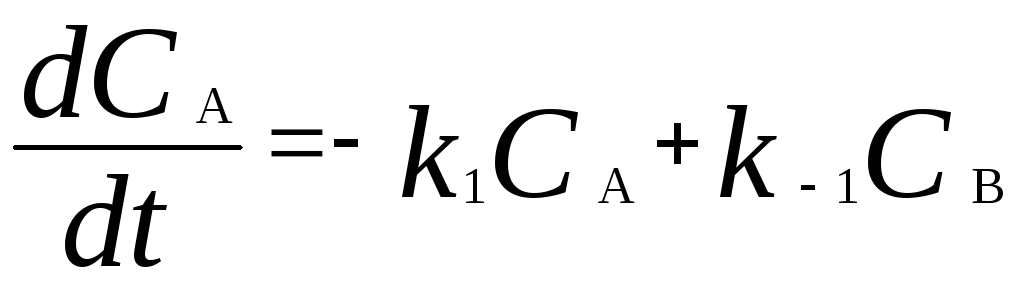 .
.
Здесь k1– константа скорости прямой реакции,k – 1 – константа скорости обратной реакции. При равновесии
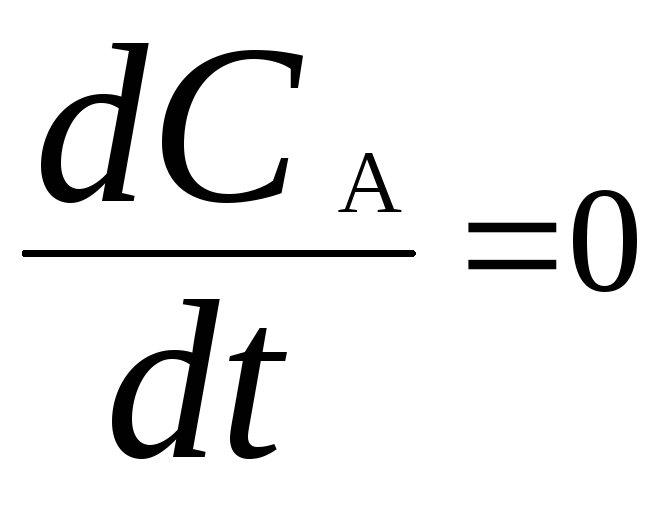 .
.
Если при t= 0СB= 0, то справедливы следующие соотношения

где С А, С B - текущие концентрации веществ A и B; С А 0 - начальная концентрация A при t = 0; k 1 и k – 1 – константы скоростей прямой и обратной реакций; СА и С В - равновесные концентрации A и B; K – константа равновесия. Интегральная форма кинетического уравнения
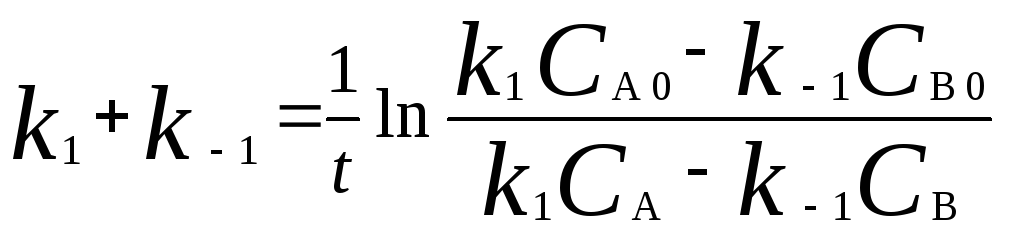 .
.
При условии, что при t = 0СB0= 0
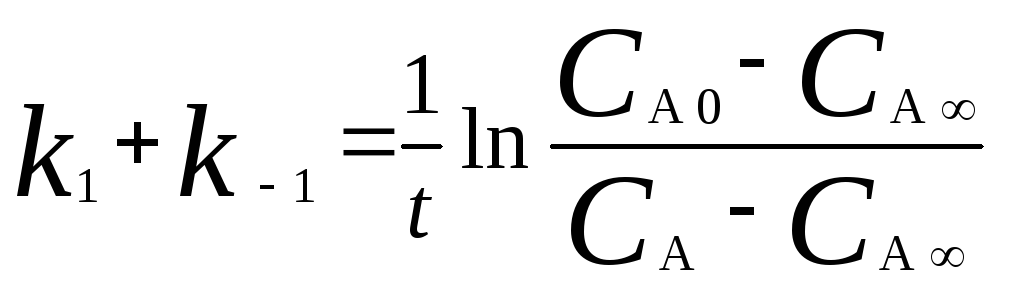 .
.
Для мономолекулярных параллельных реакций типа
 B (k1)
B (k1)![]()
![]()
 A
A
C (k 2)
дифференциальная форма кинетического уравнения имеет вид
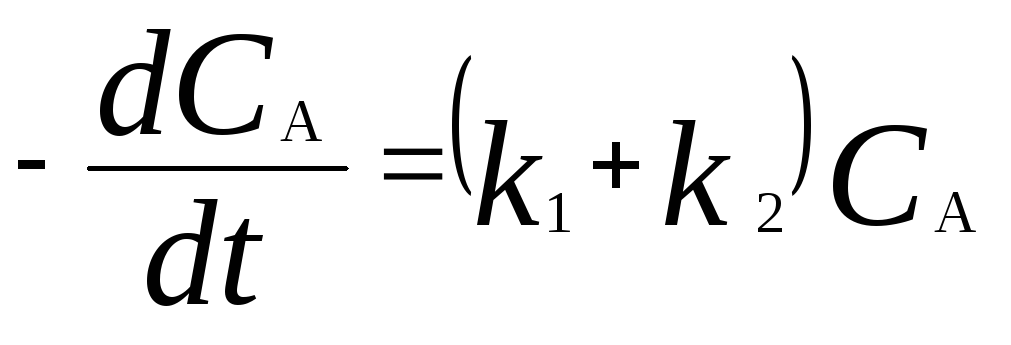 .
.
Интегрирование приводит к следующему результату
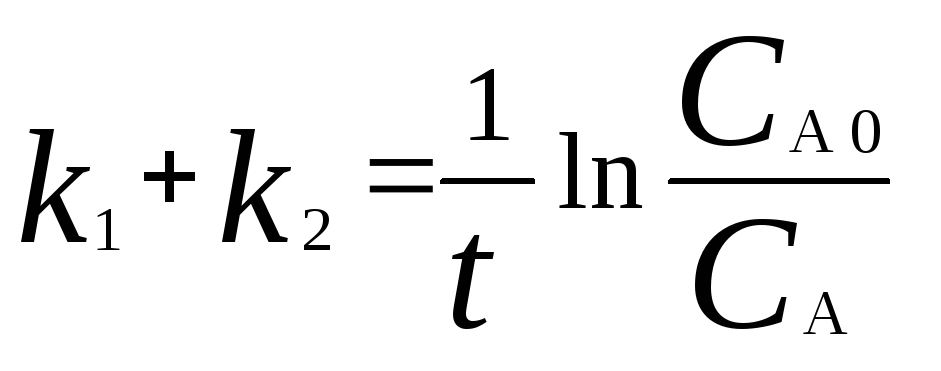 ,
,
где k1иk2– константы скоростей первой и второй реакций. Константы скоростей отдельных стадий для реакций данного типа определяют по соотношению
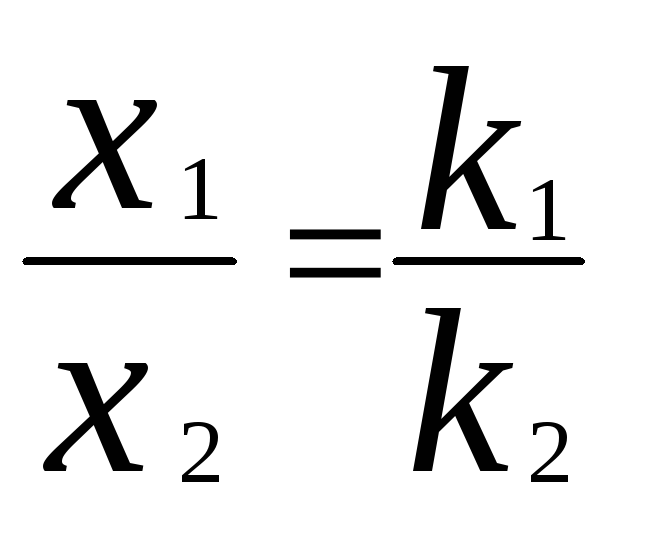 ,
,
где x1иx2 – количества моль веществBиC, образовавшихся к моменту времениt.
Для последовательных реакций первого порядка типа
![]()
дифференциальные кинетические уравнения имеют вид
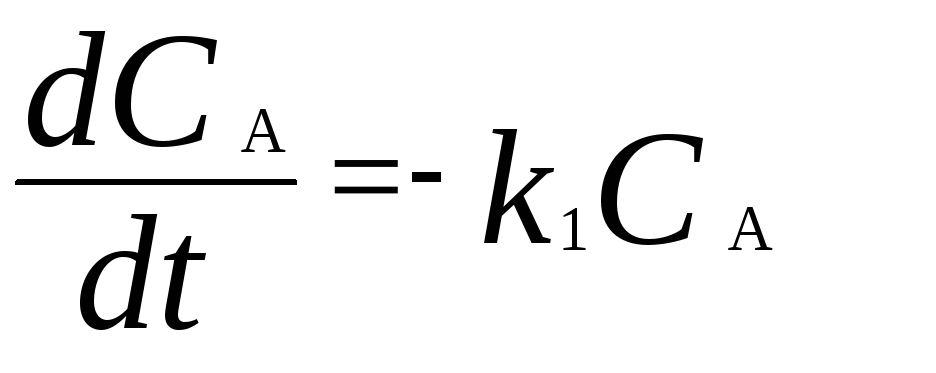 ,
,
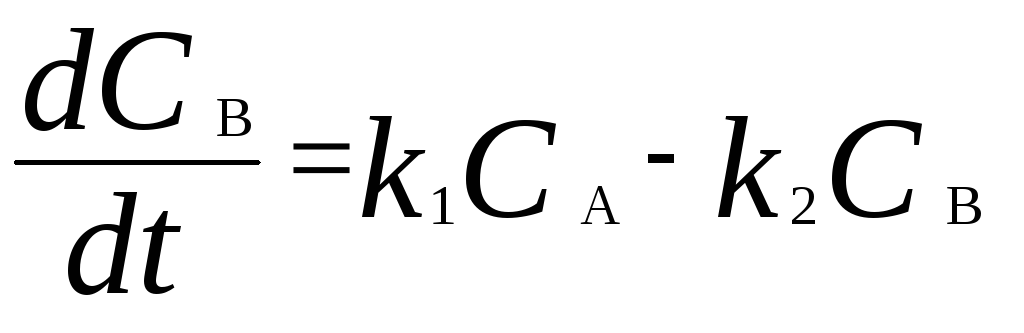 ,
,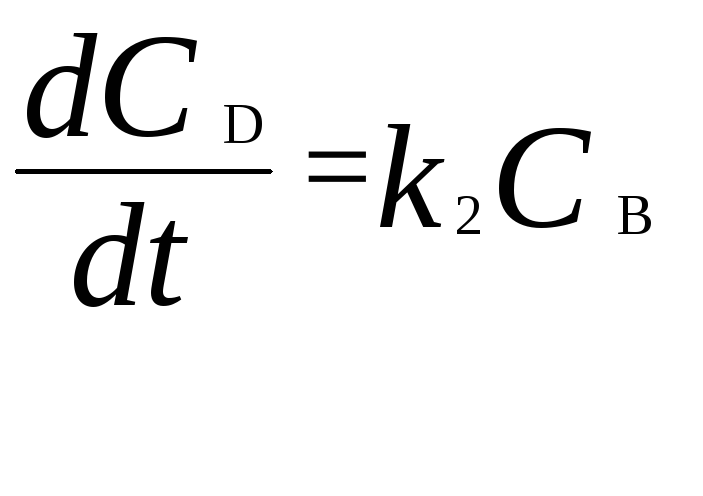 .
.
Решение этих уравнений приводит к следующим результатам
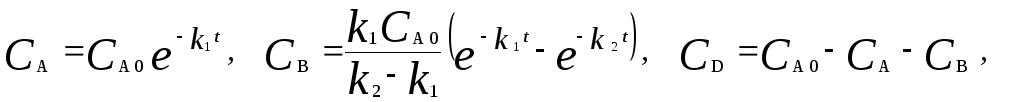
где С А, С B , С D – текущие концентрации веществ А, В и D; С А 0 – начальная концентрация вещества A; k 1 и k 2 – константы скоростей первой и второй стадий.
Точка максимума на кинетической кривой СB=f(t) характеризуется уравнениями:
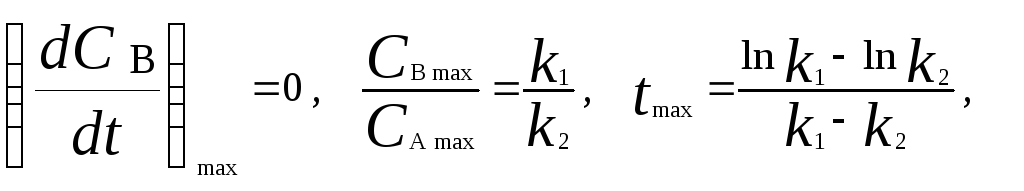
где tmax – время, соответствующее максимальной концентрации веществаB.
Приближенные методы химической кинетики
В сложных реакциях с участием активных промежуточных частиц используется метод квазистационарных (или стационарных) концентраций.В этих реакциях за малый промежуток времени (мало изменение концентрации исходных веществ) в системе устанавливается режим, при котором разность скоростей образованияroи расходованияrpпромежуточных частиц становится малой по сравнению с этими скоростями. Такой режим процесса называетсяквазистационарным, а соответствующие ему концентрации промежуточных частиц -квазистационарными концентрациями. В квазистационаром режиме можно полагать:
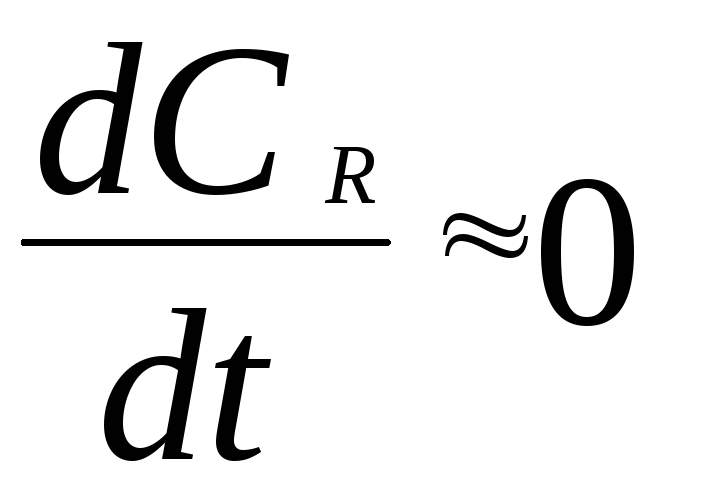 ,
,
где
![]() -
концентрация промежуточных частиц. В
-
концентрация промежуточных частиц. В![]() результате можно выразить концентрации
промежуточных частиц через концентрации
стабильных веществ, принимающих участие
в данном процессе. Если время установления
квазистационарного режима мало,
концентрации активных промежуточных
частиц будут непрерывно подстраиваться
к новым квазистационарным значениям,
то есть квазистационарный режим не
будет нарушаться на протяжении всего
процесса. Таким образом, метод
квазистационарных концентраций состоит
в том, что в системе дифференциальных
уравнений, описывающей сложный химический
процесс, дифференциальные уравнения
для активных промежуточных частиц
заменяются алгебраическими уравнениями,
выражающими равенство скоростей
образования и расходования этих частиц.
Метод квазистационарных концентраций
применяется обычно к реакциям с участием
свободных радикалов, которые представляют
собой реакционноспособные неустойчивые
частицы.
результате можно выразить концентрации
промежуточных частиц через концентрации
стабильных веществ, принимающих участие
в данном процессе. Если время установления
квазистационарного режима мало,
концентрации активных промежуточных
частиц будут непрерывно подстраиваться
к новым квазистационарным значениям,
то есть квазистационарный режим не
будет нарушаться на протяжении всего
процесса. Таким образом, метод
квазистационарных концентраций состоит
в том, что в системе дифференциальных
уравнений, описывающей сложный химический
процесс, дифференциальные уравнения
для активных промежуточных частиц
заменяются алгебраическими уравнениями,
выражающими равенство скоростей
образования и расходования этих частиц.
Метод квазистационарных концентраций
применяется обычно к реакциям с участием
свободных радикалов, которые представляют
собой реакционноспособные неустойчивые
частицы.
Квазиравновесное приближениеприменяют тогда, когда одна из реакций является обратимой, причем равновесие быстро устанавливается и медленно разрушается. Рассмотрим кинетическую схему:
1. A B ; (k 1 , k – 1 )
2. B C . (k 2 )
Поскольку равновесие на первой стадии устанавливается быстро, то k2k – 1. Тогда концентрацию промежуточного продукта В можно выразить через константу равновесия:
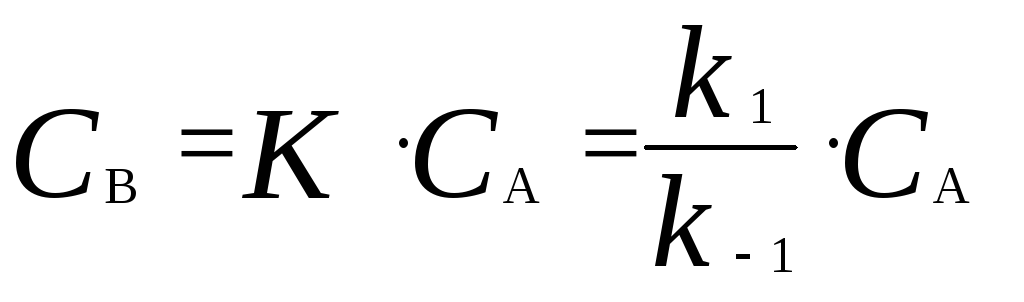 .
.
Скорость реакции равна:
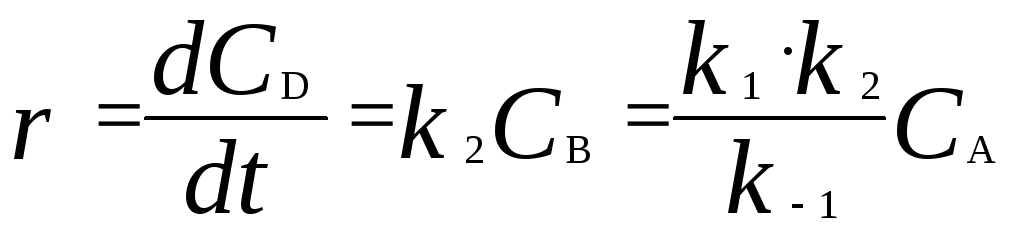 .
.
Мы получили уравнение реакции первого порядка.
Пример 16.Для обратимого процесса АВ константы скоростей прямой и обратной реакций равны соответственноk1= 0,4c– 1,k2= 0,05c– 1. Начальные концентрации веществ А и В равны 0,04 моль/л. Определить какими окажутся концентрации этих веществ через 0,2 с.
Решение.
 ,
,
где x– количество прореагировавшего вещества А,aиb– начальные концентрации веществ А и В. Решение этого уравнения:
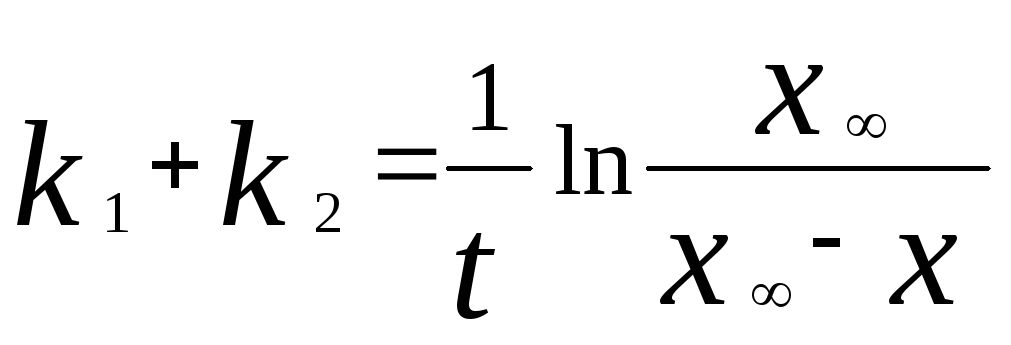 . (*)
. (*)
Здесь
![]() -
количество прореагировавшего вещества
А к моменту равновесия – равно
-
количество прореагировавшего вещества
А к моменту равновесия – равно
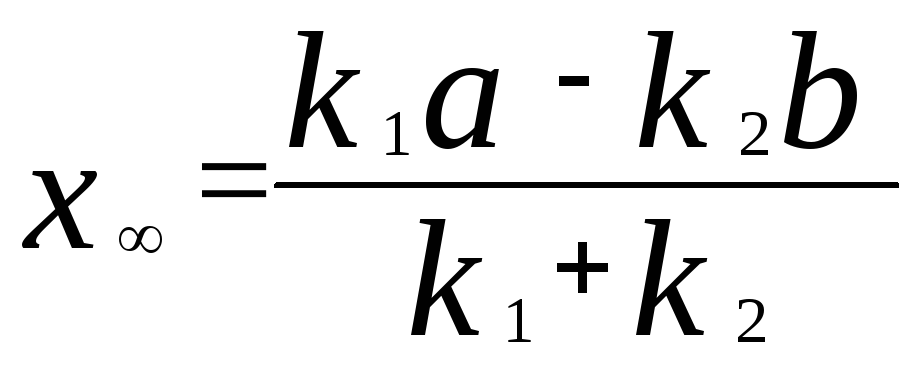 .
.
При tнаступает равновесие, которое характеризуется константой равновесия
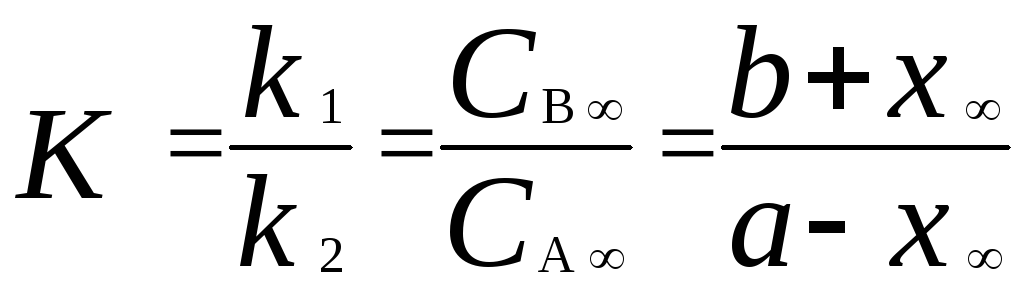 .
.
Вычисляем
![]()
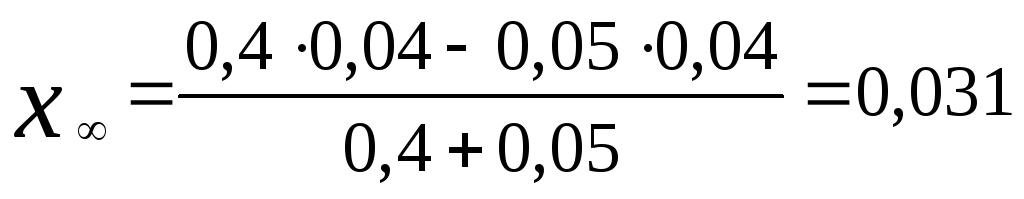 моль/л
моль/л
Из уравнения (* ) получаем
![]() моль/л;
моль/л;
СА= 0,04 – 0,0027 = 0,0373 моль/л;
СВ= 0,04 + 0,0027 = 0,0427 моль/л.
Пример 17.В параллельных реакциях первого порядка: 1. АВ ; (k1)
2. A D ; (k 2 )
Выход вещества В равен 40 %, а время превращения А на 30 % равно 5 мин. Найти k1иk2.
Решение.Кинетическое уравнение для превращения вещества в двух параллельных реакциях первого порядка имеет вид
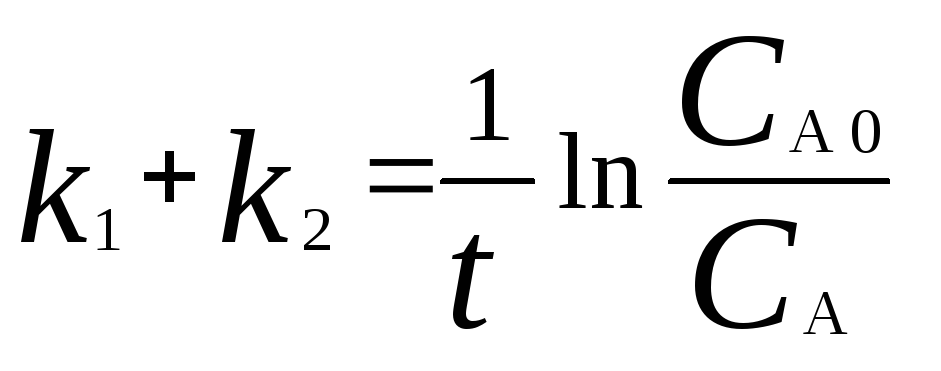 .
.
С учетом превращения вещества А на 30 % получаем уравнение:
![]() ,
,
где а– начальная концентрация вещества А. Вычисляем
![]() .
.
Выход вещества В равен 40 %, следовательно выход вещества D– 60 %. Отношение этих выходов равно отношению конечных концентраций веществ В иD. Следовательно, отношение соответствующих констант скоростей равно:
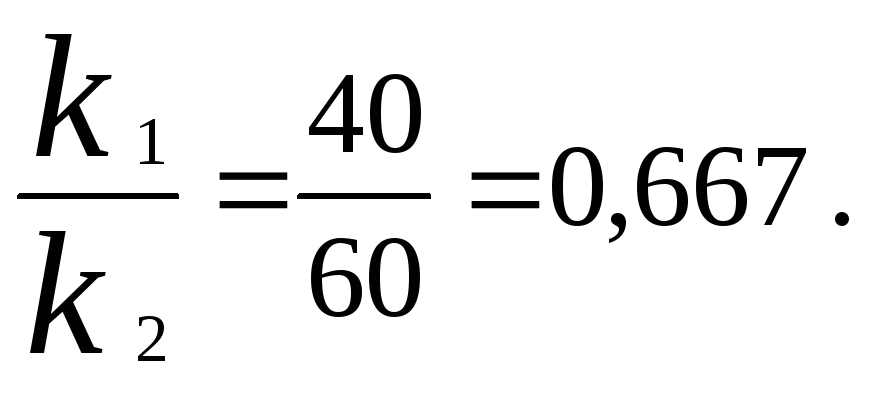
Решаем систему уравнений:
k 1 = 0,667 k 2 , k 1 + k 2 = 0,071.
0,667 k 2 + k 2 = 0,071 ; k 2 = 0,043 мин – 1; k 1 = 0,028 мин – 1 .
Пример 18.В системе осуществляется последовательная реакция
![]() .
.
Начальная концентрация вещества А равна 1 моль/л, вещества В и Dв начальный момент в системе отсутствуют. Константы скорости равныk1= 0, 2 мин– 1иk2= 0, 05 мин– 1. Вычислите: 1) время достижения максимальной концентрации вещества В; 2) максимальную концентрацию вещества В; 3) время достижения концентрацииСА= 0,01 моль/л.
Решение.1. Рассчитаем время, которое будет соответствовать максимальной концентрации промежуточного вещества В:
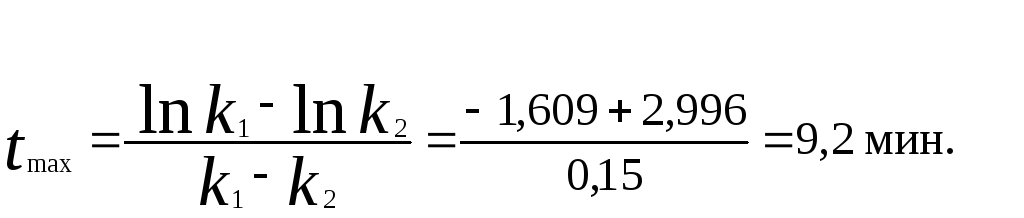
2. Рассчитаем концентрацию вещества А через время tmax:
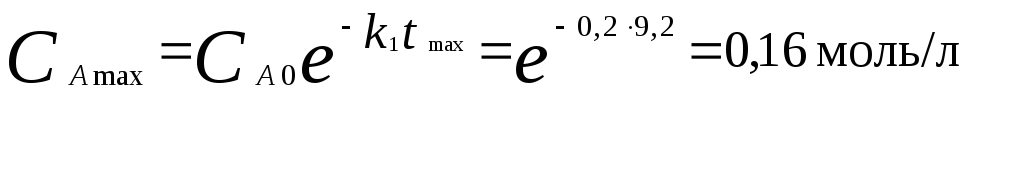 .
.
Максимальная концентрация промежуточного вещества равна:
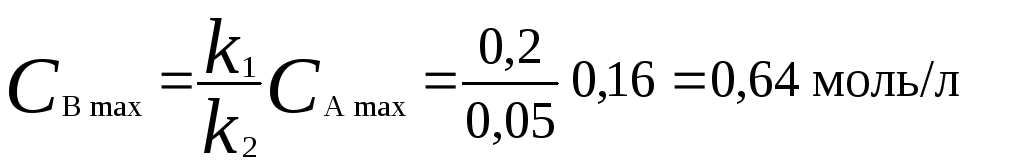
3. Рассчитаем время txдостижения концентрацииСА= 0,01 моль/л:
![]()
Пример 19. Реакция превращения пара-водорода в орто-водород протекает по следующему механизму (М – инертная частица):
1. п-Н2+ МН + Н + М ;
2. Н + п-Н2Н +о-Н2;
3. Н + Н + М п-Н2+ М .
Пользуясь методом квазистационарных концентраций, получить выражение для скорости конверсии пара-водорода.
Решение.Из уравнения (2) следует, что скорость образования орто-водорода равна:
![]() .
.
Метод квазистационарных концентраций применяем для активных атомов водорода
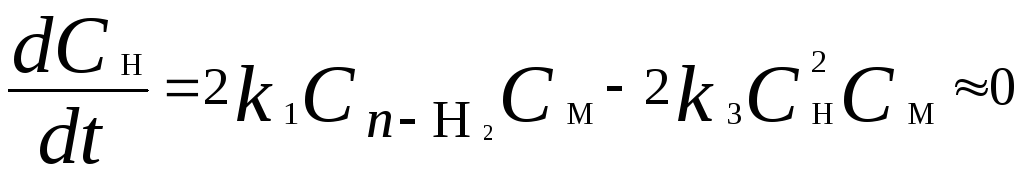 .
.
Из этого выражения следует, что
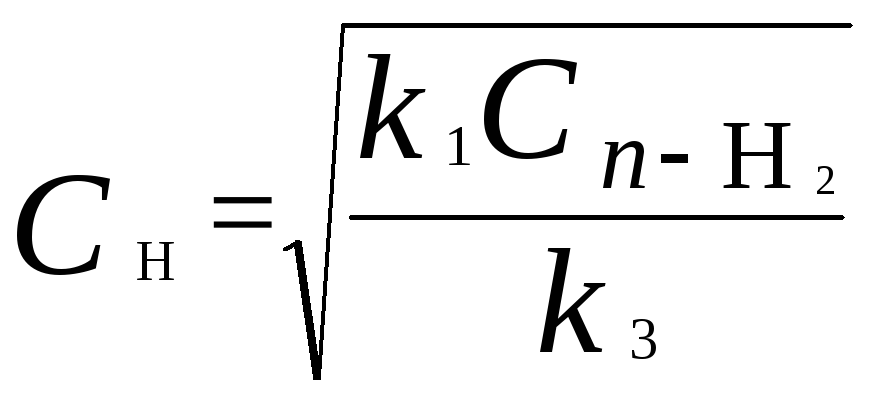 .
.
Заметим, что в реакции (2) число атомов Н не изменяется, поэтому скорость изменения их концентрации определяется первой и третьей реакциями. Таким образом, получаем
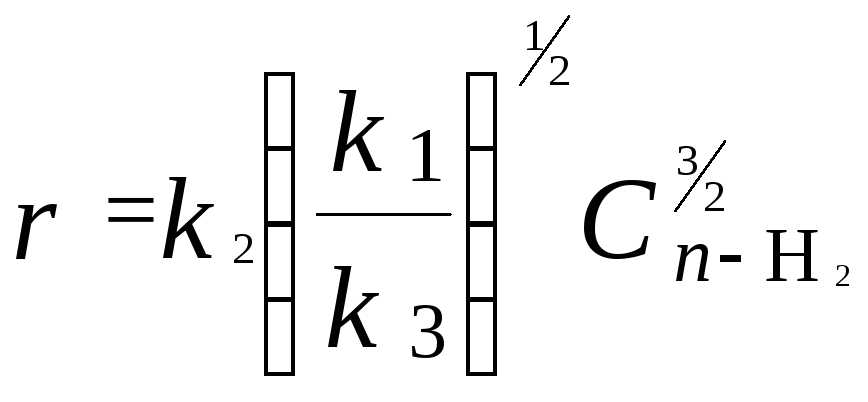 .
.
Задачи
163. Для обратимого процесса А В константы скоростей прямой и обратной реакций равны соответственно k 1 = 0,01 c – 1 и k 2 = 0,15 c – 1. Начальные концентрации веществ А и В взяты равными 0,2 моль/л. Определить концентрации этих веществ через 8 с.
164. Константа равновесия обратимой реакции А В равна 10, а константа скорости прямой реакции равна 0,2 с – 1. Определить время, за которое концентрации обоих веществ достигнут равенства, если вначале в системе содержалось только вещество А.
165. Для обратимой реакции А В начальные концентрации веществ равны С A0 =
= 0,4 моль/л и С В0 = 0. Через 10 мин после начала реакции С A = 0,15 моль/ л и С В =
= 0,25 моль/ л. Определить концентрацию вещества А через 20 мин, если константа равновесия реакции равна K = 3.
166. Константа скорости гомогенного мономолекулярного процесса цис-транс-изомеризации бутена при 417 0С равна 1,6.106 с– 1. Константа равновесия при этой температуре равна 1,14. В начальный момент времени в системе присутствует только цис-изомер. Вычислить время достижения равных концентраций изомеров.
167. Для реакции изомеризации А В при 25 0 С концентрации исходного вещества А в разные моменты времени даны в таблице. Равновесная концентрация вещества А составила С A = 0,078 моль / л. Найти константы скоростей прямой k 1 и обратной реакций k 2 . Начальная концентрация С В0 = 0.
-
t, ч
С At , моль / л
0
0,366
71,8
0,277
215,8
0,174
333,3
0,130
168. Константа равновесия обратимой реакции А В равна 10, а константа скорости прямой реакции равна 0,2 с – 1. Начальные концентрации веществ А и В равны 0,3 моль/л и 0 моль/л соответственно. Определить время, за которое прореагирует 10 % вещества А.
169. Для обратимого процесса АВ известно, чтоk1+k- 1= 5,13.10- 5c– 1, аk1/k- 1= 0,575. Начальная концентрация вещества А равна 0,32 моль/л, а вещества В в начальный момент времени нет. Определить концентрации веществ через 100 мин после начала реакции.
170. Для обратимой реакции АВ начальные концентрации составляютСА0= 18,23 моль/л и СВ 0= 0 моль/л,k1= 0,027 с– 1. Равновесная концентрация вещества А равна 4,95 моль/л. Определить значениеk- 1.
171. Константа скорости прямой реакции А В при некоторой температуре равна 10, а константа скорости прямой реакции равна 5.10- 4 с– 1. Константа равновесия равна 1,6. В начальный момент присутствует только вещество А. Определить время, за которое прореагирует 30 % вещества А.
172. Константа равновесия обратимой реакции А В равна 1,4, а константа скорости прямой реакции равна 6.10– 5 с– 1.Определите, какая доля начального количества вещества прореагирует за 40 мин, если в начальный момент в системе содержалось только вещество А.
173. В параллельных реакциях первого порядка: 1. А В; (k 1) , 2. АD. (k2) выход вещества В равен 53 %, а время превращения вещества А на 1 / 3 равно 40 с. Найтиk1иk2.
174. Параллельные элементарные реакции: 1. АВ , 2. 2 АС характеризуются следующими данными: скорости обеих реакций равны при концентрации вещества А, равной 0,2 моль / л, а при концентрации вещества А равной 0,4 моль / л скорость превращения А составляет 0,24 моль / (л.с). Определить значения констант скоростейk1 иk2.
175. Параллельные элементарные реакции: 1. А В, 2. А С характеризуются следующими данными: выход вещества В равен 63 %, а время полупревращения вещества А по приведенной схеме составляет 19 мин. Рассчитать значения констант скоростей k 1 и k 2.
176. Определить, сколько азота и оксида азота (I) образуется через 0,1 с при нагревании
4 моль/ л окиси азота при 1300 К, если константы скорости параллельных бимолекулярных реакций равны k 1 = 25,7 и k2 = 18,2 л/(моль . с).
N2 + O2 (k 1 )
2 NO
N2O + 0,5 O2 . (k 2)
177. Реакция разложения вещества А может протекать параллельно по трем направлениям:
1. А В, 2. А D, 3. А F. Концентрации продуктов в смеси через 5 мин после начала реакции были равны: С B = 2 моль / л, C D = 1,5 моль / л, C F = 3 моль / л. Определить константы скорости k1, k2, k3, если период полураспада вещества А равен t ½ = 8 мин.
178. Для некоторой системы, в которой протекают конкурирующие необратимые реакции:
1. А + В ® D ; 2. А + С ® F ; при 25 0 С соотношение продуктов составило C D : C F = 1 : 5. При 60 0 С соотношение продуктов составило C D : C F = 1 : 3. Определить энергию активации реакции 2, если для первой реакции она составляет 30 кДж / моль.
179. Последовательная реакция А В С характеризуется следующими данными: при достижении максимума концентрации вещества В отношение концентраций С А / С В = 4 : 5, а время превращения вещества А на 25 % составляет 85 с. Определить значения констант скоростей k 1 и k 2.
180
. В системе осуществляется последовательная
реакция
![]()
Максимальная концентрация вещества В равно 0,77 [A] 0 и достигается через 170 мин после начала реакции. Рассчитать k 1 и k 2 .
181. Распад радиоактивного изотопа Zn30по схеме:Zn30Ga31Ge32
характеризуется тем, что максимальное содержание радиоактивного изотопа галлия в образце достигается через 30,3 суток. Причем отношение числа атомов изотопа цинка к числу атомов изотопа галлия в это время оказывается равным 3,48. Определить периоды полураспада изотопов цинка и галлия.
182. Последовательная реакция первого порядка протекает по схеме:
![]() .
.
При 298 К k1= 0,1 мин- 1;k2= 0,05 мин- 1; начальная концентрация исходного веществаСA0 = 0,5 моль / л. Вычислить: 1. координаты максимума кривойС B =f(t); 2. Время достижения концентрацииС A = 0,001 моль / л (продолжительность реакции АB); 3. концентрацииС BиС D в момент окончания реакции АB.
183. Образец радиоактивного урана массой 200 г распадается по схеме:
![]()
(над стрелками указаны периоды полураспада). Рассчитать массы нептуния и плутония через 10 мин. После начала распада. Определить максимальную массу нептуния, которая может быть получена из данного образца урана.
184. Образец радиоактивного урана массой 200 г распадается по схеме:
![]() ,
,
где значения констант составляют k1 = 4,7 . 10 – 18 с – 1 и k2 = 1,381 . 10 – 11 с – 1 . Определить периоды полураспада урана и радия и максимальную массу, которая может быть получена из данного образца урана.
185. Был предложен следующий механизм термического разложения озона:
О3®O2 + O (k1)
O + O2 ® O3 (k – 1)
O + O3 ® 2O2 (k 2)
С помощью метода квазистационарных концентраций получить выражение для скорости распада, включающее константы k1,k- 1,k2и концентрации О2и О3.
186. Для реакцииNO2ClNO2+ 0,5Cl2предложен следующий двухстадийный механизм:
1. NO2Cl NO2 + Cl . (k 1 );
2. NO 2 Cl + Cl . NO 2 + Cl 2. (k 2 )
Используя метод квазистационарных концентраций, вывести уравнение для скорости разложения NO2Cl.
187. В одной из теорий мономолекулярных реакций был предложен следующий механизм активации молекул (схема Линдемана): 1. А + АА* + А, (k1) (активация)
2. А + А* А + А, (k- 1) (дезактивация)
3. А* В +D. (k 2) (распад)
Используя метод квазистационарных концентраций, вывести уравнение для скорости мономолекулярной реакции и определить порядок реакции при больших и малых концентрациях А.
188. Предложен следующий механизм для гомогенного пиролиза метана (М - инертная молекула): 1.CH4 + М ® CH3 . + H . + М; (k 1)
2. CH4 + CH3 . ® C2H6 + H . ; (k 2)
3. CH4 + H . ® CH3 . + H2 ; (k 3)
4. H . + CH3 . + M ® CH4 + M. (k 4)
Вывести уравнение для скорости образования C2H6на основе приведенного механизма, используя метод стационарных концентраций. Концентрации СН3 и Ночень малы, поэтому стационарны и не должны входить в уравнение.
189. Химическая реакцияN2ON2+ 0,5O2протекает по следующему механизму (М – инертная частица): 1.N2O+ МN2О* + М; (k1)
2. N2O * N2 + O . ; (k 2)
3. N2O* + МN2О + М; (k3)
4. N2O+ ОN2+O2; (k4)
