
- •1. Зависимость термодинамических функций от температуры
- •2. Фазовое равновесие в однокомпонентных системах
- •Зависимость теплоты фазового перехода от температуры описывается уравнением:
- •С учетом уравнения (21) уравнение (17) в интегральной форме принимает вид
- •3. Закон распределения. Экстракция Закон распределения выражается уравнением
- •4. Термодинамика растворов неэлектролитов
- •Для бинарного раствора парциальные давления компонентов AиBопределяются законом Рауля
- •Отсюда следует
- •Химический потенциал. Активность. Коэффициент активности
- •Коллигативные свойства растворов
- •5. Растворы сильных электролитов
- •6. Химическая кинетика сложных реакций
- •Для мономолекулярных обратимых реакций типа а в дифференциальная форма кинетического уравнения имеет вид
- •Считая концентрации n2o* и о.Стационарными, найти выражение для скорости распадаN2o.
- •7. Поверхностные явления. Адсорбция
- •Адсорбция на границе жидкость – газ
- •Содержание
- •2. Фазовое равновесие в однокомпонентных системах
- •4. Термодинамика растворов неэлектролитов
2. Фазовое равновесие в однокомпонентных системах
Общее условие равновесия фаз в однокомпонентной системе выражается уравнением Клаузиуса – Клапейрона
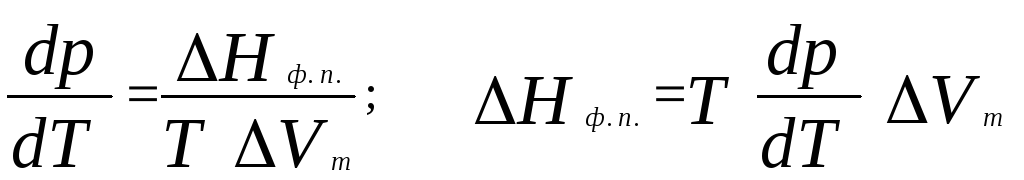 , (17)
, (17)
где Нф. п.– энтальпия фазового перехода первого
рода в условиях равновесия фаз (испарение,
плавление, возгонка, превращение
модификаций);dP/dT– температурный
коэффициент давления насыщенного пара;Vm–
разность молярных объемов фаз, находящихся
в равновесии. Для равновесий: твердое
веществопар и
жидкостьпар в
области температур, далеких от критической,
при условии, что![]()
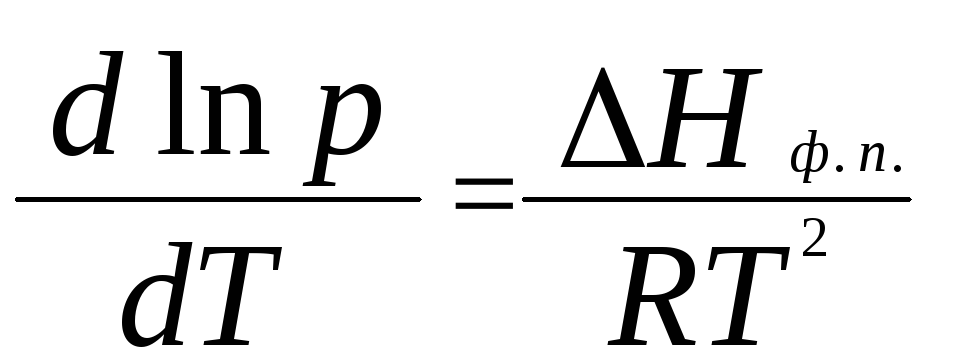 (18)
(18)
И![]() нтегрирование
уравнения (18) при условии, чтоНф. п .= const, приводит к уравнению
нтегрирование
уравнения (18) при условии, чтоНф. п .= const, приводит к уравнению
 ,
,![]() (19)
(19)
или
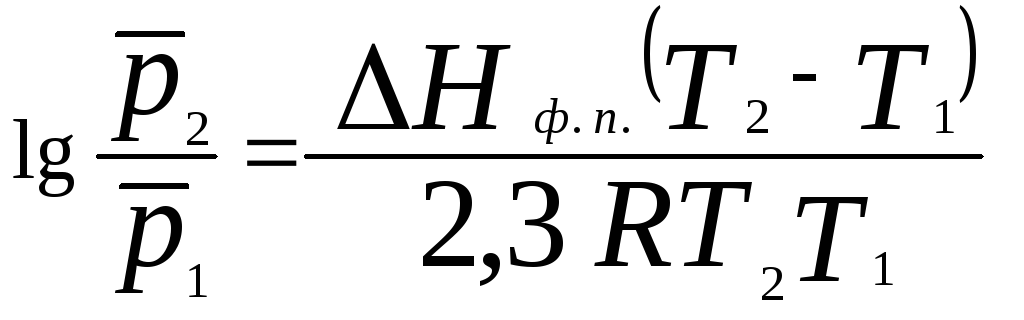 (20)
(20)
Значения Нф. п.в уравнениях (19) и (20) являются средней величиной, справедливой для интервала температурТ1 -Т2. Молярные энтальпии возгонки, плавления и испарения при данной температуре связаны уравнением:
![]() .
.
Энтальпию испарения жидкости можно приближенно оценить по правилу Трутона, согласно которому молярная энтропия испарения в нормальной точке кипения (при p= 1 атм) приблизительно постоянна:
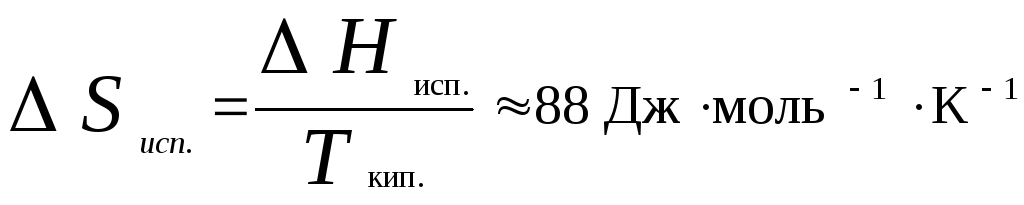 .
.
Зависимость теплоты фазового перехода от температуры описывается уравнением:
![]() ,
,
где CиC- теплоемкости находящихся в равновесии фази. В небольшом интервале температурСф. п .= const, тогда
![]()
или
![]() . (21)
. (21)
С учетом уравнения (21) уравнение (17) в интегральной форме принимает вид
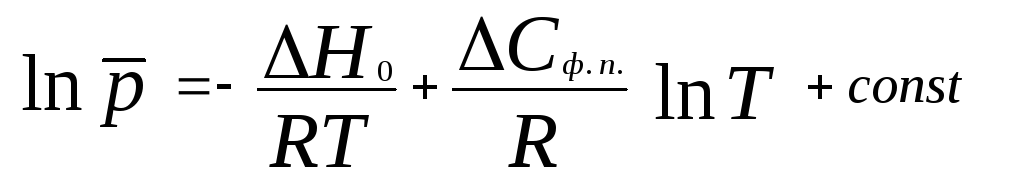 .
.
Пример 5. Зависимость давления насыщенного пара от температуры дляHCNвыражается уравнением:lgp= 9,16 – 1237 /Т. Определить теплоту испарения при температуре кипения.
Решение.Приp= 1,013 · 105Па ;Т=Тн.т.кип.и, следовательно,
lg1,013 · 105= 9,16 – 1237 /Т н.т.кип; Откуда,Т н.т.кип= 299 К .
Для расчета ΔНисп.воспользуемся уравнением КлаузиусаКлапейрона:
 .
.
Найдем d ln p/dT, дифференцируя уравнение зависимости давления пара от температуры:
d ln p / dT = 2,3 · 1237 / Т 2 .
Вычислим ΔНисп.приТн.т.кип= 299 К : ΔНисп.= RT 2 · d ln p / dT = R · 2,3· 1237
ΔН исп.= 8,314 · 2,3· 1237 = 23654 Дж/ моль.
Пример 6. Температура кипения бензола при давленииp= 1,013 · 105Па равна
353,3 К. Определить давление пара бензола при 298,2 К.
Решение.Давление пара бензола приТ1= 353,3 К равноp 1= 1,013 · 105Па.
По правилу Трутона : ΔSисп.= ΔНисп./Ткип.= 88 Дж / моль·К. Отсюда определим ΔНисп.: ΔНисп.= 88 · 353,3.10- 3= 31,1 кДж / моль .
Подставим эти данные в интегральную форму уравнения Клаузиуса –Клапейрона :
ln(p 2/p 1) = ΔНисп./R( 1/Т1– 1 /T2)
ln(p 2/ 1,013 · 105) = (31100 / 8,314) ( 1/ 353,3 – 1 / 298,2 )
Откуда p 2= 1,428 · 104Па.
Пример 7. Зависимость давления насыщенного пара (в Торр) от температуры для твердого и жидкогоSO2выражается уравнениями:
lg p(тв.) = 10,5916 – 1871,2 / Т ;
lg p (ж.) = 8,3186 – 1427,7 / Т .
Рассчитать температуру и давление в тройной точке. ( 1 Торр = 1мм.рт. ст. = 133,32 Па )
Решение.Так как для равновесных фаз в тройной точке справедливо условие:
p0ж=p0тв, приравняв приведенные уравнения, вычислим температуру и давление в тройной точке: 10,5916 – 1871,2 /Т= 8,3186 – 1427,7 /Т.
Откуда Ттр.т.= 195,1 К.
lgp тр.т. = 8,3186 – 1427,7 / 195,1 = 1,0008 ;p тр.т. = 0,046 Па .
Задачи
В задачах 46 - 50 рассчитать теплоту испарения при температуре кипения, а также давление насыщенного пара при T= 298 К, если известна зависимость давления насыщенного пара от температуры.
-
№ задачи
Вещество
Зависимость давления (Па) насыщенного пара от температуры (К)
46
Фреон CCl2F2 (ж)
lg p = 34,5 - 2406,1/T - 9,26 lgT + 0,0037T
47
TiCl4 (ж)
lg p = 8,56 - 1450/T
48
Cl2 (ж)
p = 3,38.10 6 - 3,37.10 4 T + 80,11T 2
49
Br2 (ж)
lg p(Торр) = - 2210/Т - 4,08lg T + 19,82
50
Муравьиная кислота СH2O2(ж)
lg p(Торр) = 7,884 - 1860/Т
51. Определить температуру кипения хлорбензола C6H5Cl приp= 266,6 Па, если его нормальная температура кипения 405,4 К, а приp = 5,332.104Па он кипит при 382,2 К. Вычислить теплоту испаренияНисп..
52. Энтальпия плавления и плотность жидкой и твердой ртути при температуре тройной точки (234,29 К) равны соответственно 11,8 .103Дж / кг; 13,690 кг/м3; 14193 кг/м3. Вычислить изменение давления, необходимое для изменения температуры плавления ртути на 1 К.
53. Вычислить температуру плавления, давление насыщенного пара при температуре плавления, а также и теплоту плавления серебра ( Нпл)по данным зависимости давления насыщенного пара (Па) от температуры, если:
1. для твердого серебра lgp= 13,892 - 1,402.104 /T;
2. для жидкого серебра lg p= 13,347 - 1,334.104/T.
54. Рассчитать теплоту возгонки металлического цинка, если теплота плавления Нпл.при температуре тройной точки (692,7 К) равна 6,908 к Дж /моль, а зависимость теплоты испарения от температуры описывается уравнением:Нисп = 133738,66 - 9,972Т(Дж/моль)
55. Зависимость давления насыщенного пара этилового эфира (C2H5)2O от температуры представлена данными:
|
T0, C |
-10 |
0 |
10 |
20 |
30 |
|
р, Торр |
114,8 |
184,4 |
286,8 |
432,8 |
634,8 |
Построить график зависимости lg pот 1/Ти определить молярную теплоту испарения эфира (по тангенсу угла наклона прямой), а также нормальную температуру кипения.
56. Давления паров воды при 95 и 97 0С соответственно равны 84513 и 90920 Па. Вычислить теплоту испарения воды (Дж / моль) и количество теплоты, необходимое для испарения
100 кг воды.
57. Давление паров иода при 90 0С равно 3572,4 Па, а при 1000С – 6065,15 Па. Определить давление паров иода при 1150С.
58. Давление паров жидкого аммиака при (- 10 0С) равно 2,907.105Па, а при 00С –
4,293 .105Па. Определить давление паров жидкого аммиака при температуре (- 50С).
59. Давление насыщенных паров ртути при 90 0С равно 20,91 Па, а при 1000С – 36,16 Па. Определить теплоту испарения 10 кг ртути в указанном интервале температур и давление насыщенных паров ртути при 1060С.
60. Вычислить давление насыщенных паров сероуглерода при (- 10 0С), если давление пара при 00С равно 16929 Па. Удельная теплота испарения сероуглерода равна
363,3 Дж/г.
61. Температура плавления свинца равна 327,4 0 С, разность молярных объемов свинца в жидком и твердом состояниях 0,66 см3/ моль, удельная теплота плавления свинца
23,04 Дж /г. Определить изменение температуры плавления при повышении давления по сравнению с нормальным в 10 раз.
62. Температура плавления бензола 5,490С. Разность молярных объемов бензола в жидком и твердом состоянияхV= 10,28 см3/моль. При какой температуре будет плавиться бензол под давлением 1,013. 107Па? Удельная теплота плавления бензола равна 125,7 Дж/г.
63. Рассчитать разность молярных объемов для воды (V=Vж–Vтв.), если при повышении давления на 1 Па температура плавления льда понижается на 7,5.10– 8град (dT / dp). Удельная теплота плавления льда равна 333,7 Дж / г.
64. Температура плавления кадмия равна 322 0С, его удельная теплота плавления равна 57400 Дж / кг. Плотности твердого и жидкого кадмия соответственно равны 8366 и 7989 кг / м3. Вычислить, на сколько повысится температура плавления кадмия при увеличении давления от 101325 Па до 10132500 Па.
