
- •1. Структура контрольно-разрешительной системы рб.
- •2. Функции и основные направления деятельности Республиканской контрольно-аналитической лаборатории руп «цэиз».
- •3. Функции и основные направления деятельности Республиканской клинико-фармакологической лаборатории руп «цэиз».
- •4. Основные функции и направления деятельности лаборатории фармакопейного и фармацевтического анализа руп «цэиз».
- •5. Пути реализации мз рб гос. Политики в сфере обращения лс.
- •6Лс,проверяемые по всем показателям и разделам «у» «м» фс и нд производителя.
- •7.Лс проверяемые по отдельным показателям упаков. Маркир. По фс и нд производителя
- •8. Оформление результатов проверки качества лс рб в контрольно аналитической лаборатории
- •9. Этапы процедуры гос. Регистрации лс
- •10. Организация и сроки проведения экспертизы документов регистрационного досье(рд) на лс.
- •11. Структура рег досье на лс: химико-фармацевтическая часть.
- •12. Структура регистрац. Досье: клинико-фармакологическая часть.
- •13.Цели и виды сертификации лс
- •14.Схемы сертификации лс
- •15. Этапы процедуры сертификации лс
- •16. Процедуры сертификации: выдача сертификата соответствия
- •5.8 Выдача сертификата соответствия
- •17. Процедуры сертификации: инспекционный контроль за сертифицированными лс
- •18 Приостановление или отмена действия сертификата и соглашения по сертификации
- •19 Признание иностранных сертификатов соответствия
- •20. Стандартизация, объекты стандартизации, органы, осуществляющие гос.Регулирование.
- •21.Стандарт. Виды стандартов
- •22. Основные элементы стандарта
- •23. Варианты применения гос, региональных, международных стандартов
- •24. Порядок построения фарм статей на лс и фс:
- •25.Пакет документов, представляемых с проектом фс на экспертизу.
- •26.Структура пояснительной записки к проекту фс:
- •27. Порядок регистрации, обозначения и обновления фармакопейных статей
- •28. Требования, предъявляемые к контролю качества лекарственных средств на фармацевтическом производстве
- •29. Гарантии, которые дает система обеспечения качества при производстве лекарственных средств
- •30. Требования к производству лс согласно gmp
- •32.Правила оптовой и розничной реализации лс.
- •33 Отзыв лс
- •34 Сроки годности лс
- •35 Возврат лс
13.Цели и виды сертификации лс
Цели сертиф. ЛС:
–обеспеч. Насел. РБ ЛС, безопас. и ка-во ко-ых подтвержд. при сертифик.;
– повыш. кач-ва и конкурентосп. ЛС;
– защита отеч. рынка от недоброкач. и небезопас. ЛС.
Виды сертификации:
1.Обязател. сертифик. ЛС провод. на основ. актов законодат. РБ.
2. Добровол. Сертифик. ЛС провод. по инициат. заявителя.
3.Обязател. сертифик. си-м кач-ва провод. в том случае, если ее провед. предусмот. схем. сертиф..
4.Добров. сертиф. сис-м кач-ва провод. по инициат. изгот-ля.
5.Сертификацию ЛС проводят аккредитованные органы по сертификацииЛС.
6.К сертиф. допуск. ЛС, зарегистр. и разреш. к примен. в установ. Минздр. порядке.
14.Схемы сертификации лс
1.Сертиф. ЛС провод. по сх-ам, установлен. СТБ 5.1.04 и приведен. в
Табл. 1 настоящ. станд.
2.При
обязател. сертиф. выбор схемы осущест.
орган по сертиф. в зависим. от особенн.
ЛС и их производс. в соответ. с разд. 5
настоящ. стандарта.
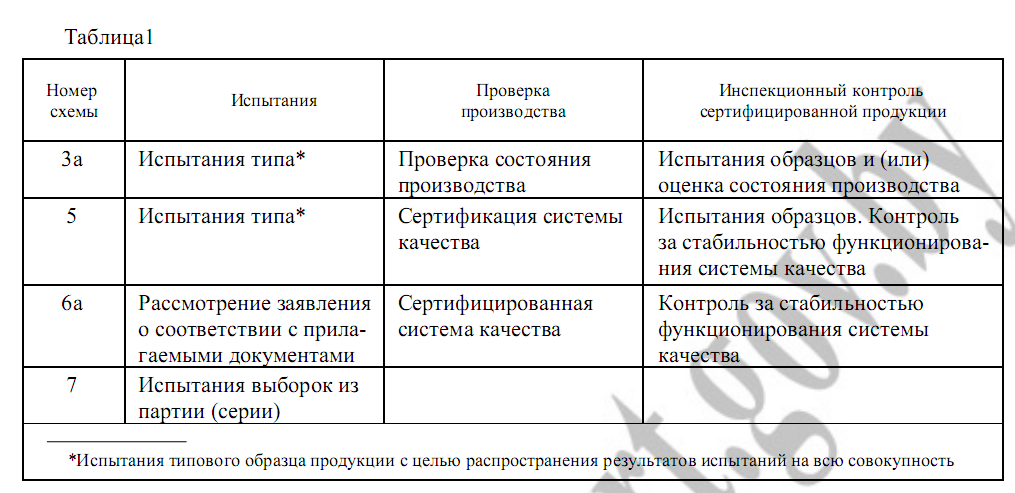
3. По схеме 3а провод. сертиф. ЛС серийн. производ. Инспекц. контроль провод. путем провед. испыт. образц. и (или) оценки соответс. производс. требов
4. По схеме 5 провод. сертиф. ЛС серийн. производ. с одноврем. сертиф. си-мы кач-ва. Инспекц. контроль провод. путем провед. испыт. образц. и контроля за стабильн. функционир. си-мы кач-ва.
5. По схеме 6а провод. сертиф. ЛС серийн. производ. с сертифицир. сис-ой кач-ва. Инспекц. контр. провод. путем провед. контр. за стабильн.функционир. сис-мы кач-ва.
6. По схеме 7 провод. сертиф. партии (серии) ЛС.
7. Сертиф. ЛС провод. на соответ. требов. фармакоп., времен. Фармакоп. статей или др. действующ. НД на ЛС.
8. Сертиф. импорт. ЛС провод. на соответс. требов. НД, разрешен. Минздр.к использ. при контроле кач-ва импорт. ЛС.
9. Орган по сертиф. ЛС несет ответствен. за соблюд. конфиденц. Информ., кроме случаев, когда ЛС представ. опасн. для жизни, здоровья людей и окруж. среды. К таким ЛС должны быть приняты меры, предусмотр. законодат. РБ
10.Расходы по провед. работ по сертиф. ЛС оплачивает заявитель на договорной основе.
15. Этапы процедуры сертификации лс
– подачу заявки на сертиф. и представ. материал., прилаг. к ней;
– анализ заявки на правильн. заполн. и представлен. документов на достаточн.;
– принят. реш. по заявке, в том числе выбор схемы сертиф. и аккредитов. испытат. лаборат. для провед. сертификац. испыт.;
– анализ документ. (нормативной, технологич., подтвержд. кач-во) на ЛС;
– идентифик. ЛС и отбор образц.;
– испыт. образц.ЛС в аккредитован. испытат. лаборатор. (центрах);
– оценку соответс. производ. требован. или сертификац. сис-мы кач-ва (если это предусмотр. схемой сертифик.);
– анализ результ. испыт.и принятие решен. о возможн. выдачи сертифик.;
– выдачу и регистр. сертифик.;
– разработку программы инспекционного контроля;
– инспекц. контроль за сертифициров. ЛС, стабильн. производ. и сис-ой
кач-ва изготов.;
– корректир. меропр.при наруш. соответс. ЛС установлен. требов. и
неправил. примен. знака соответс.;
– подготов. Информ.о результ. сертифик.;
– рассмотр. апелляций.
Каждая процедура сертиф. ЛС долж.быть документ. оформлена.
