
- •Занятие 13
- •Цель занятия
- •3. Гидроксид алюминия является лёгким аморфным осадком. Его оптимальная масса, как осаждаемой формы, при гравиметрическом определении составляет примерно:
- •4. При проведении гравиметрических определений методом осаждения навеску исходного вещества растворяют в воде (или другом растворителе) в таком соотношении, чтобы получился примерно:
- •5. Что из перечисленного неверно?
- •Предварительные расчёты
- •Занятие 14
- •Цель занятия
- •Результаты, полученные студентами первой группы
- •Занятие 15
- •Занятие 16
- •Цель занятия
- •2. Обратное титрование применяют, если:
- •3. В процессе косвенного титрования:
- •4. Согласно методике анализа Вам необходимо добавить к анализируемому раствору 10,00 мл стандартного раствора титранта. Какой мерной посудой Вы воспользуетесь?
- •5. Что из перечисленного неверно?
- •1. Проверка вместимости мерной колбы
- •2. Проверка вместимости пипетки
- •3. Проверка вместимости бюретки
- •Проверка вместимости бюретки
- •4. Определение объёма капли
- •Занятие 17
- •Цель занятия
- •9. Какие из перечисленных ниже индикаторов в водном растворе, имеющем рН 2, будут окрашены в красный цвет?
- •10. К 10 мл 0,1 м раствора вещества 0,1 моль/л добавляют 1 каплю 1% этанольного раствора фенолфталеина. В растворах каких веществ при этом произойдёт появление окраски?
- •1. Приготовление и стандартизация 0,1 м hCl
- •2. Приготовление и стандартизация 0,1 м koh
- •Занятие 18
- •Цель занятия
- •10. Что из перечисленного ниже неверно?
- •Цель занятия
- •Цель занятия
- •Занятие 21
- •Цель занятия
- •1. Приготовление и стандартизация 0,05 м эдта
- •2. Комплексонометрическое определение сульфата цинка
- •3. Комплексонометрическое определение хлорида кальция
- •Занятие 22
- •Цель занятия
- •1. Что из перечисленного верно?
- •1. Стандартизация 0,1м AgNo3
- •2. Аргентометрическое определение ki
- •Занятие 23
- •Цель занятия
- •3. Какая из перечисленных ниже формул принадлежит n-фенилантраниловой кислоте?
- •5. Редуктор Джонса:
- •10. Реактив к.Фишера представляет собой смесь:
- •1. Стандартизация раствора тиосульфата натрия
- •2. Иодометрическое определение пероксида водорода
- •Цель занятия
- •1. Какие из веществ, формулы которых приведены ниже, могут быть определены методом нитритометрического титрования на основе реакции диазотирования?
- •2. Что из перечисленного ниже верно?
- •1. Приготовление и стандартизация 0,1 м NaNo2
- •2. Нитритометрическое определение стрептоцида
- •Занятие 25
- •Цель занятия
- •1. Стандартизация 0,05 м 1/5kMnO4
- •2. Перманганатометрическое определение пероксида водорода
- •Занятие 26
- •Цель занятия
Занятие 22



Цель занятия
Знать:
общую характеристику, титранты и стандартные вещества, условия выполнения и практическое применение меркуриметрического титрования;
общую характеристику и классификацию методов осадительного титрования, требования к используемым реакциям;
алгоритм построения кривой аргентометрического титрования; факторы, влияющие на величину скачка титрования;
способы обнаружения конечной точки титрования в аргентометрии, принцип действия адсорбционных индикаторов;
стандартные растворы и стандартные вещества, используемые в аргентометрическом титровании и его практическое применение;
общую характеристику, титранты и стандартные вещества, условия выполнения и практическое применение меркурометрического титрования.
Уметь:
выполнять меркуриметрическое определение хлорида натрия;
проводить стандартизацию раствора нитрата серебра;
выполнять аргентометрическое определение иодида калия.
Меркуриметрическое титрование. Принцип метода. Условия проведения титрования. Титранты и стандартные вещества. Обнаружение конечной точки титрования. Практическое применение.
Общая характеристика и классификация методов осадительного титрования. Требования к используемым реакциям.
Общая характеристика аргентометрического титрования, его основные преимущества и недостатки.
Типичная кривая аргентометрического титрования. Факторы, влияющие на величину скачка титрования в аргентометрии.
Способы обнаружения конечной точки титрования в аргентометрии: метод Мора.
Способы обнаружения конечной точки титрования в аргентометрии: метод Фаянса. Понятие об адсорбционных индикаторах.
Способы обнаружения конечной точки титрования в аргентометрии: метод Фольгарда. Тиоцианатометрическое титрование.
Титранты и стандартные вещества, используемые в аргентометрическом титровании. Практическое применение аргентометрического титрования.
Меркурометрическое титрование. Принцип метода. Условия проведения титрования. Титранты и стандартные вещества. Обнаружение конечной точки титрования. Практическое применение.

Существует несколько методик меркуриметрического определения иодидов. В одной из них обнаружение конечной точки титрования проводят с помощью дифенилкарбазида, в другой титрование ведут до появления оранжево-красной суспензии HgI2, в третьей конечную точку титрования устанавливают по исчезновению синей окраски иодкрахмального комплекса. Объясните принцип обнаружения конечной точки титрования в перечисленных методиках. Чему будет равен фактор эквивалентности для KI при его меркуриметрическом определении по первой и по второй методике?
Часто для обнаружения конечной точки меркуриметрического титрования используется смешанный индикатор, состоящий из дифенилкарбазона и бромфенолового синего. Объясните принцип действия такого индикатора.
Почему аргентометрическое титрование не проводят в сильнощелочной среде? Рассчитайте, при каком минимальном значении рН при аргентометрическом титровании NaCl в точке эквивалентности начнёт выпадать осадок Ag2O (KS = [Ag+][OH-] = 1,610-8).
Должны ли отличаться концентрации хромат-ионов, используемых для обнаружения конечной точки титрования хлорид- и бромид-ионов?
Почему K2CrO4 не используется в качестве индикатора при аргентометрическом определения иодидов, а метод Фаянса, наоборот, является самым оптимальным вариантом обнаружения конечной точки титрования данных ионов?
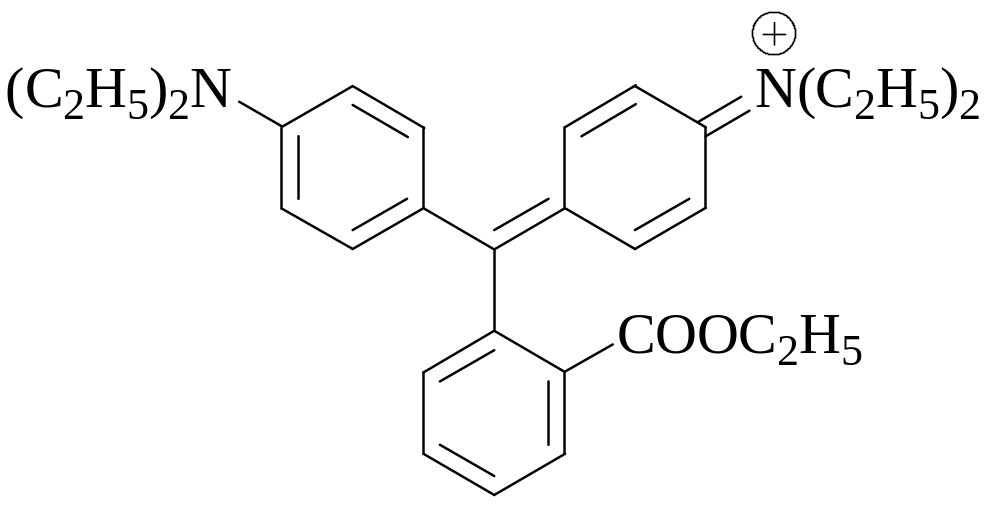
Для обнаружения конечной точки аргентометрического титрования в качестве адсорбционных индикаторов используют не только флуоресцеин и его галогенопроизводные, но и другие вещества, например родамин 6Ж. Почему данный индикатор более удобно использовать не в случае титрования раствором AgNO3, а, наоборот, в случае титрования раствора AgNO3.Почему при аргентометрическом титровании с адсорбционными индикаторами стремятся получить осадок с мелкими частицами, в то время как при гравиметрическом определении - крупнокристаллический осадок?
Предложите алгоритм количественного анализа раствора, в состав которого входят иодид калия, хлорид калия и хлорид кальция.
Приведите примеры использования аргентометрического титрования для определения органических веществ, образующих малорастворимые соли с катионом серебра.
Приготовление стандартного раствора Hg2(NO3)2 проводится следующим образом. Рассчитанную навеску Hg2(NO3)2 растворяют при слабом нагревании в 0,2 М HNO3. Затем к раствору добавляют немного металлической ртути, хорошо взбалтывают, оставляют на сутки и лишь после этого подвергают стандартизации. Объясните, почему растворение Hg2(NO3)2 проводят не в воде, а в растворе HNO3. Зачем к приготовленному раствору добавляют металлическую ртуть? Нужно ли добавлять ртуть к стандартному раствору меркуриметрического титрования?
