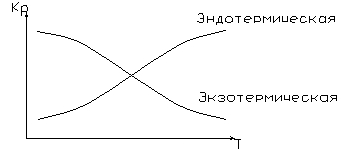- •1)Основные понятия и законы химии
- •2) Количество вещества — величина, характеризующая количество однотипных структурных единиц, содержащихся в веществе.
- •Химические свойства солей:
- •8) Правила заполнения электронами атомных орбиталей (принцип минимальной энергии, правило Клечковского, правила Паули и Гунда).
- •9)Периодический закон д.И. Менделеева. Периодическая таблица (периоды и группы).
- •12) Термодинамические системы: открытые, закрытые, изолированные; гомогенные, гетерогенные. Параметры системы.
- •Термодинамические параметры:
- •13) Функции состояния системы: внутренняя энергия, энтальпия, энтропия, химический потенциал, изобарно- и изохорно-изотермический потенциал. Изобарные, изохорные, изотермические процессы.
- •15) Экзотермическая реакция — химическая реакция, сопровождающаяся выделением теплоты.
- •Условия, влияющие на скорость химических реакций
- •19) Понятие раствора. Способы выражения состава раствора (массовая доля, молярность, моляльность, нормальность).
- •20) Идеальные растворы. Растворы неэлектролитов: понятия диффузии и осмоса. Разбавленные и концентрированные растворы; насыщенный раствор.
15) Экзотермическая реакция — химическая реакция, сопровождающаяся выделением теплоты.
Эндотерми́ческие
реа́кции (от др.-греч. ἔνδον —
внутри и θέρμη —
тепло) — химические реакции,
сопровождающиеся поглощением теплоты.
Для эндотермических реакций
изменение энтальпии и внутренней
энергии имеют
положительные значения (![]() ,
, ![]() ),
таким образом, продукты реакции содержат
больше энергии, чем исходные компоненты.
),
таким образом, продукты реакции содержат
больше энергии, чем исходные компоненты.
К эндотермическим реакциям относятся:
реакции восстановления металлов из оксидов,
электролиза (поглощается электрическая энергия),
электролитической диссоциации (например, растворение солей в воде),
ионизации,
фотосинтеза.
Пользуясь табличными значениями
![]()
![]() и
и
![]() ,
можно рассчитать энтальпии различных
химических процессов и фазовых
превращений. Основанием для таких
расчетов является закон Гесса,
сформулированный петербургским
профессором Г.
И. Гессом (1841 г.): «Тепловой
эффект (энтальпия) процесса зависит
только от начального и конечного
состояния и не зависит от пути перехода
его из одного состояния в другое».
,
можно рассчитать энтальпии различных
химических процессов и фазовых
превращений. Основанием для таких
расчетов является закон Гесса,
сформулированный петербургским
профессором Г.
И. Гессом (1841 г.): «Тепловой
эффект (энтальпия) процесса зависит
только от начального и конечного
состояния и не зависит от пути перехода
его из одного состояния в другое».
Под стандартной теплотой образования понимают тепловой эффект реакции образования одного моля вещества из простых веществ, его составляющих, находящихся в устойчивых стандартных состояниях.
16) Скорость химической реакции можно выразить как изменение количества вещества (n, по модулю) в единицу времени (t) – сравните скорость движущегося тела в физике как изменение координат в единицу времени: υ = Δx/Δt. Чтобы скорость не зависела от объема сосуда, в котором протекает реакция, делим выражение на объем реагирующих веществ (v), т.е. получаем изменение количества вещества в единицу времени в единице объема, или изменение концентрации одного из веществ в единицу времени:
n2 – n1 Δn Δс υ = –––––––––– = –––––––– = –––––––– (1) (t2 – t1) • v Δt • v Δt
где c = n/v – концентрация вещества
Условия, влияющие на скорость химических реакций
1) Скорость реакции зависит от природы реагирующих веществ. Проще говоря, разные вещества реагируют с разной скоростью. Например, цинк бурно реагирует с соляной кислотой, а железо довольно медленно.
2) Скорость реакции тем больше, чем выше концентрация веществ. С сильно разбавленной кислотой цинк будет реагировать значительно дольше.
3) Скорость реакции значительно повышается с повышением температуры. Например, для горения топлива необходимо его поджечь, т.е. повысить температуру. Для многих реакций повышение температуры на 10° C сопровождается увеличением скорости в 2-4 раза.
4) Скорость гетерогенных реакций увеличивается с увеличением поверхности реагирующих веществ. Твердые вещества для этого обычно измельчают. Например, чтобы порошки железа и серы при нагревании вступили в реакцию, железо должно быть в виде мелких опилок.
Гомогенные реакции протекают в пределах одной фазы, например, в смеси газов или в растворе.
Гетерогенные реакции протекают на границе раздела фаз, например, твердой и жидкой, твердой и газообразной.
Зако́н де́йствующих масс устанавливает соотношение между массами реагирующих веществ в химических реакциях при равновесии, а также зависимость скорости химической реакции от концентрации исходных веществ.
Константа скорости реакции (удельная скорость реакции) — коэффициент пропорциональности в кинетическом уравнении.
Физический смысл константы скорости реакции k следует из уравнения закона действующих масс: k численно равна скорости реакции при концентрации каждого из реагирующих веществ равной 1 моль/л.
МОЛЕКУЛЯРНОСТЬ РЕАКЦИИ, число частиц реагентов, взаимодействующих друг с другом в одной элементарной (простой) р-ции и превращающихся в продукты.
Правило Вант-Гоффа — При повышении температуры на каждые 10 градусов константа скорости гомогенной элементарной реакции увеличивается в два — четыре раза.
17) Энергия активации (активированный комплекс, энергетические диаграммы экзо- и эндотермических реакций, влияние катализаторов, уравнение Аррениуса). Катализ (гомогенный и гетерогенный; ферменты, промоторы, ингибиторы).
Энергия активации, разность между значениями средней энергии частиц (молекул, радикалов, ионов и др.), вступающих в элементарный акт химической реакции, и средней энергии всех частиц, находящихся в реагирующей системе.
Константа скорости реакции k связана с Энергия активации (Е) уравнением Аррениуса: k = koe-E/RT где R - газовая постоянная, Т - абсолютная температура в К, ko - постоянная, называемая предэкспоненциальным множителем константы скорости.
Активированный комплекс интерпретируется как момент дискретно-ступенчатой непрерывности превращения вещества. Поэтому, строго говоря, активированный комплекс – не частица, а динамическое состояние.
Катализ – явление изменения скорости химической реакции в присутствии веществ, состояние и количество которых после реакции остаются неизменными.
Если катализатор и реагирующие вещества находятся в одном агрегатном состоянии, обычно газообразном или жидком, то катализ называется гомогенным. В роли катализаторов в гомогенном катализе часто выступают растворы кислот, оснований, солей d-элементов, растворители. Катализ является гетерогенным, если катализатор и реагирующие вещества находятся в разных агрегатных состояниях или образуют самостоятельные фазы. В роли катализаторов в этом случае чаще всего выступают твердые вещества, обычно d-элементы или их соединения.
ФЕРМЕНТЫ , белки, выполняющие роль катализаторов в живых организмах. Осн. ф-ции ферментов- ускорять превращение в-в, поступающих в организм и образующихся при метаболизме (для обновления клеточных структур, для обеспечения его энергией и др.), а также регулировать биохим. процессы (напр., реализацию ге-нетич. информации), в т. ч. в ответ на изменяющиеся условия.
ПРОМОТОРЫ, в-ва, добавление к-рых в небольших кол-вах к катализаторам увеличивает их активность, селективность или стабильность. Если в-во добавляют к катализатору в больших кол-вах или если оно само по себе каталитически активно, то такой катализатор наз. смешанным.
ИНГИБИТОРЫ, в-ва, тормозящие хим. р-ции. Ингибирование характерно для каталитич и цепных р-ций, к-рые протекают с участием активных центров или активных частиц. Тормозящее действие обусловлено тем, что ингибитор блокирует активные центры катализатора или реагирует с активными частицами с образованием малоактивных радикалов, не способных продолжать цепь.
18) Обратимые и необратимые реакции. Химическое равновесие; константа равновесия, влияние температуры на константу равновесия. Принцип Ле-Шателье.
Обратимые реакции — химические реакции, протекающие одновременно в двух противоположных направлениях (прямом и обратном), например:
3H2 + N2 ⇌ 2NH3.
Необратимые реакции — реакции, при которых взятые вещества нацело превращаются в продукты реакции, не реагирующие между собой при данных условиях, например, разложениевзрывчатых веществ, горение углеводородов, образование малодиссоциирующих соединений, выпадение осадка, образование газообразных веществ.
Ba(ClO2)2 + H2SO4 → 2HClO2 + BaSO4↓
NaHCO3 + CH3COOH → CH3COONa + H2O + CO2↑
Принцип Ле-Шателье - внешнее воздействие на систему, находящуюся в состоянии равновесия, приводит к смещению этого равновесия в направлении, при котором эффект произведенного воздействия ослабляется.
Увеличение давления смещает равновесие в сторону реакции, ведущей к уменьшению объема.
Повышение температуры смещает равновесие в сторону эндотермической реакции.
Увеличение концентрации исходных веществ и удаление продуктов из сферы реакции смещают равновесие в строну прямой реакции.
Катализаторы не влияют на положение равновесия.
При равенстве энтальпийного и энтропийного факторов ΔН = ТΔS ΔG = 0, что является термодинамическим условием химического равновесия.
Количественной характеристикой химического равновесия является константа равновесия, которая может быть выражена через равновесные концентрации Сi, парциальные давления Pi или мольные доли Xi реагирующих веществ. Для некоторой реакции

соответствующие константы равновесия выражаются следующим образом:
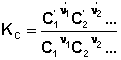 (1)
(1) 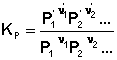 (2)
(2)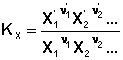 (3)
(3)
Для
эндотермических реакций (![]() )
значение константы равновесия
)
значение константы равновесия ![]() возрастает
с повышением температуры, а для
экзотермической реакции (
возрастает
с повышением температуры, а для
экзотермической реакции (![]() )
– понижается (рис.1.)
)
– понижается (рис.1.)