
- •Билет №1
- •Билет №2
- •Физ свва
- •400 Кг/м³ (жидкий).
- •Билет №3
- •Билет №4
- •Билет№5
- •Основные промышленные группы 0%9f%d0%be%d0%bb%d0%b8%d0%bc%d0%b5%d1%80"полимеров, синтезируемых поликонденсацией
- •Билет №6
- •Билет №7
- •Реакции, которые протекают только в одном направлении и завершаются полным превращением исходных реагирующих веществ в конечные вещества, называются необратимыми.
- •Химические свойства
- •Химические свойства металлов
- •Билет №8
- •Физические свойства
- •Применение
Химические свойства
Для ацетилена (этина) характерны реакции присоединения:
HC≡CH + Cl2 -> СlСН=СНСl
В лаборатории ацетилен получают действием воды на 0%9A%D0%B0%D1%80%D0%B1%D0%B8%D0%B4_%D0%BA%D0%B0%D0%BB%D1%8C%D1%86%D0%B8%D1%8F"карбид кальция 6ei5LGn165M"смHYPERLINK "http://www.youtube.com/watch?v=6ei5LGn165M". видео данного процесса (0%92%D1%91%D0%BB%D0%B5%D1%80,_%D0%A4%D1%80%D0%B8%D0%B4%D1%80%D0%B8%D1%85"Ф. HYPERLINK "http://ru.wikipedia.org/wiki/%D0%92%D1%91%D0%BB%D0%B5%D1%80,_%D0%A4%D1%80%D0%B8%D0%B4%D1%80%D0%B8%D1%85"Вёлер, 1862 г.),
CaC2+ 2 Н2О = С2Н2↑ + Са(ОН)2
а также при 0%94%D0%B5%D0%B3%D0%B8%D0%B4%D1%80%D0%B8%D1%80%D0%BE%D0%B2%D0%B0%D0%BD%D0%B8%D0%B5"дегидрировании двух молекул 0%9C%D0%B5%D1%82%D0%B0%D0%BD"метана при температуре свыше 1400° Цельсия:
2СН4 = С2Н2↑ + Н2↑
Ацетилен используют:
для 0%A1%D0%B2%D0%B0%D1%80%D0%BA%D0%B0"сварки и резки 0%9C%D0%B5%D1%82%D0%B0%D0%BB%D0%BB"металлов,
как источник очень яркого, белого света в автономных светильниках
3
Химические свойства металлов
Для металлов характерно свойство восстановления. Реакции с галогенами и кислородом воздуха протекают с различными скоростями и при различных температурах с разными металлами. Так, щелочные металлы легко окисляются кислородом воздуха и взаимодействуют с простыми веществами, железо и медь взаимодействуют с простыми веществами только при нагревании, золото и платиновые металлы не окисляются вообще. Многие металлы образуют на поверхности оксидную пленку, которая защищает их от дальнейшего окисления.



Менее энергично металлы взаимодействуют с серой:


Трудно вступают в реакцию с азотом и фосфором:
 (нитрид
магния)
(нитрид
магния)
 (фосфид
кальция)
(фосфид
кальция)
Активные металлы взаимодействуют с водородом:
 (гидрид
кальция)
(гидрид
кальция)
Взаимодействие с водой:
Активные металлы (щелочные металлы) взаимодействуют с водой при обычных условиях с образованием гидроксидов и выделением водорода:


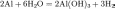
Билет №8
1
Реакция ионного обмена — одна из видов 0%A5%D0%B8%D0%BC%D0%B8%D1%87%D0%B5%D1%81%D0%BA%D0%B0%D1%8F_%D1%80%D0%B5%D0%B0%D0%BA%D1%86%D0%B8%D1%8F"химической реакции, характеризующаяся выделением в продукты реакции воды,0%93%D0%B0%D0%B7"газа или 0%A1%D0%BE%D0%BB%D0%B8"осадка.
Реакцию обмена в растворе принято изображать тремя уравнениями: молекулярным, полным ионным и сокращённым ионным. В ионном уравнении слабые электролиты, газы и малорастворимые вещества изображают молекулярными формулами.
Na2CO3 + H2SO4 → Na2SO4 + CO2↑ +H2O
2Na+ + CO32- + 2H+ + SO42- → 2Na+ + SO42- + CO2↑ + H2O
CO32- + 2H+ → CO2↑ + H2O
Условия необратимости реакций ионного обмена
1. Если образуется осадок (¯) (1_6-4.html"смотри таблицу растворимости)
Pb(NO3)2 + 2KI ® PbI2¯ + 2KNO3
Pb2+ + 2I- ® PbI2¯
2. Если выделяется газ ()
Na2CO3 + H2SO4 ® Na2SO4 + H2O + CO2
CO32- + 2H+ ® H2O + CO2
3. Если образуется малодиссоциированное вещество (H2O)
Ca(OH)2 + 2HNO3 ® Ca(NO3)2 + 2H2O
H+ + OH- ® H2O
4. Если образуются комплексные соединения (малодиссоциированные комплексные ионы)
CuSO4 • 5H2O + 4NH3 ® [Cu(NH3)4]SO4 + 5H2O
Cu2+ + 4NH3 ® [Cu(NH3)4]2+
В тех случаях, когда нет ионов, которые могут связываться между собой с образованием осадка, газа, малодиссоциированных соединений (H2O) или комплексных ионов реакции обмена обратимы «.
2
Арены или ароматические углеводороды – это соединения, молекулы которых содержат устойчивые циклические группы атомов (бензольные ядра) с замкнутой системой сопряженных связей.
Простейшие представители (одноядерные арены):
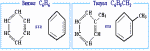
Многоядерные арены: нафталин С10Н8, антрацен С14Н10 и др.

Термин "ароматические соединения" возник давно в связи с тем, что некоторые представители этого ряда веществ имеют приятный запах. Однако в настоящее время в понятие "ароматичность" вкладывается совершенно иной смысл.
Бензо́л (0%A3%D0%B3%D0%BB%D0%B5%D1%80%D0%BE%D0%B4"C60%92%D0%BE%D0%B4%D0%BE%D1%80%D0%BE%D0%B4"H6, PhH) — 0%9E%D1%80%D0%B3%D0%B0%D0%BD%D0%B8%D1%87%D0%B5%D1%81%D0%BA%D0%B8%D0%B5_%D1%81%D0%BE%D0%B5%D0%B4%D0%B8%D0%BD%D0%B5%D0%BD%D0%B8%D1%8F"органическое химическое соединение, 0%A6%D0%B2%D0%B5%D1%82"бесцветная 0%96%D0%B8%D0%B4%D0%BA%D0%BE%D1%81%D1%82%D1%8C"жидкость с приятным сладковатым0%97%D0%B0%D0%BF%D0%B0%D1%85"запахом. Простейший 0%90%D1%80%D0%B5%D0%BD%D1%8B"ароматический углеводород. Бензол входит в состав 0%91%D0%B5%D0%BD%D0%B7%D0%B8%D0%BD"бензина, широко применяется в0%9F%D1%80%D0%BE%D0%BC%D1%8B%D1%88%D0%BB%D0%B5%D0%BD%D0%BD%D0%BE%D1%81%D1%82%D1%8C"промышленности, является исходным сырьём для производства 0%9B%D0%B5%D0%BA%D0%B0%D1%80%D1%81%D1%82%D0%B2%D0%BE"лекарств, различных 0%9F%D0%BB%D0%B0%D1%81%D1%82%D0%BC%D0%B0%D1%81%D1%81%D0%B0"пластмасс, синтетической 0%A0%D0%B5%D0%B7%D0%B8%D0%BD%D0%B0"резины, красителей. Хотя бензол входит в состав 0%9D%D0%B5%D1%84%D1%82%D1%8C"сырой нефти, в промышленных масштабах он синтезируется из других её компонентов. Токсичен,0%9A%D0%B0%D0%BD%D1%86%D0%B5%D1%80%D0%BE%D0%B3%D0%B5%D0%BD"канцерогенен.
