
- •2. Воспламенение
- •2.1. Адиабатические химические превращения
- •2.2. Два типа воспламенения
- •2.3. Стационарная теория теплового воспламенения
- •2.4. Нестационарная теория теплового взрыва
- •2.5. Тепловой взрыв в динамических условиях /4/
- •2.6. Вынужденное воспламенение (зажигание)
- •2.7. Тепловая теория зажигания
- •Процесс горения
- •Диффузионное и кинетическое горение
- •Диффузионное пламя
- •Расход воздуха на горение
- •После преобразования получим
- •Продукты сгорания. Дым
- •Определяем объем влажных продуктов сгорания метана
- •Теплота сгорания
- •Температура горения
- •Оценка пожарной опасности веществ и материалов
- •Превращение горючих веществ при нагревании
- •Теория окисления горючих веществ
- •Цепь Разветвление
- •Теория самовоспламенения
- •Температура самовоспламенения
- •Процесс возгорания и воспламенения
Лекция Горение веществ
Горением называют физико-химический процесс, для которого характерны три признака: химическое превращение, выделение тепла, излучение света. По этим признакам горение можно отличить от других явлений. Например, «горение» электрической лампочки нельзя назвать горением, хотя при этом выделяется тепло и свет. В этом явлении нет одного из признаков горения — химического процесса. Свечение нити лампочки — это накаливание ее при пропускании электрического тока.
Горение процесс сложный и состоит из нескольких стадий. Первой стадией горения является воспламенение
2. Воспламенение
2.1. Адиабатические химические превращения
Особенностью
процесса горения является своеобразный
характер
его возникновения. Последнее происходит
при известных условиях
самопроизвольно, путем резкого перехода
от медленной, почти
незаметной реакции к быстрому реагированию,
воспринимаемому как вспышка или взрыв
и характеризуемому появлением пламени.
Это
значит, что в реагирующей системе в
момент воспламенения создаются
такие условия, при которых возможно
прогрессивное ускорение
хода химических реакций. С точки зрения
химического превращения,
общим условием воспламенения является
условие
![]() >
0.
>
0.
Рассматривая закономерности химических реакций, обычно температуру считают постоянной, процесс - изотермическим, и тогда скорость химической реакции при денной температуре определяется только величиной действующих концентраций реагирующих веществ. В ходе превращения их значения прогрессивно уменьшаются, и поэтому для обычной изотермической реакции всегда < 0.
Это означает, что любая обычная изотермическая реакция является всегда реакцией не ускоряющейся и, следовательно, невзрывной.
Существенно новые и практически наиболее важные свойства реакций возникают в случав, когда в силу экзотермичности превращения и малого теплоотвода температура в системе прогрессивно возрастает по мере хода реакции, поскольку при расходовании вещества происходит соответствующее выделение тепла. Последнее частично теряется в окружающем пространстве, в частично идет на разогрев системы.
Между величиной Т и величиной С всегда может быть установлена связь, конкретная форма которой зависит от формы теплоотвода, состава смеси и прочего. В простейшем предельном случае протекания процесса в адиабатических условиях такая связь устанавливается следующим образом. Если Со - начальная молярная концентрация вещества (находящегося в недостатке), Сυ - теплоемкость продуктов горения при постоянном объеме в интервале от То до Т, Q- тепловой эффект реакция, то
![]()
![]() =
=
![]() .
.
![]() ,
=1.
(2.1)
,
=1.
(2.1)
При
полном сгорании С = О, Т = Тк
и
поэтому
![]() .
.
Откуда
![]() ,
,
![]()
или
окончательно
(2.2)
C
=
![]() (2.2)
(2.2)
При
помощи выражений (2.2) или подобного ему
выражения для температуры
величину скорости реакция можно
свести
или к
функции
только Т,
или к функции только С.
Так как
![]() ,
,
тo, используя выражения (2.3), (2.8), получим
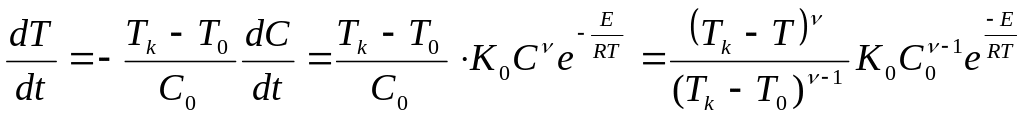
Это уравнение в конечном счете позволяет найти связь между температурой Т и временем t, а затем и изменение скорости реакции W во времени. Характер этого изменения сильно отличается от характера изменения скорости реакции W- для изотермической реакции (рис.2.1).
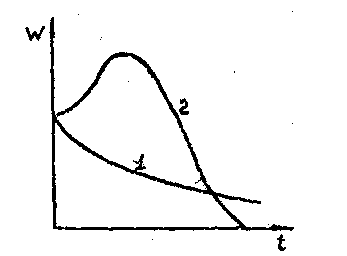
.2.1. Изменение скорости реакции при процессеs I - изотермическом; 2 - адиабатическом
Скорость изотермической реакция изменяется со временем и максимальна в начале процесса. Кривая 2 соответствует адиабатическим условиям и показывает с самого начала быстрый рост скорости реакции под действием возраставшей температуры, т.е. >0, в дальнейшем с некоторого момента, когда содержание реагирующего вещества уменьшается, реакция начинает замедляться, и скорость ее стремится к нулю. В этой части процесса <0. Граница перехода от взрывного процесса к невзрывному определяется, очевидно, условием = 0. Используя это условие, можно получить для адиабатических реакций общее соотношение для определения границ взрывного (самоускоряющегося) протекания адиабатических химических реакций.
Если ввести для характеристики химического состояния системы так называемую химическую переменную - безразмерную величину, характеризующую глубину протекания реакции, изменяющуюся от 0 (начало) до I (конец реакции), то скорость реакции W может быть представлена в следующем виде:
W
=
![]() ;
(2.5)
;
(2.5)
![]() ,
(2.6)
,
(2.6)
Для
адиабатического превращения можно
записать термодинамическое соотношение
![]() ,
где Q
- тепловой
эффект, отнесенный к
=
I.
Тогда
,
где Q
- тепловой
эффект, отнесенный к
=
I.
Тогда
![]() ,
,
откуда на пределе перехода к взрывному процессу следует
![]() .
.
Реакция будет ускоряющейся и, следовательно, взрывной, если
![]()
Но
![]() всегда отрицательна (скорость реакции
уменьшается с уменьшением
концентрации вещества), поэтому реакция
будет ускоряющейся,
если
всегда отрицательна (скорость реакции
уменьшается с уменьшением
концентрации вещества), поэтому реакция
будет ускоряющейся,
если
![]()
Физическое значение в том, что увеличение скорости адиабатической реакции за счет повышения температуры должно соответствующим образом компенсировать неизбежное уменьшение скорости реакции за счет уменьшения концентрации реагирующих веществ.
В обычных условиях воспламенения, когда начальная температура невелика и концентрации реагирующих веществ имеют максимальные значения, адиабатическая реакция всегда имеет взрывной характер. С этой точки зрения, адиабатическая реакция, какой бы она ни была медленной вначале, с некоторого момента станет заметной.
Характер изменения температуры, концентрации и скорости реакции показан на рисунке 2.2.
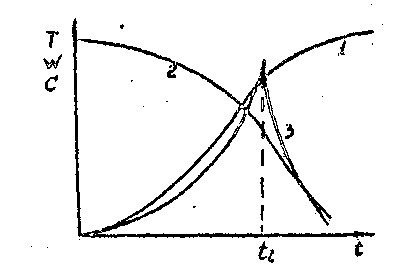
Рис.2.2. Развитие в экзотермической химической реакции во времени в адиабатических условиях: I – температура, 2 - концентрация исходного реагента; 3 - скорость реакции, ti- адиабатический индукционный период (время индукции)
Временная зависимость скорости взрывной химической реакции имеет характер, близкий к описываемому Е - функцией; она практически равна нулю вплоть до некоторого момента, затем когда полностью выгорает реагирующее вещество, скорость реакции возрастает до своего максимального значения и вновь быстро уменьшается до 0. Поэтому временную зависимость скорости реакции, в некоторых исследованиях приближенно аппроксимируют -функцией}
W(t)= Ao(t-ti),
где
нормировочная константе A0
определена
из условия расходования в реакции всего
горючего вещества
![]() ,
а
время адиабатической индукции ti
можно
определить как время, в течение которого
скорость реакции достигает своего
максимума.
,
а
время адиабатической индукции ti
можно
определить как время, в течение которого
скорость реакции достигает своего
максимума.
