- •1 Охрана труда при выполнении лабораторных работ в лаборатории № 324 3
- •2 Лабораторные работы по курсу «Водоподготовка и водно-химические режимы тэс и аэс». Часть 1. Водоподготовка 12
- •1 Охрана труда при выполнении лабораторных работ в лаборатории № 324
- •1.1 Общие требования
- •1.2 Характеристика основных химических веществ, применяемых в лаборатории № 324
- •1.2.1 Аммиак водный технический nh4oh.
- •1.2.2 Едкий натр NaOh.
- •1.2.3 Серная кислота h2so4.
- •1.2.4 Соляная кислота.
- •1.2.5 Полиакриламид паа.
- •1.2.6 Трилон б.
- •1.2.7 Гидразингидрат n2h4h2o.
- •1.3 Хранение кислот и щелочей.
- •1.4 Требования по охране труда в аварийных ситуациях
- •1.5 Необходимые реагенты и их приготовление
- •1.5.1 Приготовление растворов кислот и щелочей
- •1.5.2 Приготовление раствора трилона б
- •1.5.3 Приготовление аммиачного буферного раствора
- •1.5.4 Приготовление раствора натрия сернистого
- •1.5.5 Расчет и приготовление рабочего раствора коагулянта оксихлорида алюминия(оха)
- •1.5.6 Приготовление растворов индикаторов
- •Выполнение определения.
- •Лабораторная работа № 2 Определение сухого и плотного остатков воды
- •Общие сведения.
- •Выполнение определения.
- •Вычисление результатов.
- •Лабораторная работа № 3 Определение кислотности воды
- •Общие сведения.
- •Необходимые реактивы
- •Выполнение определения
- •Вычисление результатов.
- •Лабораторная работа № 4 Определение щелочности природной и технической воды
- •Общие сведения
- •Щелочные компоненты различных вод
- •Необходимые реактивы
- •Выполнение определения
- •Лабораторная работа № 5 Определение общей жесткости воды трилонометрическим методом
- •Общие сведения
- •Сущность метода
- •Необходимые реактивы
- •Выполнение определения.
- •Вычисление результатов
- •Контрольные вопросы:
- •Лабораторная работа № 6 Определение кальциевой жесткости воды трилонометрическим методом
- •Общие сведения
- •Необходимые реактивы:
- •Выполнение определения
- •Вычисление результатов
- •Лабораторная работа № 7 Определение оптимальной дозы коагулянта при обработке воды
- •Общие сведения
- •Выполнение определения
- •Результаты опыта
- •Лабораторная работа № 8 Умягчение воды методом осаждения накипеобразователей.
- •Общие сведения
- •Определение необходимого расхода NaOh
- •Выполнение определения
- •Лабораторная работа № 9 Умягчение воды методом натрий-катионирования
- •Общие сведения
- •Выполнение работы
- •Процесс регенерации фильтра
- •Лабораторная работа № 10 Обессоливание воды методом ионного обмена.
- •Общие сведения
- •Лабораторные работы по курсу «Водоподготовка и водно-химические режимы тэс и аэс». Часть II. Водно-химические режимы тэс и аэс
- •Лабораторная работа № 1 Определение величины присоса охлаждающей воды в конденсатор турбины
- •Общие сведения.
- •Выполнение работы
- •Выполнение определения
- •Лабораторная работа № 2 Определение концентрации свободной угольной кислоты в воде
- •Общие сведения
- •Выполнение работы
- •Лабораторная работа № 3 Контроль состояния проточной части турбин и поверхностей нагрева парогенераторов.
- •Общие сведения
- •Контроль за состоянием проточной части турбины
- •Контроль состояния поверхностей нагрева парогенераторов
- •Лабораторная работа № 4 Определение степени загрязнённости экранных труб котла
- •Общие сведения
- •Методика определения
- •Лабораторная работа № 5 Определение скорости коррозии металла энергетического оборудования.
- •Общие сведения
- •Лабораторная работа № 6 Сепаратор spiroventair&dirt
- •Общие сведения
- •Порядок выполнения работы
- •Лабораторная работа № 7 Водно-химический режим энергоблока с котлом барабанного типа
- •Общие сведения.
- •Выполнение работы
Лабораторная работа № 10 Обессоливание воды методом ионного обмена.
Цель работы: Ознакомление с процессом обессоливания воды путем eё последовательной обработки на водород – катионитовых и ОН–ионитовых фильтрах. Изучение свойств водород-катионированной и обессоленной воды.
Общие сведения
Обессоливание воды предполагает удаление из нее всех катионов и анионов растворенных солей.
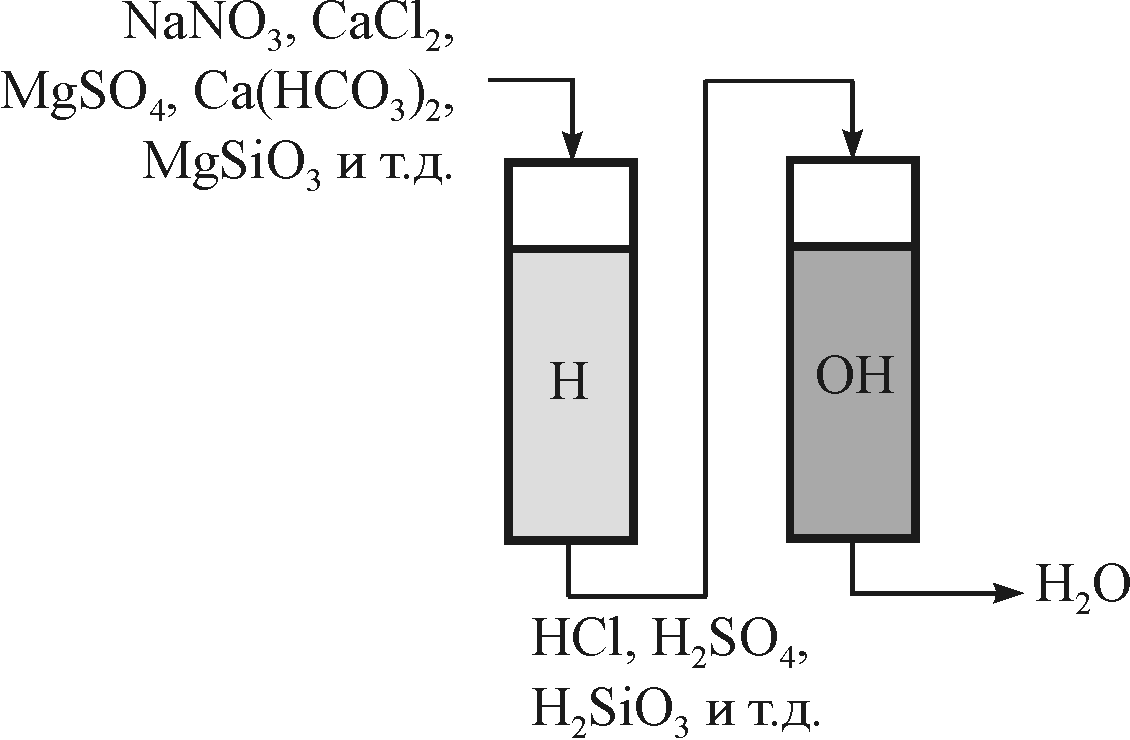
Рисунок 1.2 - Ступень химического обессоливания воды |
При водород – катионировании происходит обмен всех растворенных в воде катионов (Na+, Ca2+, Mg2+) на обменный катион H+ по приведенным реакциям:
2Н2О
Са(НСО3)+2НRСаR2+2Н2СО3 2СО2 (1.41)
2Н2О
Mg(НСО3)2+2НRMgR2+2Н2СО3 (1.42)
2СО2
СаСl2 + 2HR CaR2 + 2HCl (1.43)
MgSO4 + 2HR MgR2 + H2SO4 (1.44)
Анализ приведенных реакций показывает,
что за счет разрушения бикарбонат иона
, который при водород-катионировании
переходит в свободную углекислоту СО2,
изменяется не только катионный, но и
анионный состав воды. Снижается общая
жесткость воды, полностью удаляется
карбонатная жесткость. Присутствующие
в исходной воде сульфаты, хлориды,
силикаты и нитраты кальция, магния,
натрия преобразуются в минеральные
кислоты (серную, соляную, кремниевую,
азотную). Вода приобретает кислую
реакцию. Максимальная величина кислотности
эквивалентна суммарной концентрации
всех анионов сильных кислот в исходной
воде (![]() ,
,
![]() ,
,
![]() ).
).
Величина кислотности водород-катионированной
воды непостоянна. Она снижается в
процессе фильтрования по мере истощения
катионита. Для того, чтобы получить
обессоленную воду, необходимо предотвратить
поступление в фильтрат катионов
![]() .
Поэтому водород – катионитные фильтры
в схемах обессоливания отключают на
регенерацию по проскоку в фильтрат
катионов
.
Косвенным показателем проскока катионов
служит снижение кислотности. Процесс
восстановления водород – катионитного
фильтра аналогичен процессу восстановления
натрий – катионитного фильтра (см.
лабораторную работу № 9). Отличие состоит
в регенерационном растворе.
.
Поэтому водород – катионитные фильтры
в схемах обессоливания отключают на
регенерацию по проскоку в фильтрат
катионов
.
Косвенным показателем проскока катионов
служит снижение кислотности. Процесс
восстановления водород – катионитного
фильтра аналогичен процессу восстановления
натрий – катионитного фильтра (см.
лабораторную работу № 9). Отличие состоит
в регенерационном растворе.
Регенерация водород – катионитных фильтров производят 1,0 – 1,5% - ным раствором H2SO4 по реакциям:
2NaR+H2SO42HR+Na2SO4 (1.45)
2СaR2+H2SO42HR+СaSO4 (1.46)
2MgR2+H2SO42HR+MgSO4 (1.47)
При проведении регенерации концентрацию кислотности раствора увеличивают постепенно во избежание обрастания зерен катионита отложениями сульфата кальция CaSO4, нерастворимыми в воде (загипсовывание катионита).
При ОН – ионировании воды обменным анионом является анион OH–, который в процессе фильтрования воды через слой анионита поглощает находящиеся в ней анионы.
Для удаления из обрабатываемой воды
анионов сильных кислот (![]() ,
,
![]() ,
,
![]() ,
,
![]() )
фильтр загружают слабоосновным анионитом
на котором протекают следующие реакции:
)
фильтр загружают слабоосновным анионитом
на котором протекают следующие реакции:
![]() (1.48)
(1.48)
Н2SO4+2ROHR2SO4+2H2O (1.49)
![]() (1.50)
(1.50)
Анионы слабых кислот (![]() )
не вступают в обменные реакции со
слабоосновным анионитам. Для удаления
из водород – катионированной воды всех
анионов фильтр загружают высокоосновным
анионитом, который способен удалять из
воды, кроме анионов сильных кислот,
также и анионы слабых кислот по реакциям:
)
не вступают в обменные реакции со
слабоосновным анионитам. Для удаления
из водород – катионированной воды всех
анионов фильтр загружают высокоосновным
анионитом, который способен удалять из
воды, кроме анионов сильных кислот,
также и анионы слабых кислот по реакциям:
![]() (1.51)
(1.51)
![]() (1.52)
(1.52)
Сильноосновные аниониты значительно дороже слабоосновных, а их обменная емкость невелика, поэтому их применяют на второй и третьей ступнях обессоливания для удаления из воды в основном анионов кремниевой кислоты. Для удаления основного количества угольной кислоты в схемах ВПУ используют декарбонизаторы. Углекислота, оставшаяся в воде после декарбонизатора, удаляется сильноосновным анионитом.
При истощении анионита анионитные
фильтры первой ступени обессоливания
отключают на регенерацию по проскоку
в фильтрат ионов
![]() ,
а анионитовые фильтры второй ступени
– по проскоку ионов
,
а анионитовые фильтры второй ступени
– по проскоку ионов
![]() .
.
Для восстановления обменных свойств слабо – и высокоосновных анионитов используют 4,0 % - ый раствор NaOH.
![]() (1.53)
(1.53)
![]() (1.54)
(1.54)
RCl+NaOH ROH+NaCl (1.55)
На ВПУ ТЭС технологический процесс обессоливания воды складывается из нескольких ступеней. В зависимости от количества ступеней обессоливания различают следующие схемы:
упрощенное обессоливание;
двухступенчатое обессоливание;
трехступенчатое обессоливание.
Выбор конкретной схемы обессоливания зависит от качества исходной воды, а также от типа парогенераторов, установленных на ТЭС. На АЭС выбор схемы обессоливания воды зависит от типа реактора.
Порядок выполнения работы.
Перед началом выполнения лабораторной работы по обессоливанию воды производят отборы проб водопроводной воды для определения ее жесткости и щелочности (методики определения смотри в лабораторных работа № 4 и 5).
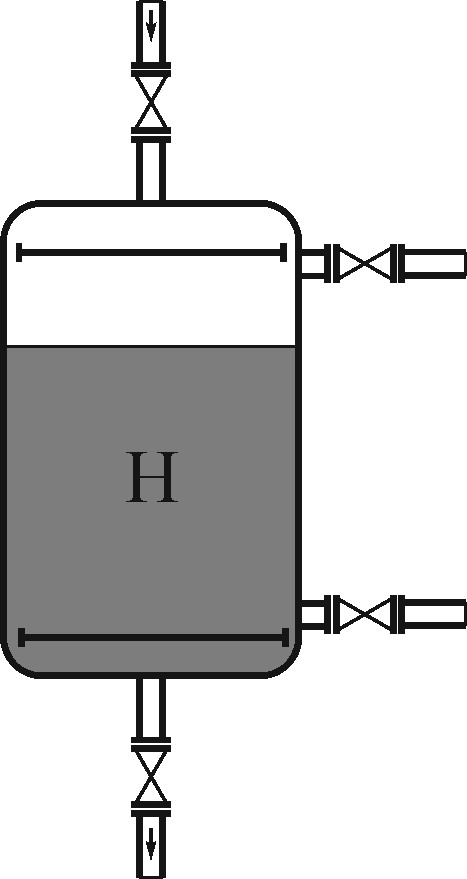
Рис. 1.3 - Модель водород – катионитного фильтра |
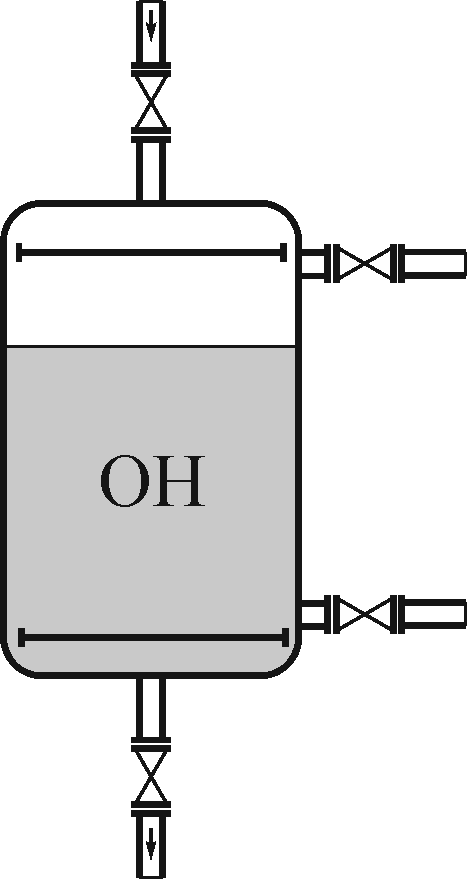
Рис. 1.4 - Модель ОН – ионитного фильтра |
Модель водород – катионитного фильтра представлена на рис. 1.3. Для выполнения работы открывают краны 1 – 2 и производят пропуск водопроводной воды сверху – вниз со скоростью фильтрования 10 – 15 м/г. Умягченную водород-катионированную воду отбирают в сосуд емкостью 1000 мл. Из него производят отборы проб умягченной воды мерными цилиндрами по 100 мл в чистые конические колбы для определения остаточной жесткости и кислотности (методику определения кислотности смотри в лаб. работе № 3). Оставшуюся водород – катионированную воду в количестве не менее 500 мл пропускают через ОН – ионитный фильтр со скоростью 10 м/ч (рис.1.4). Производят отборы проб обессоленной воды по 100 мл для проведения анализов на остаточную жесткость и щелочность.
Результаты анализов показателей качества водопроводной, умягченной водород-катионированной и обессоленной воды заносим в таблицу 1.13.
Таблиц 1.13
Вода |
Показатель качества, мг-экв/дм3 |
Опыт |
||
1 |
2 |
3 |
||
Водопроводная |
Жо, мг-экв/дм3 |
|
|
|
Що = Жк, мг-экв/дм3 |
|
|
|
|
Жнк, мг-экв/дм3 |
|
|
|
|
Умягченная |
Жост, мг-экв/дм3 |
|
|
|
К, мг-экв/дм3 |
|
|
|
|
Обессоленная |
Жост, мг-экв/дм3 |
|
|
|
Щмо, мг-экв/дм3 |
|
|
|
|
Щфф, мг-экв/дм3 |
|
|
|
|
По полученным результатам обессоливания воды сделать обоснованный вывод о характере изменения показателей качества воды по отдельным стадиям ее обработки.
Контрольные вопросы:
1. Чем отличается умягченная вода от обессоленной?
2. На чем основан метод ионообменного обессоливания воды?
3. Чем определяется кислотность водород-катионированной воды?
4. За счет чего изменяется анионный состав воды при водород-катионировании?
5. По какому показателю отключают на регенерацию водород-катионитовые фильтры в схемах обессоливания и почему?
6. Чем объясняется низкая концентрация раствора Н2SО4 при регенерации Н-фильтров?
7. Чем отличаются слабо- и высокоосновные аниониты?
8. Почему высокоосновные аниониты применяют на 2-й и 3-й ступенях обессоливания?
9. От чего зависит на ТЭС и АЭС выбор конкретной схемы обессоливания?
10. Написать реакции работы и регенерации водород-катионитового фильтра.
11. Написать реакции работы и регенерации анионитного фильтра.
12. Чему эквивалентна максимальная кислотность водород-катионированной воды?
13. Что служит косвенным показателем проскока в фильтрат катиона Na+?
14. Проанализировать достоинства и недостатки водород-катионированной воды.