
- •1 Охрана труда при выполнении лабораторных работ в лаборатории № 324 3
- •2 Лабораторные работы по курсу «Водоподготовка и водно-химические режимы тэс и аэс». Часть 1. Водоподготовка 12
- •1 Охрана труда при выполнении лабораторных работ в лаборатории № 324
- •1.1 Общие требования
- •1.2 Характеристика основных химических веществ, применяемых в лаборатории № 324
- •1.2.1 Аммиак водный технический nh4oh.
- •1.2.2 Едкий натр NaOh.
- •1.2.3 Серная кислота h2so4.
- •1.2.4 Соляная кислота.
- •1.2.5 Полиакриламид паа.
- •1.2.6 Трилон б.
- •1.2.7 Гидразингидрат n2h4h2o.
- •1.3 Хранение кислот и щелочей.
- •1.4 Требования по охране труда в аварийных ситуациях
- •1.5 Необходимые реагенты и их приготовление
- •1.5.1 Приготовление растворов кислот и щелочей
- •1.5.2 Приготовление раствора трилона б
- •1.5.3 Приготовление аммиачного буферного раствора
- •1.5.4 Приготовление раствора натрия сернистого
- •1.5.5 Расчет и приготовление рабочего раствора коагулянта оксихлорида алюминия(оха)
- •1.5.6 Приготовление растворов индикаторов
- •Выполнение определения.
- •Лабораторная работа № 2 Определение сухого и плотного остатков воды
- •Общие сведения.
- •Выполнение определения.
- •Вычисление результатов.
- •Лабораторная работа № 3 Определение кислотности воды
- •Общие сведения.
- •Необходимые реактивы
- •Выполнение определения
- •Вычисление результатов.
- •Лабораторная работа № 4 Определение щелочности природной и технической воды
- •Общие сведения
- •Щелочные компоненты различных вод
- •Необходимые реактивы
- •Выполнение определения
- •Лабораторная работа № 5 Определение общей жесткости воды трилонометрическим методом
- •Общие сведения
- •Сущность метода
- •Необходимые реактивы
- •Выполнение определения.
- •Вычисление результатов
- •Контрольные вопросы:
- •Лабораторная работа № 6 Определение кальциевой жесткости воды трилонометрическим методом
- •Общие сведения
- •Необходимые реактивы:
- •Выполнение определения
- •Вычисление результатов
- •Лабораторная работа № 7 Определение оптимальной дозы коагулянта при обработке воды
- •Общие сведения
- •Выполнение определения
- •Результаты опыта
- •Лабораторная работа № 8 Умягчение воды методом осаждения накипеобразователей.
- •Общие сведения
- •Определение необходимого расхода NaOh
- •Выполнение определения
- •Лабораторная работа № 9 Умягчение воды методом натрий-катионирования
- •Общие сведения
- •Выполнение работы
- •Процесс регенерации фильтра
- •Лабораторная работа № 10 Обессоливание воды методом ионного обмена.
- •Общие сведения
- •Лабораторные работы по курсу «Водоподготовка и водно-химические режимы тэс и аэс». Часть II. Водно-химические режимы тэс и аэс
- •Лабораторная работа № 1 Определение величины присоса охлаждающей воды в конденсатор турбины
- •Общие сведения.
- •Выполнение работы
- •Выполнение определения
- •Лабораторная работа № 2 Определение концентрации свободной угольной кислоты в воде
- •Общие сведения
- •Выполнение работы
- •Лабораторная работа № 3 Контроль состояния проточной части турбин и поверхностей нагрева парогенераторов.
- •Общие сведения
- •Контроль за состоянием проточной части турбины
- •Контроль состояния поверхностей нагрева парогенераторов
- •Лабораторная работа № 4 Определение степени загрязнённости экранных труб котла
- •Общие сведения
- •Методика определения
- •Лабораторная работа № 5 Определение скорости коррозии металла энергетического оборудования.
- •Общие сведения
- •Лабораторная работа № 6 Сепаратор spiroventair&dirt
- •Общие сведения
- •Порядок выполнения работы
- •Лабораторная работа № 7 Водно-химический режим энергоблока с котлом барабанного типа
- •Общие сведения.
- •Выполнение работы
Определение необходимого расхода NaOh
Приведенные выше реакции умягчения воды показывают, что едкий натр расходуется на осаждение всех видов солей жесткости и на связывание свободной углекислоты.
На основании этого необходимое количество NaOH для умягчения воды в мг/кг можно определить по формуле:
GNaOH=ЭNaOH·(ЖO + 0,012·Ж3К + αNaOH), мг/кг; (1.32)
где ЭNaOH – эквивалент едкого натра, мг-экв;
ЖO – общая жесткость воды, мг-экв/дм3;
ЖК – карбонатная жесткость воды, мг-экв/дм3;
αNaOH – избыток едкого натра, мг-экв/дм3;
Перед началом проведения работы необходимо определить:
общую жесткость обрабатываемой воды, ЖO, мг-экв/дм3;
карбонатную жесткость воды, ЖК=Щ, мг-экв/дм3
концентрацию приготовленного раствора NaOH.
Для умягчения берется V=500 мл воды, предварительно подогретой до 90…95 °С.
Дозировку едкого натра удобнее производить в виде раствора. С учетом конценрации рабочего раствора и его количества, полученного по формуле (1.32) определим объемное количество едкого натра по формуле:
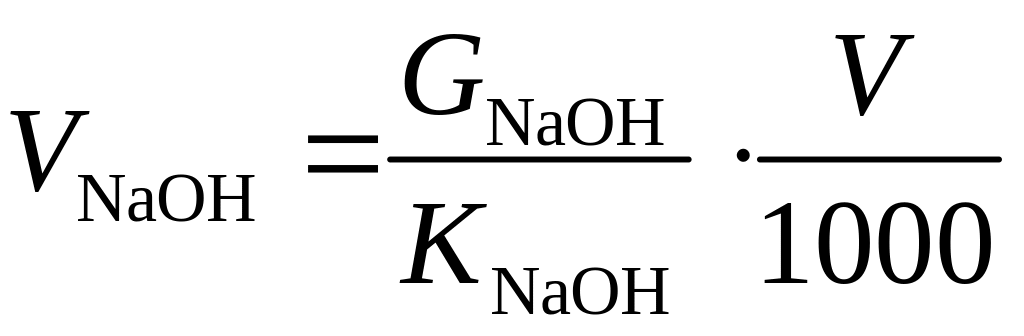 ,
мл (1.33)
,
мл (1.33)
Выполнение определения
В стакан емкостью 750 мл наливают мерным цилиндром 500 мл воды, подлежащей умягчению, и нагревают ее на электрической плитке до температуры 90-100 °С. Затем при помощи пипетки или цилиндра вводят необходимую дозу реагента в виде раствора известной концентрации.
После ввода едкого натра содержимое стакана тщательно перемешивают стеклянной палочкой и выпавшему осадку дают отстояться в течение 10-15 минут. Затем осадок отфильтровывают на бумажном фильтре и производят определение общей жесткости и щелочности фильтрата умягченной воды (см. лабораторные работы № 4, 5).
Полученные показатели качества исходной и умягченной воды заносят в таблицу 1.11.
Таблица 1.11
Определяемые показатели |
Исходная вода |
Умягченная вода |
Жесткость, мг-экв/дм3 |
|
|
Щелочность, мг-экв/ дм3 |
|
|
Проанализировать полученные результаты.
Контрольные вопросы:
1. Что называют процессом умягчения воды?
2. На чем основан метод умягчения осаждением накипеобразователей?
3. Основные реагенты-осадители, применяемые на ВПУ ТЭС и АЭС.
4. Для каких природных вод целесообразно применение метода известкования (реакции)?
5. Особенности метода содоизвесткования (реакции).
6. Особенности едконатрового метода осаждения (реакции).
7. Назовите малорастворимые соединения кальция и магния, образующиеся в результате обработки воды реагентами-осадителями.
8. В каком аппарате на предочистке ВПУ проводят умягчение воды осаждением накипеобразующих солей?
Лабораторная работа № 9 Умягчение воды методом натрий-катионирования
Цель работы: Ознакомление с умягчением воды методом ионного обмена на модели натрий-катионитового фильтра. Изучение свойств натрий-катионированной воды.
Общие сведения
У
Рисунок 1.1 - Na-катионитовый
фильтр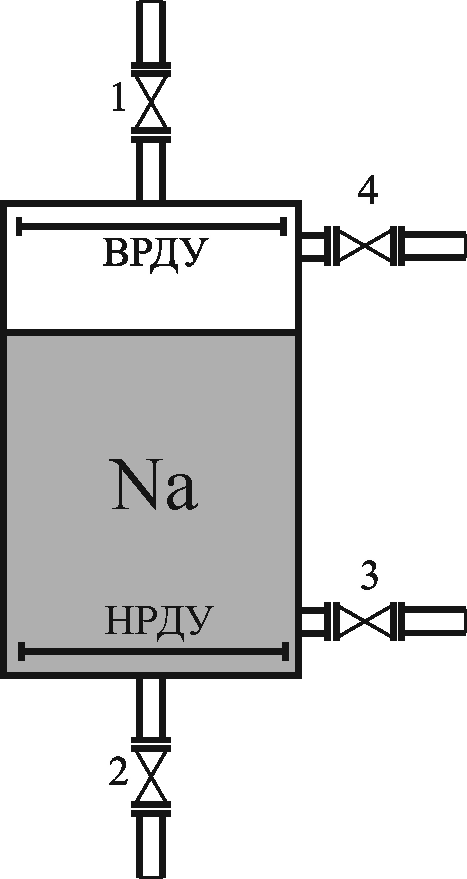
В зависимости от обменного катиона различают следующие процессы умягчения воды:
водород-катионирование (обменный катион H+);
натрий-катионирование (обменный катион Na+);
аммоний-катионирование (обменный катион NH3+).
В данной лабораторной работе процесс умягчения воды будет проходить на Na- катионитовом фильтре (рисунок 1.1).
Лабораторная установка состоит из фильтра диаметром 50 мм, высотой 240 мм, заполненного катионитом С-100 на высоту 120 мм. Для управления отдельными процессами работы фильтра он оборудован верхним и нижним дренажно-распределительным устройством и зажимами (задвижками) 1,2,3,4.
Полный цикл работы фильтра состоит из следующих процессов:
умягчение воды;
взрыхление слоя катионита;
пропуск регенерационного раствора (10%- ый раствор NaCl)
отмывка катионита.
