
- •Изучение изотермического процесса
- •Введение
- •Тема: изучение изотермического процесса
- •1. Теоретическая часть
- •1.1. Идеальный газ
- •1.2. Уравнение состояния газа
- •1.3. Изопроцессы идеального газа
- •1.3.1. Изотермический процесс
- •1.3.2. Изобарический процесс
- •1.3.3. Изохорический процесс
- •1.4. Работа, совершаемая газом
- •1.5. Внутренняя энергия системы
- •1.6. Первое начало термодинамики
- •1.7. Уравнение адиабаты
- •2. Метод работы
- •2.1. Определение изотермического модуля всестороннего сжатия
- •2 .2. Описание установки
- •3. Порядок выполнения работы
- •4. Контрольные вопросы
- •Библиографический список
- •Содержание
- •Изучение изотермического процесса
- •680021, Г. Хабаровск, ул. Серышева, 47.
1.3. Изопроцессы идеального газа
Во всех изопроцессах состав газа не изменяется.
Термодинамические процессы, в которых изменение состояния газа происходит, когда один из параметров сохраняется постоянным, а два оставшихся изменяются, носят общее название изопрцессов.
1.3.1. Изотермический процесс
1.3.1. Изотермический процесс – процесс,
когда изменение состояния газа происходит
при постоянной температуре и массе
газа. (![]() ).
).
Такой закон описывается уравнением
Бойля и Мариотта, установленном на
основе экспериментов. При изотермическом
процессе произведение давления на объем
для данной массы газа (![]() )
есть величина постоянная:
)
есть величина постоянная:
![]() . (1.7)
. (1.7)
Р, Па
Г рафически
эта зависимость изображается равнобокой
гиперболой и носит название изотермы
(рис 1.1). Для одной и той же массы разные
изотермы соответствуют различным
температурам:
рафически
эта зависимость изображается равнобокой
гиперболой и носит название изотермы
(рис 1.1). Для одной и той же массы разные
изотермы соответствуют различным
температурам:
![]() .
.
Рис 1.1. График
изотермического процесса
1.3.2. Изобарический процесс
1.3.2. Изобарический процесс – процесс,
когда изменение состояния газа происходит
при постоянном давлении (![]() ).
).
Обозначим объем
некоторой массы газа при
![]() через
через
![]() .
При изобарическом нагревании его на
.
При изобарическом нагревании его на
![]() объем возрастет и сделается равным
объем возрастет и сделается равным
![]() .
Такой процесс описывается законом
Гей-Люссака, который также был установлен
опытным путем: при изобарическом процессе
относительное увеличение объема данной
массы газа (
)
.
Такой процесс описывается законом
Гей-Люссака, который также был установлен
опытным путем: при изобарическом процессе
относительное увеличение объема данной
массы газа (
)
![]() прямо пропорционально увеличению
температуры при постоянном давлении
(
).
прямо пропорционально увеличению
температуры при постоянном давлении
(
).
![]() ;
;
![]() , (1.8)
, (1.8)
где – коэффициент пропорциональности, называемый коэффициентом объемного расширения.
Коэффициент
численно равен относительному увеличению
объема газа (по отношению к объему газа,
который он занимает при
![]() )
при нагревании его на 1 градус. Как
показали опыты, этот коэффициент для
всех газов одинаков и равен
)
при нагревании его на 1 градус. Как
показали опыты, этот коэффициент для
всех газов одинаков и равен
![]() .
.
Следовательно, ![]() и
и
![]() – уравнения Гей-Люссака (1.9).
– уравнения Гей-Люссака (1.9).

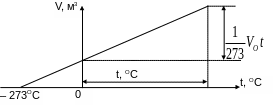
Рис. 1.2. График изобарного процесса
График зависимости объема газа
от температуры
![]() является прямой линией (рис 1.2).
является прямой линией (рис 1.2).
1.3.3. Изохорический процесс
1.3.3. Изохорический процесс – процесс,
когда изменение состояния газа происходит
при постоянном объеме (![]() ).
).
Если давление некоторой массы газа при
температуре
будет
![]() ,
то при изохорическом нагревании газа
на
давление возрастает и становится равным
,
то при изохорическом нагревании газа
на
давление возрастает и становится равным
![]() .
Изохорический процесс описывается
опытным законом Шарля: при изохорическом
процессе относительное увеличение
давления данной массы газа (
)
.
Изохорический процесс описывается
опытным законом Шарля: при изохорическом
процессе относительное увеличение
давления данной массы газа (
)
![]() прямо пропорционально увеличению
температуры при постоянном объеме (
).
прямо пропорционально увеличению
температуры при постоянном объеме (
).
![]() , (1.10)
, (1.10)
где – коэффициент
пропорциональности, называемый
температурным коэффициентом давления
и численно равный относительному
увеличению давления газа (по отношению
к давлению газа, взятому при
)
при нагревании газа на 1 градус.
Эксперименты показали, что этот
коэффициент для всех газов одинаков и
равен
,
следовательно,
![]() и
и
![]() – закон Шарля.
– закон Шарля.
![]() (1.11)
(1.11)


Рис. 1.3. График изохорного процесса
График зависимости давления газа P от температуры t изображается в виде прямой линии (рис. 1.3). Из рисунка видно, что, продолжив эту прямую в область отрицательных температур (по Цельсию) до пересечения ее с осью Х (точка О1), можно получить уравнение:
![]() ,
откуда
,
откуда
![]() .
.
Давление газа на стенки сосуда является следствием ударов молекул об эти стенки, т. е. связано с передачей импульсов стенкам сосуда при ударах молекул. Приведенный выше результат означает, что при прекращается поступательное движение молекул. Поэтому температура носит название абсолютного нуля температуры.
Температура, отсчитанная от абсолютного нуля, именуется абсолютной температурой (температурой по Кельвину) и обозначается буквой Т.
Точка плавления льда при нормальном
атмосферном давлении оказалась равной
![]() ,
а по шкале Цельсия она принята за
,
поэтому абсолютная температура Т связана
с температурой t (по шкале
Цельсия) следующим соотношением:
,
а по шкале Цельсия она принята за
,
поэтому абсолютная температура Т связана
с температурой t (по шкале
Цельсия) следующим соотношением:
![]() ;
для приближенных подсчетов можно
считать, что
;
для приближенных подсчетов можно
считать, что
![]() .
.
Преобразуем выражение (1.9), характеризующее изобарический процесс, заменяя температуру, отсчитанную по шкале Цельсия, абсолютной температурой:
![]() .
.
Обозначим объем газа при температуре
![]() через
через
![]() ,
а при температуре
,
а при температуре
![]() – через
– через
![]() .
Напишем
.
Напишем
![]() ;
;
![]() .
Поделив почленно равенства, получим:
.
Поделив почленно равенства, получим:
![]() . (1.12)
. (1.12)
При изобарическом процессе объем некоторой массы газа прямо пропорционален его абсолютной температуре.
Аналогично можно прийти к выводу, что при изохорическом процессе давление некоторой массы газа прямо пропорционально его абсолютной температуре. Так формулируется закон Шарля.
![]() . (1.13)
. (1.13)
