
- •Общие методические указания
- •Химическая посуда и ее предназначение
- •Работа 1 определение молярной массы эквивалента металла методом вытеснения водорода
- •Основные теоретические положения
- •Математически закон эквивалентов для условной реакции вида
- •Порядок выполнения работы
- •Форма 1 Экспериментальные и расчетные данные
- •Давление насыщенного водяного пара при различных температурах
- •Контрольные задания Вариант 1
- •Вариант 2
- •Вариант 3
- •Вариант 4
- •Вариант 5
- •Вариант 6
- •Вариант 7
- •Вариант 8
- •Вариант 10
- •Вариант 11
- •Вариант 12
- •Вариант 13
- •Вариант 14
- •Вариант 15
- •Работа 2 основные классы неорганических соединений
- •Основные теоретические положения
- •Оксиды – это соединения, состоящие из двух элементов, одним из которых является кислород. Образование названия оксида (его номенклатура) подчиняется следующим правилам:
- •Химические свойства кислот
- •Химические свойства солей
- •Перевод кислых (основных) солей в среднюю соль
- •Порядок выполнения работы
- •Получение и свойства гидроксидов
- •Получение и свойства кислот
- •Контрольные задания Вариант 1
- •Вариант 3
- •Вариант 4
- •Порядок выполнения работы
- •Часть 1. Определение изменения энтальпии растворения безводной соли
- •Изменение температуры калориметра для процесса растворения cоли (указать название соли)
- •Часть 2. Определение изменения энтальпии реакции нейтрализации сильной кислоты сильным основанием
- •Экспериментальные и расчетные данные для процесса нейтрализации
- •Часть 1. Определение изменения энтальпии растворения безводной соли
- •Форма 4 Экспериментальные и расчетные данные для процесса растворения соли (указать название соли)
- •Часть 2. Определение изменения энтальпии реакции нейтрализации сильной кислоты сильным основанием
- •Контрольные задания
- •Определение константы скорости и энергии активации реакции окисления йодоводородной кислоты пероксидом водорода
- •Основные теоретические положения
- •Порядок выполнения работы
- •Экспериментальные и расчетные данные
- •Контрольные задания Вариант 1
- •Вариант 7
- •Титульный лист
- •Метрологическая карта средств измерения
- •Приложение 3 Интегральные энтальпии растворения солей в воде при 25 0с
- •Приложение 4
- •Изменение энтальпии нейтрализации 1 моль эквивалентов
- •Сильной кислоты сильным основанием при различных
- •Температурах
- •Библиографический список
- •Третьяков ю.Д. Практикум по неорганической химии: Учеб. Пособие. – м.: Академия, 2004.
- •Химия Лабораторный практикум
- •Часть 1
Определение константы скорости и энергии активации реакции окисления йодоводородной кислоты пероксидом водорода
Цель работы: получить общие представления о химической кинетике, практически ознакомиться с методом определения константы скорости и энергии активации химической реакции.
Основные теоретические положения
Раздел химии, изучающий скорость и механизм химических реакций, называется химической кинетикой. Скоростью химической реакции называется изменение количества реагирующего вещества за единицу времени в единице реакционного пространства. Скорость химической реакции зависит от природы реагирующих веществ, их концентраций, температуры, давления (в случае газообразных участников реакции) и присутствия катализатора.
Зависимость скорости от концентрации выражается основным законом химической кинетики – законом действия масс (для простых реакций, протекающих в одну стадию в одном направлении в соответствии со стехиометрическим уравнением): при постоянной температуре скорость химической реакции прямо пропорциональна произведению концентраций реагирующих веществ, возведенных в степени, равные их стехиометрическим коэффициентам.
В общем случае для реакции вида
аА + bВ + ... → mM + nN + ...
математическое выражение закона имеет вид
![]() , (10)
, (10)
где – скорость химической реакции; k – коэффициент пропорциональности, называемый константой скорости реакции, который равен скорости реакции при единичных концентрациях реагирующих веществ (т.е. при СA = СB = 1 моль/дм3, k = ); СA и СB – концентрации реагентов, моль/дм3; а и b – стехиометрические коэффициенты.
Константа скорости химической реакции k определяется природой реагирующих веществ и зависит от температуры и от присутствия катализатора. Выражение (10) называется кинетическим уравнением реакции.
В химической кинетике реакции классифицируют по молекулярности, т.е. по числу частиц, участвующих в элементарном взаимодействии, и по порядку кинетического уравнения данной реакции (по порядку реакции). Известны одно-, двух- и трехмолекулярные (моно-, би- и тримолекулярные) реакции, например:
моно- А → В + С; би- А + В → С или 2А → В + С.
Порядком химической реакции n называют сумму показателей степеней при концентрациях реагентов в кинетическом уравнении. Различают общий и частный (по каждому веществу) порядки реакции. Общий порядок реакции есть сумма частных порядков. Реакции, скорость которых не зависит от концентрации, имеют нулевой порядок.
Для реакции первого порядка уравнение для расчета константы скорости реакции имеет вид
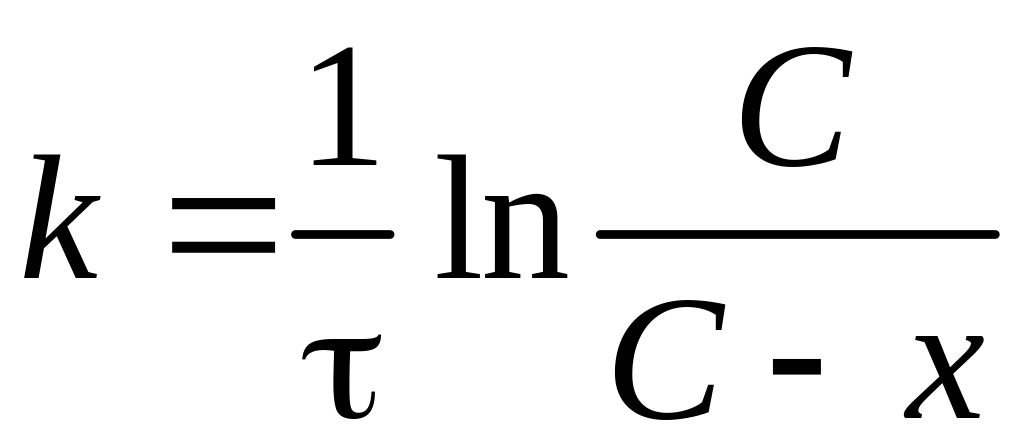 ,
время-1,
,
время-1,
где С – начальная концентрация вещества, моль/дм3; х – количество вещества, вступившего в реакцию к моменту времени τ.
Зависимость скорости гомогенной химической реакции от температуры определяется эмпирическим уравнением Вант-Гоффа:
![]() ,
,
где 2 и 1 – скорости реакции при температурах Т2 и T1; γ – температурный коэффициент скорости реакции (для большинства реакций он лежит в пределах значений 2 – 4). Указанная зависимость может быть выражена в виде следующего правила: при повышении температуры на каждые 10° скорость реакции увеличивается в 2 – 4 раза, если реакция проводится при температуре, близкой к комнатной.
Зависимость константы скорости реакции от температуры также может быть выражена уравнением Аррениуcа:
![]() ,
,
где А – предэкспоненциальный множитель, не зависящий от Т и концентрации; Т – абсолютная температура, К; ЕА – энергия активации, Дж/моль.
Энергия активации равна тому избытку энергии, которым должны обладать молекулы реагентов по сравнению со средней энергией молекул при данной температуре, чтобы их столкновение приводило к химическому взаимодействию. Величина ЕА химической реакции может быть рассчитана по уравнению Аррениуса, если известны значения констант скоростей при разных температурах:
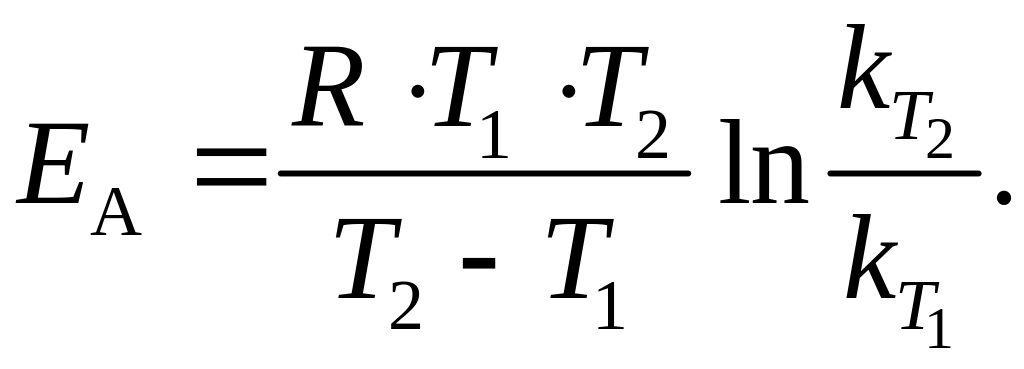 (11)
(11)
Химизм процесса окисления йодоводородной кислоты
пероксидом водорода
Реакция окисления йодоводородной кислоты пероксидом водорода выражается уравнением
2HI + Н2О2 2Н2О + I2.
Количество прореагировавшего пероксида водорода определяется эквивалентным количеством йода путем титрования последнего раствором тиосульфата натрия Na2S2О3:
I2 + 2Na2S2О3 2NaI + Na2S4О6.
Йодоводородную кислоту получают действием серной кислоты на йодиды, например KI или NaI:
2KI + H2SO4 K2SO4 + 2HI.
Так как в результате опыта концентрации KI и HI остаются постоянными, то скорость реакции в условиях опыта зависит только от концентрации пероксида водорода. Следовательно, для вычисления константы скорости этой реакции можно применить уравнение первого порядка.
