
Распад пиримидиновых оснований:
NH2 O O

 |
|| НАДФН2 НАДФ
||
|
|| НАДФН2 НАДФ
||

 N
+Н2О; -NH3
HN CH
HN
CH +Н2О
N
+Н2О; -NH3
HN CH
HN
CH +Н2О


O= цитозин- O= CH дегидро- O= CH2 гидролаза
NH дезаминаза NH урацил(ДГ) NH
цитозин урацил дгидроурацил
NH2
|
C=O
|
NH +H2O
| NH3 + CO2 + -аланин.
CH2 гидролаза
|
CH2
|
COOH
Карбомоил--аланин.
-аланин либо подвергается дальнейшему распаду с образованием аммиака, углекислого газа, воды, либо используется на синтез КоА, карнозина и т.д. Тимин распадается аналогично, но при распаде дает не -аланин, а -аминомасляную кислоту: NH2 – CH2 – CH – COOH
|
CH3
Поскольку из аммиака, образовавшегося при распаде пиримидиновых оснований, синтезируется мочевина, то ее и можно считать конечным продуктом распада пиримидиновых оснований. В норме содержание мочевины в сыворотки крови составляет 2,5 – 8,3 ммоль/л. Суточная экскреция с мочой: 20 – 35 г. Поскольку конечным продуктом распада пиримидиновых оснований (NH3, CO2 , бета-аланин) хорошо растворимы в воде, то клинические симптомы, связанные с нарушением распада пиримидинов выражены слабо. Повышение содержания мочевины в сыворотке отмечают при гемолитической анемии, отравлении и т.д. Снижение содержания мочевины в сыворотке отмечают при генетических нарушениях цикла образования мочевины. Повышение содержания мочевины в моче связаны с гипертиреозом, постоперационными состояниями. Снижается мочевина в моче при гепатопатиях, почечной недостаточности, лечении инсулином.
Синтез нуклеиновых кислот.
1) Синтез пиримидиновых нуклеотидов. Для того, чтобы синтезировать нуклеиновую кислоту, представляющую собой, как известно, полинуклеотидную цепочку, необходимо синтезировать отдельные нуклеотиды. Для синтеза пуриновых и пиримидиновых нуклеотидов могут использоваться либо уже готовые азотистые основания, углеводы и фосфорная кислота, поступающие, например, в клетку из ЖКТ, или образующиеся при внутриклеточном распаде НК, либо для синтеза используются простые соединения: СО2, аммиак, аспартат, глицин, глютамин, рибоза. Существует два отдельных пути синтеза нуклеотидов – один для пиримидинов, другой для пуринов. Но если для синтеза пуринов в клетке есть ферменты, способные утилизировать для синтеза нуклеотидов готовые пуриновые основания, то клетки не располагают эффективными путями для использования свободных пиримидиновых оснований для синтеза нуклеотидов. В то же время они обладают способностью использовать пиримидиновые рибонуклеозиды уридин и цитидин. При этом достаточно добавить фосфорную кислоту и нуклеотид готов. Этот процесс каталиируют соответствующие ферменты: уридинкиназа и цитидинкиназа. Однако гораздо чаще пиримидиновые АО синтезируются из «предшественников». Первым продуктом нуклеотидной природы пиримидинового пути является уридин – 5 – монофосфат, которые затем служит предшественником всех остальных пиримидиновых нуклеотидов. Фосфорибозный компонент для синтеза уридин – 5 – монофосфата переносится в виде 5 – фосфорибозил – 1 – пирофосфат, который, в свою очередь, получается из рибозо – 5 – фосфата, а рибоза – 5 – фосфат из глюкозы, скажем, через пентозофосфатный путь. Схематически этот процесс можно представить так:
Г
 ексозы…….
НО3РОСН2 О
ОН АТФ АМФ
ексозы…….
НО3РОСН2 О
ОН АТФ АМФ

Н Н Н Н фосфорибозил
трансфераза
ОН ОН
Рибоза – 5 - фосфат
 Н2О3РОСН2
О
Н2О3РОСН2
О
О О О
Н Н || ||
Н Н Р – О – Р – ОН
| |
ОН ОН OH OH
5 – фосфорибозил – 1 – пирофосфат
Для дальнейшего синтеза пиримидиновых нуклеотидов необходимо синтезировать циклическую пиримидиновую структуру. Первым этапом синтеза является образования карбомоилфосфат:
2АТФ 2АДФ –H3PO4 NH2
 NH3
+ CO2
C
OPO3H2
NH3
+ CO2
C
OPO3H2
карбомоилфосфатсинтетаза ||
из глютамина O
С этим продуктом (карбомоилфосфат) вы уже встречались в ходе орнитинового цикла, как с промежуточным продуктом в процессе синтеза мочевины. Однако, карбомоилфосфат, необходимый для синтеза мочевины образуется в митохондриях при участии митохондриального фермента карбомоилфосфатсинтетазы – 1, а карбомоилфосфат, участвующий в биосинтезе пиримидиновых оснований, образуется в цитозоле под действием другой формы того же фермента – карбомоилфосфатсинтетазы – 2. Образовавшийся в цитозоле карбомоилфосфат взаимодействует с аспартатом, образуя N – карбомоиласпартат
NH2 COOH NH2 COOH
| | | |
C = O + CH2
-H3PO3
C
CH2
= O + CH2
-H3PO3
C
CH2
| | || |
O PO3H2 H2N–CH аспартаттранс O HN CH
Карбомоил аспартат карбомоилаза |
фосфат COOH
N – карбомоиласпартат
Далее происходит дегидротация и циклизация:
NH2 COOH O O
| | || ||
C
 CH2
- H2O
C НАДН2
C
CH2
- H2O
C НАДН2
C
 ||
HN | NH
CH2 НАД HN
CH
||
HN | NH
CH2 НАД HN
CH
O CH дигидроортаза | | | ||
| C CH дигидрооротат C C-COOH
COOH || NH ДГ || NH
O COOH O
Дигидрооротовая кслота оротовая кислота
На этой стадии к оротовой кислоте присоединяется уже полученный нами ранее
5 – фосфорибозил – 1 – пирофосфат, с образованием оротидиловой кислоты:
O
||

 C
Н2О3Р– СН2
О О O O
C
Н2О3Р– СН2
О О O O
HN CH || || - ПФ
 | ||
+ Н Н Н Н Р – О – Р - ОН
| ||
+ Н Н Н Н Р – О – Р - ОН
C C-COOH | | оротофосфорибозил-
|| NH OH OH трансфераза
O ОН ОН
оротовая кислота 5 – фосфорибозил – 1 – пирофосфат
O O
|| ||
C C
NH CH -СО2 HN CH
| || | ||
C C оротидилат C CН

 ||
NH
декарбоксилаза
|| NH
||
NH
декарбоксилаза
|| NH
O COOH O
Н2О3РН2С О Н2О3РН2С О
Н Н Н Н
Н Н Н Н
ОН ОН ОН ОН
Оротидиловая кислота Урацил – 5 – монофосфат (УМФ)
Необходимо отметить, что из 6 ферментов, участвующих в синтезе УМФ, первые 3 (карбомоилфосфатсинтетаза, аспартаттранскарбомоилаза и дегидрооротаза) связаны в составе одной полипетидной цепи. Два же последних фермента (оротатфосфорибозилтрансфераза и оротидилатдекарбоксилаза) образуют другой комплекс. Суммарно же процесс синтеза УМФ можно представить:
C
 O2
+ NH3
+ АСПАРТАТ 2АТФ 2АДФ
O
O2
+ NH3
+ АСПАРТАТ 2АТФ 2АДФ
O
+ 5 – фосфорибозил- || из аспартата
-
 1 – пирофосфат 6 ферментов
C
1 – пирофосфат 6 ферментов
C
HN CH
 Из
NH3
| || УМФ
Из
NH3
| || УМФ
C CH
|| N
из СО2 O |
Рибоза – Н3РО4
из ФРПР
Но для синтеза НК необходимы трифосфаты. Уридинтрифосфат полуается из УМФ путем нуклеозидкиназных реакций:
АТФ АДФ АТФ АДФ
 УМФ
УДФ
УТФ
УМФ
УДФ
УТФ
нуклеозидкиназа нуклеозидкиназа
Т ак же, нукледифосфаты и нуклеозидтрифосфаты могут взаимно превращаться под действием нуклеозид-дифосфат-киназ: УДФ + АТФ УТФ + АДФ.
нуклеозид-дифосфат-киназ
Синтез ЦТФ. Из УТФ образуется ЦТФ путем аминирования в положении 4 пиримидинового кольца. Источником азота может быть глютамин (превращаясь при этом в глютомат) или же просто аммиак. Схематично этот процесс выглядит так:
O NH2
|| |
C C
N H
CH АТФ АДФ
+ Фк HN CH
H
CH АТФ АДФ
+ Фк HN CH
| || | ||
C C +NH3; -H2O C CН

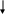 ||
NH
(глютамин)
|| NH
||
NH
(глютамин)
|| NH
O O
рибоза глютамат рибоза
| |
Ф – Ф – Ф ЦТФ - синтетаза Ф – Ф – Ф
УТФ ЦТФ.
Синтез ТТФ.
Известно, что тиминовые нуклеотиды содержатся в ДНК, то есть в их состав входит не рибоза, а дезоксирибоза. Соответственно, синтезируются ТМФ из нуклеотиддифосфатов, содержащих не рибозу, а дезоксирибозу. Мы уже говорили, что предшественником всех пиримидиновых нуклеотидов является уридин – 5 –монофосфат. Путем нуклеозидкиназной реакции, как было показано выше, УМФ превращаются в УДФ. Но для того чтобы УДФ превратить в дУДФ, то есть нуклеотиддифосфат, содержащий дезоксирибозу, необходимо участие трех белков: тиоредоксинредуктазы, тиоредоксина и рибонуклеотидредуктазы. Схемы действия этих белков относительно проста: тиоредоксинредуктаза катализирует восстановление тиоредоксина, тиоредоксин (восстановленный) активирует рибонуклеотидредуктазу, а она, в свою очередь, способствует восстановлению рибозы (в составе нуклеотиддифосфата) до дезоксирибозы. Таким образом, мы получаем дУДФ. дУДФ переходит в дУМФ, который подвергается метилированию. Донором метильной группы является N(5) , N(10) – метилен – FН4 (тетрогидрофолвая кислота).
O О
НN N(5), N(10)-CH2 – FH4 НN СН3
O N тимилатсинтетаза O N
дезоксирибозы. дезоксирибозы.
Н3РО4 Н3РО4
дЦМФ дТМФ
В дальнейшем для получения ТДФ и ТТФ можно привести две стадии фофорилилрования (с использованием нуклеозидкиназ). Получающиеся в результате реакции образования ТМФ гидрофолат (FH2) необходимо восстановить снова до тетрагидрофолата (FH4). Это осуществляется под действием фолатредуктазы и НАДФН. На ингибировании фолатредуктазы (а, соответственно, и образовании ТМФ) основано действие группы антифолатных средств, оказавшихся эффективными противоопухолевыми препаратами. Особенно эффективен: аминоптерин и метотрексат. Тимидилатсинтетаза (фермент, катализирующий реакцию
д УМФ дТМФ ) непосредственно ингибируется 5-фторурацилом и 5-фторо-2`- дезоксиуридином, что тоже используется в противораковой терапии. Таким образом недостаток тимидина и FH4 в быстрорастущих и делящихся раковых клетках останавливает клеточный рост и даже приводит к гибели клеток. Биосинтез пиримидиновых нуклеотидов регулируется ингибированием по принципу обратной связи. Схема регуляции:
ингибитор ингибитор
ЦМФ ЦТФ
С О2
+ глютамин + АТФ карбомоил-
N-карбомоиласпартат
О2
+ глютамин + АТФ карбомоил-
N-карбомоиласпартат
(NН3) карбомоил- фосфат аспартат-
фосфат-синтаза транскарбомоилаза (АТК-аза)
УМФ УТФ ЦТФ
ЦТФ ингбирует АТК-азу, снижая сродство этого фермента к субстрату. АТФ, напротив, активирует АТК-азу, повышая сродство этого фермента к субстрату. При этом идет конкуренция АТФ и ЦТФ за активный центр фермента. АТФ в высокой концентрации вытесняет ЦТФ. Это имеет высокий биологический смысл: (1) активация АТК-азы под действием АТФ уравнивает скорости образования пуриновых и пиримидиновых нуклеотидов (а для синтеза НК нужны их сопоставимые количества); (2) активация под действием АТФ сигнализирует о его досточной концентрации в качестве субстрата для некоторых реакций биосинтеза пиримидиновых нуклеотидов (например, синтеза карбомоилфосфата, фосфорилирования УМФ до УТФ).
2) Синтез пуриновых нуклеотидов.Мы уже упоминали, о том, что для синтеза пуриновых нуклеотидов могут использоваться готовые пуриновые азотистые основания, либо пуриновые нуклеозиды, либо идет синтез из предшественников. В первом случае используются два фермента: а) аденинфосфорибозилтрансфераза (переносит фосфорибозу с ФРПФ на аденин с образованием АМФ). б) гипоксантин-гуанинфосфорибозилтрансфераза (переносит фосфорибозил с ФРПФ на гипоксантин и гуанин с образованием инозинмонофосфата и ГМФ соответственно).
Причем второй фермент работает более активно. А при генетическом дефекте (его отсутствии) развивается синдром Леш-Нихана, возможно развитие мочекаменной болезни, подагры. Если же для синтеза пуриновых нуклеотидов используется готовый нуклеозид, то, как и в случае пиримидиновых нуклеотидов работают киназы (например, аденозинкиназа), катализирующие присоединение к нуклеозиду остатка фосфорной кислоты. Процесс биосинтеза пуриновых оснований из предшественников несколько отличается от синтеза примидиновых оснований. Если, в случае синтеза пиримидиновых нуклеотидов, 5-фосфорибозил – 1- пирофосфат присоединялся на одной из последних стадий образования уридин – 5`-монофосфата – первого продукта нуклеотидной природы, образующегося в ходе пиримидинового пути, то при синтезе первого продукта нуклеотидной природы пуринового пути – инозин - 5`-монофосфата (УМФ) – 5 – фосфорибозил – 1 – пирофосфат принимает участие уже в первой реакции:
Н2О3РОСН2 О Н2О3РОСН2 NH2
О О О О
Н Н || || (1) Н Н
Н Н Р – О – Р – ОН (2) H H
| |
ОН ОН OH OH OH OH
5 – фосфорибозил – 1 – пирофосфат 5-фосфорибозил – 1 – амин
(1) – +глютамин; -глютамат; - ПФ
(2) – амидофосфорибозилтрансфераза.
+Затем 5-фосфорибозил – 1 – амин вступает в реакцию с глицином.
Н2О3РОСН2 NH3 ( +) Н2О3РОСН2 NH–C–CH2
О АТФ АДФ+Фк || |
Н Н +глицин –Н2О Н Н O NH2
Н Н H H
ОН ОН OH OH
5-фосфорибозил – 1 – амин рибонуклеотид
глицинамида
(глицинамидрибозилфосфат)
… УМФ
Далее идет еще 7 реакций до образования инозин – 5 – монофосфата:
СО2, аспартат, глицин, 2 глютамина, 2 тетрогидрофолата
5 – фосфорибозил –1 – пирофосфат
4 АТФ
10 ферментов
4 АДФ
+ Из СО2
 4
Н3РО4
4
Н3РО4
 О
Из глицина
О
Из глицина

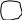

 Из аспартата
||
Из аспартата
||
 HN
N
HN
N
 Из FH4
Из FH4
Из FH4
Из FH4

 N
N
N
N
 |
|
 Рибоза - ФК
Рибоза - ФК
Из глютамина Из 5 – фосфорибозил – 1 – пирофосфата
Далее, из инозин –5 – фосфата возможен синтез АМФ и ГМФ:
O O NH

 ||
+НАД НАДН2 || - H2O
|
||
+НАД НАДН2 || - H2O
|
H
 N
N +НО2
HN N
+ионMg HN
N
N
N +НО2
HN N
+ионMg HN
N
 ГТФ ГДФ
+ Н3РО4
ГТФ ГДФ
+ Н3РО4
ДГ Аспартат
|| (УМФ - ДГ)
 O
NH N
N
N Фумарат
N N
O
NH N
N
N Фумарат
N N
Рибоза Рибоза Рибоза
| | |
ФК ФК ФК
(Ксантозин-5-монофосфат) (Инозин-5-монофосфат) (АМФ)
2
 АТФ
Глютамин
АТФ Нуклеотид-
АТФ
Глютамин
АТФ Нуклеотид-
 киназа
киназа
2АДФ
+ Глютамат АДФ
2 Н3РО3
(АДФ)
Н3РО3
(АДФ)
О АТФ Нуклеотид-
|| Киназа
HN N
АДФ
(АТФ)
H2N
N N
Рибоза
|
ФК АТФ АДФ АТФ АДФ
(ГМФ) Нуклеотидкиназа (ГДФ) Нуклеотидкиназа (ГТФ)
Образование дезокси – пуриновых нуклеотидов идет так же, как и образование дезокси – пиримидиновых нуклеотидов: на уровне ди- фосфатов участвуют 3 белковых фактора (рибонуклеотидредуктаза – активируется восстановленной формой тиоредоксина, который в свою очередь восстанавливается с помощью тиоредоксинредуктазы). Биосинтез пуриновых нуклеотидов тоже регулируется по типу обратной связи (как и биосинтез пиримидиновых нуклеотидов). Так, накопление АМФ и ГМФ, действует ингибирующе на амидофосфорибозилтрансферазу, фермент, который катализирует первую реакцию синтеза пуриновых оснований (реакцию переноса аминогруппы с глютамина на 5-фосфорибозил – 1- пирофосфат). Второй регуляторный механизм действует на одной из более поздних стадий синтеза пуриновых нуклеотидов. Так, избыток ГМФ в клетке вызывает аллостерическое ингибирование процесса образования ГМФ из инозиновой кислоты, но при этом не влияет на синтез АМФ из инозин – 5 – монофосфата. Избыток же АМФ ингибирует синтез АМФ из инозин – 5 – монофосфата, но не влияет на синтез ГМФ.
