
- •2. Химическая технология и защита окружающей среды
- •3. Основные направления в развитии химической промышленности.
- •4. Хтп и их классификация
- •5. Уровни анализа, описания и расчета хтп.
- •6. Основные показатели хтп: степень превращения, выход продукта
- •7. Расходные коэф-ты. Избирательность хтп (φ)
- •Скорость хтп. Способы увеличения скорости
- •9. Материальный баланс процесса.
- •10. Тепловой баланс процесса.
- •11. Задачи термодинамического анализа
- •12. Равновесие Принцип Ле-Шателье и его применение в хт. Равновесная степень превращения
- •13.Константа равновесия и способы ее выражения
- •14. Влияние температуры на константу равновесия, ее расчет
- •15.Общая характеристика гомогенных хтп
- •16. Влияние концентраций реагентов на скорость гомогенных процессов и степень превращения
- •Основное кинетическое уравнение:
- •17. Влияние концентрации реагентов на избирательность гомогенных хтп.
- •18. Температура как фактор повышения скорости процесса и управления выходом продукта реакции (необратимые, обратимые, экзо- и эндотермические реакции)
- •19. Влияние температуры на скорость, избирательность процесса и выход продукта при протекании сложных реакций
- •20. Влияние давления на скорость газофазных реакций
- •1 Влияние давления на скорость необратимых процессов
- •2 Влияние давления на скорость обратимых процессов
- •21. Характер изменения основных параметров хтп во времени
- •22. Принципы расчета оптимальных параметров проведения процессов
- •23. Применение катализаторов в гомогенных системах (гомогенный катализ)
- •24. Общая характеристика гетерогенных хтп.
- •25. Процессы протекающие во внешнедиффузионной области.
- •26. Внутредиффузионная область протекания процессов.
- •27. Кинетическая область протекания процессов.
- •28. Основные методы изготовления и требования к катализаторам.
- •29. Особенности протекания каталитических процессов. Гетерогенные каталитические процессы.
- •Области протекания гетерогенных каталитических процессов.
- •Влияние этих торможений на избирательность Кт.
- •Влияние внутридиффузионных торможений на кинетику процесса.
- •30. Переходные области протекания гетерогенного хтп.
- •31. Моделирование хтп. Общие понятия.
- •37. Основные характеристики потоков и их влияние на хтп
- •38. Протекание хтп в потоке идеального вытеснения (ив)
- •39. Температурные режимы протекания хтп.
- •40. Протекание хтп в потоке полного (идеального) смешения.
- •4 0.1. Технологические расчеты.
- •40.2. Закономерность хтп без теплообмена.
- •41. Теплообмен с окружающей средой как фактор интенсификации хтп в потоке.
- •42. Секционирование реакционной зоны потока смешения.
- •42.1. Методы расчета каскада реакционных зон.
- •43. Сопоставление протекания хтп в различных идеальных потоках.
- •43.1. Процессы без тепловых эффектов ( при изотермическом температурном режиме).
- •43.2. Процессы с большими тепловыми эффектами.
- •43.3. Сравнение по избирательности.
- •44. Протекание хтп в неидеальных потоках.
- •45. Химические реакторы
- •45.1. Классификация
- •46. Основные требования к промышленным реакторам:
- •47. Отклонения реальных реакторов от идеализированных моделей
- •48. Реакторы для гомогенных процессов
- •49. Реакторы для проведения гетерогенных процессов в системе г — ж
- •50. Химико-технологические системы (хтс). Основные определение.
- •51. Моделирование химика-технологической системы
- •52. Организация химико-технологического процесса. Выбор схемы процесса
- •53. Основные условные обозначения технолог.Операторов. Основные способы отражения структуры хтс.
- •54. Технологическая схема хтс. Схемы с открытой цепью и циклические
- •55. Элементы анализа и синтеза хтс.
- •56. Основные типы связей.
- •59. Задачи, решаемые при исследовании хтс.
- •60. Сырьё в химической технологии. Комплексное использование сырья.
- •61. Методы очистки воды для производственных процессов. Очистка сточных вод. Замкнутые водооборотные циклы.
- •62. Очистка газообразных промышленных выбросов.
- •63. Обработка твердых отходов
- •64. Виды энергии, применяемые в химической промышленности. Использование тепла отходящих газов: регенераторы, рекуператоры, котлы-утилизаторы.
- •65. Методы обогащения твёрдых, жидких материалов и газов.
5. Уровни анализа, описания и расчета хтп.
Анализ и описание ХТП проводят послед-но с учетом уровня протекания пр-са. Всего сущ-ет 6 уровней протекания пр-са.
Протекание ХТП на этих уровнях описывается законами кинетики химической реакции. При описании, анализе и расчете протекания реакции, как элемента ХТП используют известные кинетические закономерности без раскрытия механизма реакции.
1. Молекулярный уровень.
На этом уровне описание ХТП происходит как молекулярное взаимодействие реагирующих в-в. Протекание ХТП опис-ся закономерностями кинетики в хим. р-ции.
При описании, анализе и расчете протекания хим. р-ции как элемента ХТП исп-ют известные кинетические закономерности без раскрытия мех-ма р-ции. Поэтому, говорят, что описание пр-са на этом уровне проводят на языке формальной кинетики. Сущ-ет еще теоретическая кинетика, главная задача к-рой изучение зав-ти протекания ХТП в зав-ти от строения исх в-в. Формальная кинетика изучает скорость р-ции, выход продукта, степень превращения и т.д. В простейшем случае эти закономерности м. изучать для описания гомогенных пр-сов.
2. Уровень малого объема.
Опис-ся протекание гетерогенных пр-сов для малого объема взаимодействующих фаз. Напр., для частицы тв материала, реагирующего с газом или ж-ю; для зерна кат-ра; пузырька газа, поднимающегося в ж-ти; для капли ж-ти, омываемой газом и др.
Необходимость рассмотрения пр-сов на этом уровне связана с тем, что для анализа и расчета гетерогенных пр-сов знания закономерностей протекания только хим. р-ций в большинстве случаев недостаточно. Эти закономерности необходимо дополнить закономерностями протекания физ. пр-сов переноса массы и теплоты.
Совместное протекание хим. р-ции пр-сов переноса теплоты и массы опис-ся уже закономерностями макрокинетики.
3. Уровень потока.
На этом уровне рассм-ся протекание пр-са на совокупности тв частиц, капель ж-ти, зерен кат-ра и др. разновидностей малого объема, находящихся в потоке реагирующих в-в. Учитываются эффекты, связанные с хар-ром движения потоков, с изм-ем тем-ры и конц-ции в различных участках реакционного объема. Для гетерогенных пр-сов закономерности их протекания в малом объеме дополняются закономерностями изм-ия конц-ции и тем-ры по длине реакционной зоны (lр.з.), ч/з к-рую проходит поток.
4. Уровень реактора.
На этом уровне учитываются конструктивные особенности реакционных зон, их число, взаимное расположение, соотношение технологических показателей пр-са при прохождении потока из одной реакционной зоны в др.
5. Уровень ХТС.
Здесь учитываются взаимные связи м/д реакторами, теплообменниками, смесителями и др. аппаратами и трубопроводами, используемыми для переработки сырья в конечные (целевые) продукты.
6. Уровень предприятия, отрасли или министерства.
В ОХТ это не рассм-ся.
6. Основные показатели хтп: степень превращения, выход продукта
1. Степень превращения – доля одного из реагентов, вступающего в р-цию от нач кол-ва этого реагента.
Напр.,
![]()
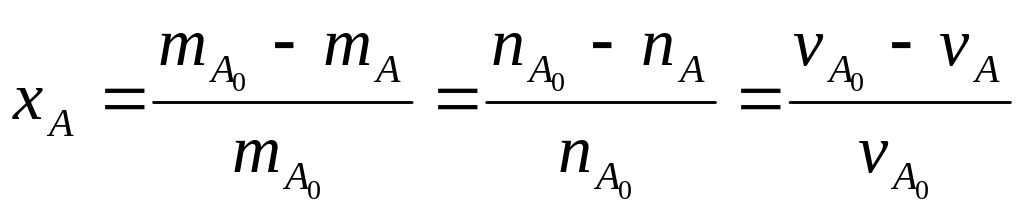
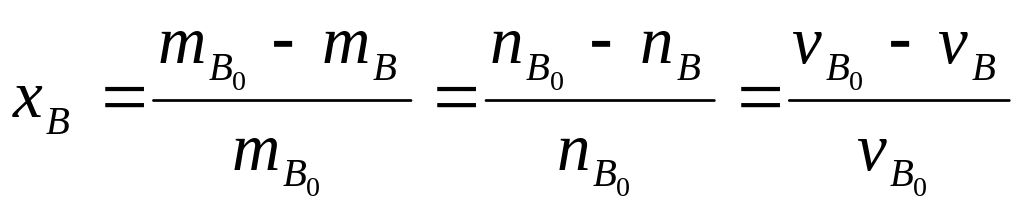
где mА, mВ, nА, nB, vА, vB – это масса, число молей и объем реагентов А и В в конце пр-са; а с “0” – в начале пр-са.
Если
реагенты А и В взяты в стехиометрическом
соотношении, то
![]()
![]() .
.
Степень превращения реагента, взятого с избытком от стехиометрического соотношения, всегда ниже, чем поступающего в недостатке.
Если αВ – коэф-т избытка в-ва В по отношению к стехиом., то
![]()
Если р-ция протекает без изм-ия объема (изохорическая), то конц-ции реагентов А и В равны
![]()
![]()
![]()
![]()
![]() [об.%]
[об.%]
Из этих ф-л вытекает расчетная ф-ла:
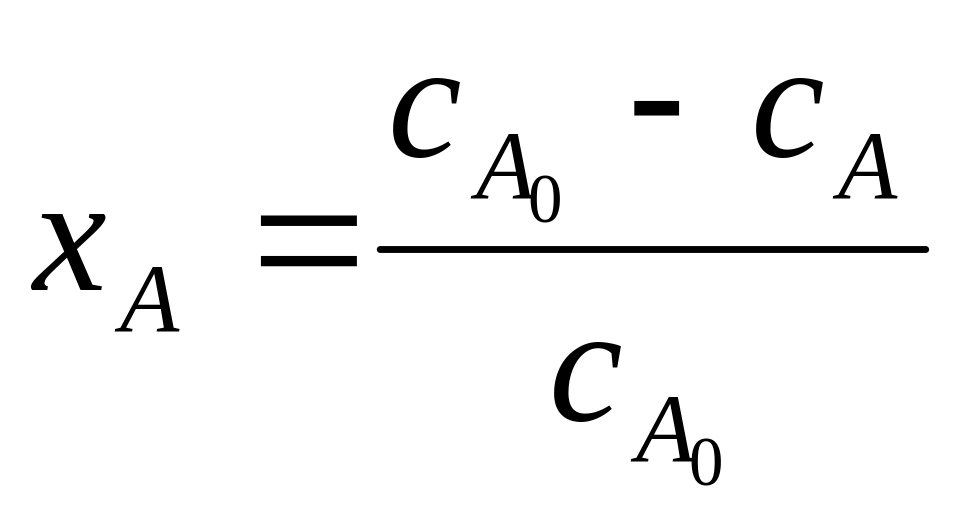
От протекания р-ции с изм-ем объема хi рассчитывают по ф-ле:
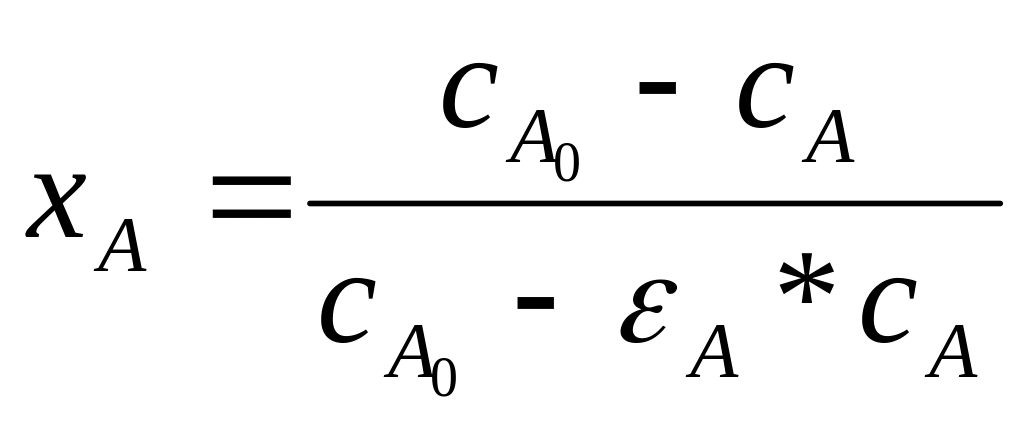
где εА – относит. изм-ие объема реакционной смеси при полном превращении реагента А, т.е.

где ... – это объем реакционной смеси в конце и начале пр-са.
В
общем виде значение
![]() для р-ции
для р-ции
![]() равно
равно
![]()
где β – доля всей стехиом. смеси в начальный момент времени.
Для пр-сов межфазной массопередачи (испарение, конденсация, абсорбция, десорбция и др.) степень превращения наз-ся степенью межфазного перехода (степень абсорбции и т.д.)
2. Выход продукта – отношение практически полученного продукта к его максимальному, рассчитанному по стехиом. ур-ию р-ции при степени превращения реагентов =1
Обычно, mmax рассчитывают по исх в-ву, находящемуся в недостатке, но иногда для оценки эф-ти исп-ия исх в-ва, взятого с избытком, mmax опр-ют по кол-ву этого в-ва.
В-во В в избытке, то численное значение фактического выхода продукта D по в-ву А (ФD(А)) будет выше, чем по в-ву В, но при этом
![]()
Максим-ый
выход продукта j
по i
![]() Фmax
j(i)
при протекании простых необр-ых р-ций
в общем случае равен:
Фmax
j(i)
при протекании простых необр-ых р-ций
в общем случае равен:
![]()
Для простых необр-ых р-ций фактический выход продукта по к-либо исходному в-ву численно равен степени превращения этого в-ва, т.е.
![]()
Для обр-ых р-ций исходные в-ва превращаются в продукты не полностью, и если в ф-ле (2.7) вместо mф подставить mр, то получим равновесный выход:
![]()
Степень превращения, достигаемая при равновесии, наз-ся равновесной степенью превращения (хр, х*).
Для хар-ки степени превращения обратимого пр-са к равновесию на практике исп-ют, так называемый “выход от теоретического” или “выход от равновесного”, к-рый равен отношению фактически получаемого продукта (mф) к кол-ву его, к-рое получилось бы, если пр-с пришел в состояние равновесия (mр)
![]()
Выход продукта во многом опр-ся степенью совершенства ХТП, затраты сырья на ед. продукции и экономические показатели производства.
