
- •2. Химическая технология и защита окружающей среды
- •3. Основные направления в развитии химической промышленности.
- •4. Хтп и их классификация
- •5. Уровни анализа, описания и расчета хтп.
- •6. Основные показатели хтп: степень превращения, выход продукта
- •7. Расходные коэф-ты. Избирательность хтп (φ)
- •Скорость хтп. Способы увеличения скорости
- •9. Материальный баланс процесса.
- •10. Тепловой баланс процесса.
- •11. Задачи термодинамического анализа
- •12. Равновесие Принцип Ле-Шателье и его применение в хт. Равновесная степень превращения
- •13.Константа равновесия и способы ее выражения
- •14. Влияние температуры на константу равновесия, ее расчет
- •15.Общая характеристика гомогенных хтп
- •16. Влияние концентраций реагентов на скорость гомогенных процессов и степень превращения
- •Основное кинетическое уравнение:
- •17. Влияние концентрации реагентов на избирательность гомогенных хтп.
- •18. Температура как фактор повышения скорости процесса и управления выходом продукта реакции (необратимые, обратимые, экзо- и эндотермические реакции)
- •19. Влияние температуры на скорость, избирательность процесса и выход продукта при протекании сложных реакций
- •20. Влияние давления на скорость газофазных реакций
- •1 Влияние давления на скорость необратимых процессов
- •2 Влияние давления на скорость обратимых процессов
- •21. Характер изменения основных параметров хтп во времени
- •22. Принципы расчета оптимальных параметров проведения процессов
- •23. Применение катализаторов в гомогенных системах (гомогенный катализ)
- •24. Общая характеристика гетерогенных хтп.
- •25. Процессы протекающие во внешнедиффузионной области.
- •26. Внутредиффузионная область протекания процессов.
- •27. Кинетическая область протекания процессов.
- •28. Основные методы изготовления и требования к катализаторам.
- •29. Особенности протекания каталитических процессов. Гетерогенные каталитические процессы.
- •Области протекания гетерогенных каталитических процессов.
- •Влияние этих торможений на избирательность Кт.
- •Влияние внутридиффузионных торможений на кинетику процесса.
- •30. Переходные области протекания гетерогенного хтп.
- •31. Моделирование хтп. Общие понятия.
- •37. Основные характеристики потоков и их влияние на хтп
- •38. Протекание хтп в потоке идеального вытеснения (ив)
- •39. Температурные режимы протекания хтп.
- •40. Протекание хтп в потоке полного (идеального) смешения.
- •4 0.1. Технологические расчеты.
- •40.2. Закономерность хтп без теплообмена.
- •41. Теплообмен с окружающей средой как фактор интенсификации хтп в потоке.
- •42. Секционирование реакционной зоны потока смешения.
- •42.1. Методы расчета каскада реакционных зон.
- •43. Сопоставление протекания хтп в различных идеальных потоках.
- •43.1. Процессы без тепловых эффектов ( при изотермическом температурном режиме).
- •43.2. Процессы с большими тепловыми эффектами.
- •43.3. Сравнение по избирательности.
- •44. Протекание хтп в неидеальных потоках.
- •45. Химические реакторы
- •45.1. Классификация
- •46. Основные требования к промышленным реакторам:
- •47. Отклонения реальных реакторов от идеализированных моделей
- •48. Реакторы для гомогенных процессов
- •49. Реакторы для проведения гетерогенных процессов в системе г — ж
- •50. Химико-технологические системы (хтс). Основные определение.
- •51. Моделирование химика-технологической системы
- •52. Организация химико-технологического процесса. Выбор схемы процесса
- •53. Основные условные обозначения технолог.Операторов. Основные способы отражения структуры хтс.
- •54. Технологическая схема хтс. Схемы с открытой цепью и циклические
- •55. Элементы анализа и синтеза хтс.
- •56. Основные типы связей.
- •59. Задачи, решаемые при исследовании хтс.
- •60. Сырьё в химической технологии. Комплексное использование сырья.
- •61. Методы очистки воды для производственных процессов. Очистка сточных вод. Замкнутые водооборотные циклы.
- •62. Очистка газообразных промышленных выбросов.
- •63. Обработка твердых отходов
- •64. Виды энергии, применяемые в химической промышленности. Использование тепла отходящих газов: регенераторы, рекуператоры, котлы-утилизаторы.
- •65. Методы обогащения твёрдых, жидких материалов и газов.
21. Характер изменения основных параметров хтп во времени
Хар-р протекания пр-са в аппарате периодического действия очень сильно зав-ит от времени.
1. Необратимые (а) и обратимые (б) простые р-ции.
![]()
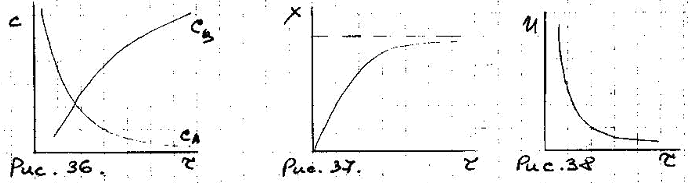
![]() ,
,
![]() ,
,
![]()
Аналогично изменяется с, Х, U для обратимых р-ций
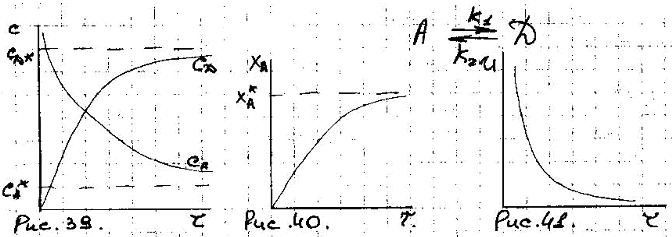
2. Сложные реакции.
2.1) Параллельные реакции
k1 В
А n = 1,
k2
![]()
 D
D
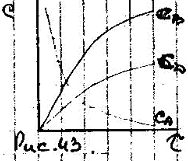 Для
р-ции I
порядка избирательность во времени не
изменяется. .
Для
р-ции I
порядка избирательность во времени не
изменяется. .
Выводы:
Если при протекании парал-еых р-ций основная р-ция описывается ур-ем более высокого порядка, чем побочная, то
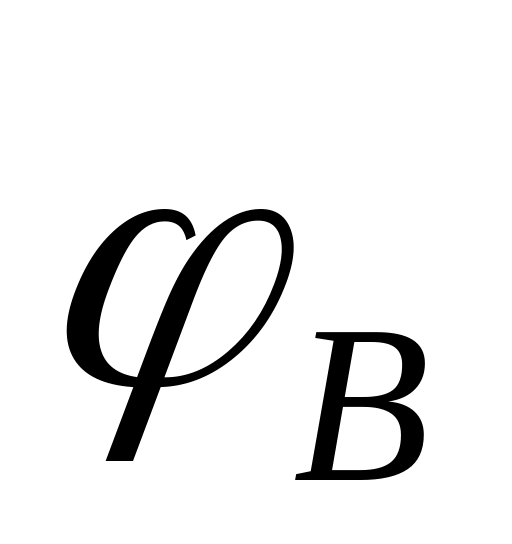 падает по мере увеличения τ, соотв-но
уменьшается и выход ФВ(А)
целевого продукта.
падает по мере увеличения τ, соотв-но
уменьшается и выход ФВ(А)
целевого продукта.При протекании парал-ных р-ций ХА и ФВ(А) растут во времени, не изм-ся и при очень большом времени выход продукта численно становится равным избирательности пр-са. Степень ХА 1, а выход ФВ(А) .
ХА* = ФВ(А)
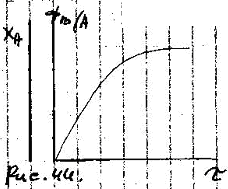
2.2) Последовательные реакции.
k1 k2
А В D
Если обе р-ции явл-ся необратимыми и опис-ся ур-ми I порядка и они протекают без изменения объема, то скорости обр-ия или расходования в-в опис-ся следубщими диф. ур-ми:
![]() ,
,
![]() ,
,
![]()
![]()
П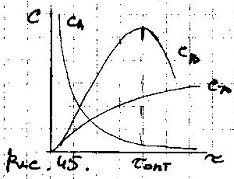 осле
преобр-ия всех этих ур-ий и решения этой
системы ур-ий получают выр-ия, описывающие
изменения конц-ции в-в во времени. При
этом становится очевидным следующий
хар-р изм-ия этих конц-ций.
осле
преобр-ия всех этих ур-ий и решения этой
системы ур-ий получают выр-ия, описывающие
изменения конц-ции в-в во времени. При
этом становится очевидным следующий
хар-р изм-ия этих конц-ций.
Хаар-р изм-ия конц-ции во времни для послед-ных р-ций будет зависеть лишь от порядка р-ций, приводящих к обр-ию целевого продукта В и побочного продукта D, а численные значения конц-ции будут опис-ся соотношением констант скоростей этих р-ций.
Возможны 2 варианта:
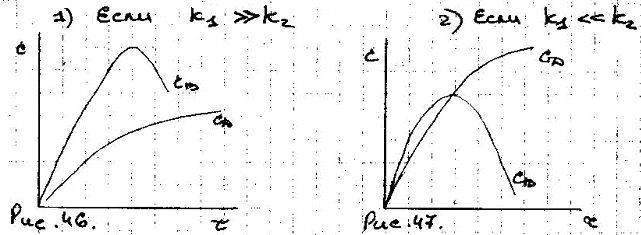
Выход целевого продукта, как и его конц-ция, опис-ся также кривой с максимумом, и в задачу технолога входит определение оптимальгного времени протекания пр-са:
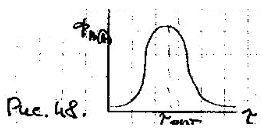 .
.
22. Принципы расчета оптимальных параметров проведения процессов
Оптимальным значением какого-либо параметра проведения ХТП принято считать такое при котором конечные показатели процесса являются наилучшими. Чаще всего оптимизируют по одному показателю, который называется критерием оптимизации. Наиболее обоснованы экономические критерии, однако учесть влияние всех параметров на экономику очень сложно, поэтому чаще всего используют в качестве критерия оптимизации технологические показатели. К таким критериям относят скорость U процесса, связанную с производительностью работы оборудования, В продукта, Х сырья, φ (избирательность) и др. Оптимизирующие параметры, это параметры, с помощью которых технолог может управлять процессом (с, t, Р, τ). Критерий оптимизации, который записывается в виде функций оптимизирующих параметров, называют целевой функцией. Задача оптимизации – определение значений оптимизирующих параметров, при которых целевая функция достигает экстремального (max, min) значения. Наиболее часто используют аналитический метод оптимизации. Как правило, он реализуется легко для простых случаев. Его суть – после необходимых преобразований, целевую функцию дифференцируют по оптимизирующему параметру и находит его значение из условия равенства производной нулю. В качестве примера рассмотрим 3 случая:
1. Определить оптимальную температуру проведения необратимой реакции 1-го порядка:
А-В. Примем за критерий оптимизации скорость процесса.
Тогда целевая функция F=U=ko*Ca*e-E/kT
Очевидно, что целевая функция с ростом температуры растет неограниченно и экстремум отсутствует. В этом случае оптимизация значения температуры определяется ограничениями по тех.допустимой Т (Топт=Тмакс).
2. Расчет Топт для обратимых экзотермических реакций: А↔В=q
Критерий оптимизации U.
F=U=ko1*Ca*e-E1/kT- ko2*Cв*e-E2/kT
Са и Св не являются оптимизирующими параметрами, так как их значения и соотношение являются результатом реакции.
![]()
П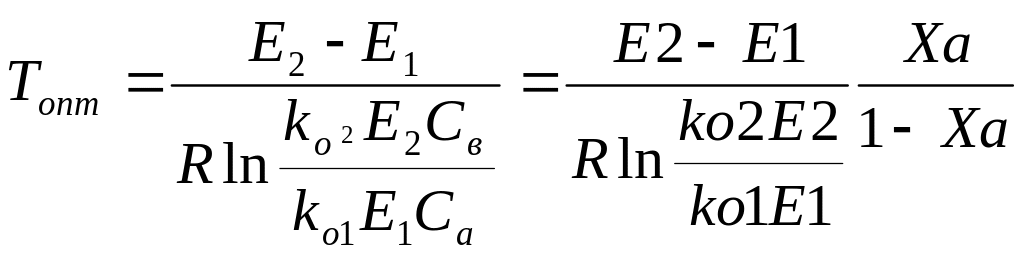 осле
преобразования уравнения получаем
формулу для расчета оптимальных
температур:
осле
преобразования уравнения получаем
формулу для расчета оптимальных
температур:
Задаются производными значениями либо Сц, либо Ха, рассчитывают соот. значения Топт.
Так
как при
![]() ,
то при малых степенях превращено
Топт=Тмах.доп..
Рассчитать оптимальные соотношения
концентрации N2
и Н2
для синтеза NH3.
За критерий оптимизации примем U.
Скорость синтеза NH3
описывается уравнением Темкина
(справочные данные):
,
то при малых степенях превращено
Топт=Тмах.доп..
Рассчитать оптимальные соотношения
концентрации N2
и Н2
для синтеза NH3.
За критерий оптимизации примем U.
Скорость синтеза NH3
описывается уравнением Темкина
(справочные данные):
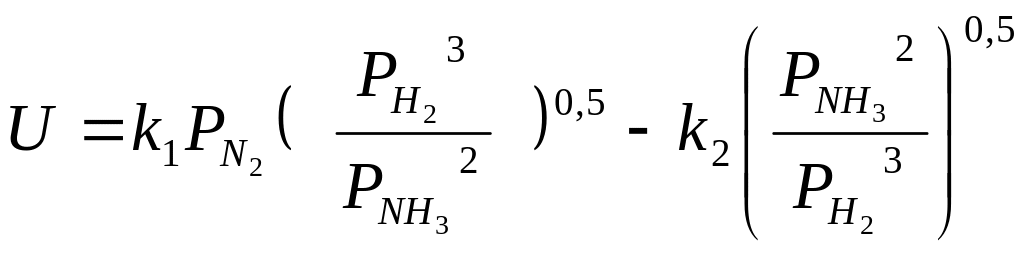
Упрощаем задачу. Примем, что процесс протекает вдали от равновесия, вторым членом можно пренебречь (скорость обратной реакции), также можно пренебречь влиянием процессов реакции при U превращения. Тогда F=U=k1PN2PH21,3
Обозначим через у- мольную долю Н2 в смеси.
Тогда РН2=уРобщ; PN2=(1-у)Робщ.
Скорость
реакции можно записать в следующем
виде:
![]()
![]() ,
уопт=3/5;
1- уопт=2/5;
(PN2/PH2)опт=2/3.
,
уопт=3/5;
1- уопт=2/5;
(PN2/PH2)опт=2/3.
Если процесс протекает вблизи равновесия, необходимо учитывать и скорость обратной реакции. Проведя математический анализ можно показать: NN2/NH2=(PN2/PH2)опт=1/3.
