
- •1. Перенос энергии электромагнитной волной, вектор Пойтинга, интенсивность. Шкала электромагнитных волн.
- •2. Основные законы геометрической оптики. Принцип Ферма. Оптический путь. Принцип Гюйгенса.
- •3. Интерференция и когерентность. Интерференция от двух точечных излучателей на примере опыта Юнга.
- •4.Интерференция по методу деления волнового фронта: бипризма Френеля, зеркало Ллойда.
- •5.Интерференция света в плоскопараллельных пластинах. Линии равного наклона и равной толщины.
- •6. Принцип Гюйгенса-Френеля. Зоны Френеля. Метод векторных диаграмм.
- •7.Дифракция Френеля от простейших преград. Зонная пластинка.
- •Дифракция от диска
- •8. Дифракция Фраунгофера от щели (случай нормального падения света). Расчет интенсивности методом векторных диаграмм.
- •9. Количественный критерий вида дифракции.
- •10. Дифракция Фраунгофера на решетке (случай нормального падения света).
- •11.Дифракционная решетка как спектральный прибор: угловая дисперсия, разрешающая сила, критерий Рэлея.
- •12.Поляризация света. Виды поляризации. Закон Малюса.
- •Вопрос 13. Поляризация света при отражении и преломлении. Закон Брюстера.
- •14. Дисперсия света. Фазовая и групповая скорости.
- •15. Абсолютно черное тело. Законы излучения.
- •Закон Кирхгофа.
- •Закон Стефана-Больцмана.
- •Закон смещения Вина.
- •16. Тепловое излучение. Закон Кирхгофа.
- •19. Тормозное рентгеновское излучение.
- •20. Фотоэлектрический эффект.
- •21. Рассеяние рентгеновских лучей. Эффект Комптона.
- •22. Модель атома Резерфорда. Опыты по рассеиванию α-частиц.
- •23. Закономерности в атомных спектрах. Формула Бальмера.
- •24. Постулаты Бора. Правило квантования орбит.
- •25. Элементарная боровская теория водородного атома.
- •26.Волновые свойства микрочастиц. Гипотеза Луи де Бройля.
- •27.Соотношение неопределенностей Гейзенберга.
- •28. Свойства волновой функции. Принцип суперпозиции.
- •29. Уравнение Шредингера. Квантование энергии частиц.
- •Вопрос 30. Частица в потенциальной яме.
- •31.Атома водорода. Квантовые числа.
- •33. Металлы, диэлектрики и полупроводники с точки зрения зонной теории.
25. Элементарная боровская теория водородного атома.
Бор предположил, что из всех возможных орбит электрона осуществляются только те, для которых момент импульса равен целому кратному постоянной Планка ħ, делённой на 2π.
 ,
n=1,2,3,…(63.1)
,
n=1,2,3,…(63.1)
n – главное квантовое число;
 =1,054*
=1,054* Дж/с – постоянная Планка.
Дж/с – постоянная Планка.
Рассмотрим электрон, движущийся в поле атомного ядра с зарядом Ze. При Z=1 такая система соответствует атому водорода, при иных Z – водородоподобному иону.
Согласно второму закону Ньютона произведение массы электрона на его центростремительное ускорение должно равняться кулоновской силе.

Исключая v из (63.1) и (63.2), получаем, что радиус электронных орбит в атоме может принимать лишь ряд дискретных значений:


- схема энергетических уровней, определяемая (63.5).
Для первой орбиты водородного атома (Z=1, n=1) получается:

Внутренняя энергия атома слагается из кинетической энергии электрона (ядро неподвижно) и энергии взаимодействия электрона с ядром (потенциальной энергии):

Из
(63.2) следует, что
 .
Следовательно:
.
Следовательно:

Учтя значения r, даваемые (63.3), получим дозволенные значения внутренней энергии атома:

При переходе атома водорода (Z=1) из состояния n в состояние m испускается квант:

Частота испущенного света равна:

Таким
образом, мы пришли к обобщённой формуле
Бальмера, причём для постоянной Ридберга
получается значение
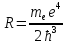 ,
и если подставить значения констант,
то получается величина, поразительно
похожая на экспериментальное значение
постоянной Ридберга.
,
и если подставить значения констант,
то получается величина, поразительно
похожая на экспериментальное значение
постоянной Ридберга.
Теория Бора была весьма крупным шагом в развитии теории атома. Она с полной отчетливостью показала неприменимость классической физики к внутриатомным явлениям и главенствующее значение квантовых законов в микромире.
26.Волновые свойства микрочастиц. Гипотеза Луи де Бройля.
Материальные частицы должны обладать и волновыми свойствами.
Бройль распространил корпускулярно – волновой дуализм на частицы с массой покой ≠0
Формула де Бройля:
 – де Бройлевская длина волны с импульсом
р
– де Бройлевская длина волны с импульсом
р



 E2m=ћω2m
E2m=ћω2m
 E2m=ћω2m
E2m=ћω2m
27.Соотношение неопределенностей Гейзенберга.
Принцип неопределённости Гейзенберга – фундаментальное неравенство (соотношение неопределённостей), устанавливающее предел точности одновременного определения пары характеризующих систему физических наблюдаемых, описываемых не коммутирующими операторами (x и p, I и U):
 – постоянная Планка
– постоянная Планка

Соотношение неопределённостей и устойчивость атома



(боровский
радиус)

Следствие:
- для микрочастицы теряет смысл понятие траектории
- невозможность полного покоя микрочастиц
- обл. изменения координаты ограничивает область локал.
28. Свойства волновой функции. Принцип суперпозиции.
Волновая функция (ψ-функция) – это функция, которая характеризует состояние частиц. Физический смысл ψ-функции приписывается квадрату |ψ (x1,x2…xn,t)|2, который интерпретируется, как плотность вероятности обнаружить систему в положении, описываемом координатами: х1=х01, х2=х02, хn=x0n в момент времени t.
 .
.
Вероятность
того, что частица будет обнаружена в
любой области пространства конечного
объёма V: P=
Условие
нормировки:
 = 1
= 1
Принцип суперпозиции квантовых состояний.
Для волновых функций справедлив принцип суперпозиции, заключающийся в том, что если система может пребывать в состояниях, описываемых ψ – функциями ψ1 и ψ2, то она может пребывать и в состоянии, описываемом волновыми функциями ψ1 и ψ2.
ψ∑ = с1ψ1 + с2ψ2 при любых комплексных с1 и с2
Не применимо для релятивистской механики.
