
- •Введение
- •Основные закономерности химико-технологического процесса.
- •Основные технологические понятия.
- •Технологическая схема.
- •Равновесие в химико-технологическом процессе.
- •Скорость химико-технологических процессов.
- •Кинетика гетерогенных химических реакций.
- •1. Теоретические основы составления балансов хтп.
- •1.1. Классификация хтс:
- •О тсюда
- •1.5. Общие принципы составления материальтного и теплового баланса.
- •1.6. Классификация систем по виду уравнения Данкелера.
- •1 .7. Использование уравнения Дамкелера для составления математической модели хтп.
- •1.8. Совместимость понятий при рассмотрении хтп.
- •2. Катализ в химической технологии.
- •2.2. Гомогеный катализ и его скорость.
- •Способы осуществления экзотермической каталитической реакции по линии оптимальных температур.
- •Химические реакторы.
- •Основные требования к промышленным реакторам.
- •Технологическая классификация.
- •Математические модели основных типов химических реакторов.
- •Реактор периодического действия (рпд).
- •Реакторы непрерывного действия.
- •С с равнение трёх типов реакторов.
- •Каскад реакторов идеального смешения.
- •4. Реальные химические реакторы.
- •4.1.Масштабирование реальных химических реакторов.
- •4.2.Типовые конструкции химических реакторов.
- •4.3.Реакторы для проведения гомогенных реакций в жидкой фазе.
- •4.4.Реакторы для проведения реакций в системе газ/жидкость.
- •4.5.Реакторы для проведения реакций в системе газ/твёрдая фаза.
- •4.6.Реакторы для проведения газовых реакций.
- •4.7.Промышленные печи.
- •5.Сырьё, вода и энергия в химической промышленности.
- •5.1.Сырьё.
- •5.2.Вода.
- •6.Технология серной кислоты.
- •6.1.Нитрозный способ образования серной кислоты.
- •6.2.Контактный метод получения серной кислоты.
- •6.3.Метод двойного контактирования.
1 .7. Использование уравнения Дамкелера для составления математической модели хтп.
-
Р


 азовая
загрузка реагента, обработка до заданной
степени превращения, разовая выгрузка
продукта.
азовая
загрузка реагента, обработка до заданной
степени превращения, разовая выгрузка
продукта.
В![]()

![]() случае осуществления в реакторе
гомогенной реакции, отсутствует
переходящий поток раздела фаз, то для
этого процесса С/
0.
случае осуществления в реакторе
гомогенной реакции, отсутствует
переходящий поток раздела фаз, то для
этого процесса С/
0.
Характеристическое уравнение реактора периодического действия.
-
В
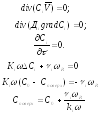 системе осуществляется гетерогенная
ХР, в стационарном режиме можно пренебречь
диффузионным потоком.
системе осуществляется гетерогенная
ХР, в стационарном режиме можно пренебречь
диффузионным потоком.
1.8. Совместимость понятий при рассмотрении хтп.
У


 равнение
Дамкелера.
равнение
Дамкелера.
Закрытая система Открытая система
х![]()
![]() арактерно:
отсутствует конвективный характерно:
конвективный поток
арактерно:
отсутствует конвективный характерно:
конвективный поток
поток вещества(div(C ) = 0); вещества(div(C ) 0);
имеет место изменение технологической отсутствует изменение
переменной во времени (С/ 0). технологической переменной во
Периодические, нестационарные. времени (С/ = 0).
Непрерывный, стационарный.


Если в системе высока турбулизация потока, то можно принебреч диффузионным потоком вещества. div(ДigradCi) = 0.
Если система гомогенная, то отсутствует переходящий поток вещества
KiCi = 0.
Если в системе имеется ХР, обязательно наличие источника или стока iR 0.
2. Катализ в химической технологии.
Катализ - изменение скорости ХР или её интенсивности в результате воздействия специальных веществ (катализаторы, ингибиторы).
Катализаторы - вещества, которые многократно вступая в промежуточные взаимодействия с исходными реагентами и промежуточными продуктами, изменяют механизм ХР и увеличивают скорость достижения равновесия, при этом по окончание реакции они восстанавливают свои первоначальные свойства.
Катализаторами могут быть: газы, жидкости, твёрдые вещества, по этому по агрегатному состоянию различают: гомогенный катализ - все компоненты ХР, включая и катализатор в одной фазе; гетерогенный катализ - есть другая фаза, т.е. есть поверхность раздела фаз.
По механизму действия различают следующие процессы:
-
Каталитические реакции - где осуществляются ОВ процессы (Ме, оксиды или сульфиды Ме);
-
Каталитические процессы в которых протекает кислотно - основное взаимодействие (передача ионов Н+, ОН-, катализаторы: кислоты, основания, индифферентные растворы пропитанные ими).
-
Каталитические процессы с автокаталитическими реакциями (промежуточные продукты - катализаторы).
-
Различают положительный (, катализаторы) и отрицательный катализ (, ингибиторы).
Сущность ускоряющего или замедляющего воздействия катализатора заключается в изменении реакционного пути, в результате чего изменяется и энергия активации.
A+BR A+BR
Без катализатора С катализатором
A+BAB* A+kt↔Akt*
AB*R Akt*+BABkt*
 ABkt*kt+R
ABkt*kt+R
В промышленности основным видом каталитическокого процесса является гетерогенный катализ с использованием твёрдого катализатора или твёрдого носителя, пропитанного катализатором.
2.1. Характеристики катализаторов (на примере твёрдых).
-
Производителльность - количество продукта, полученное в единицу времени с единицы объёма катализатора.
-
А
 ктивность
- показывает насколько снижает катализатор
энергию активации ХР.
ктивность
- показывает насколько снижает катализатор
энергию активации ХР.
Чем больше снижается энергия активации, тем выше активность.
-
В
 ремя
контактирования. Различают фиктивное
и действительное время контактирования.
ремя
контактирования. Различают фиктивное
и действительное время контактирования.
 фикт
= VR/B,
с; на практике, как правило пользуются
фиктивным.
фикт
= VR/B,
с; на практике, как правило пользуются
фиктивным.
факт = Vфактkt, с.
-
Температура зажигания - минимальная температура при которой каталитический процесс идти с достаточной для практических целей скоростью (чем ниже температура, тем выше активность).
-
ИзбирательносЂь (селективность) - способность катализатора изберательно ускорять целевую реакцию при наличии нескольких побочных.
-
Механическая прочность - характеризует способность катализатора противостоять механическим воздействиям. Зависит от способа изготовления, от пористости зерна катализатора.
-
Отравляемость - снижение его активности под действием малых количеств веществ, называемых ядами (примеси исходных реагентов, продукты реакции). При отравлении катализатора на внешней и внутренней поверхности либо образуется химическое соедениние, либо происходит адсорбция, вследствии чего затрудняется доступ реагента к поверхности катализатора. Различают обратимую (возможна регенерация, при этом образовавшиеся на поверхности вещества удоляются и активность восстанавливается) и необратимую отравляемость катализатора. Яды: H2S, соединения As; синильная кислота.
Твёрдые катализаторы в промышлености чаще всего выпускают в виде таблеток, гранул, зёрен.
Твёрдый католизатор: смесь нескольких компонентов - собственно вещество катализатора (жидкости, Ме, оксиды Ме).
Трегеры (носители) - пористые индеферентные вещества на внутреннейц и внешней поверхности которых наносится катализатор (носители искусственные: кокс, керамика, силикагель{SiO2 в активной форме}; естественные: пемза, уголь каолин).
Промоторы (активаторы) - вещества будучи добавленными в незначительных количествах в катализатор резко повышают его активность.
Методы получения ктализаторов:
-
Осаждение гидроокисей с последующей формовкой зёрен, прокалкой, для придания им механической прочности - осаждённые катализаторы.
-
Совместное прессование порошков с получением катализатора в виде таблеток.
-
Сплавление нескольких веществ с последующей грануляцией и выщелачиванием - катализаторы скелетного типа.
-
Пропитка пористого носителя раствором, содержащим катализатор, с последующей сушкой и прокалкой.
