
- •Глава 7. Снотворные средства
- •7.1. Снотворные средства с ненаркотическим типом действия
- •7.2. Снотворные средства с наркотическим типом действия
- •Глава 8. Противоэпилептические средства
- •Глава 9. Противопаркинсонические средства
- •Глава 10. Вещества с анальгетической активностью
- •10.1. Опиоидные (наркотические) анальгетики
- •10.2. Неопиоидные средства центрального действия
- •10.3. Препараты смешанного действия
- •Глава 11. Аналептики
- •Глава 12. Психотропные средства
- •12.1. Нейролептики (антипсихотические средства)
- •12.1.1. Производные фенотиазина
- •12.1.2. Производные бутирофенона
- •12.1.3. Производные тиоксантена
- •12.1.4 «Атипичные» нейролептики
- •12.2. Антидепрессанты
- •12.2.1. Средства, угнетающие обратный нейрональный захват моноаминов
- •12.2.2. Ингибиторы моноаминоксидазы (ингибиторы мао)
- •12.2.3. «Атипичные» антидепрессанты
- •12.3. Соли лития
- •12.4. Анксиолитики (транквилизаторы)
- •3) Снотворный;
- •4) Противосудорожный,
- •12.5. Седативные средства
- •12.6. Психостимуляторы
- •12.7. Ноотропные средства (нейрометаболические стимуляторы)
- •22. Медиаторы центральной системы
- •24. Транквилизаторы и снотворные средства
- •25. Противоэпилептические средства
- •26. Препараты, применяемые при паркинсонизме
- •27. Антипсихотические средства — нейролептики
- •28. Средства, применяемые при аффективных состояниях. Антидепрессанты
- •29. Опиоидные (наркотические) анальгетики
- •31. Лекарственная зависимость и злоупотребление лекарствами
29. Опиоидные (наркотические) анальгетики
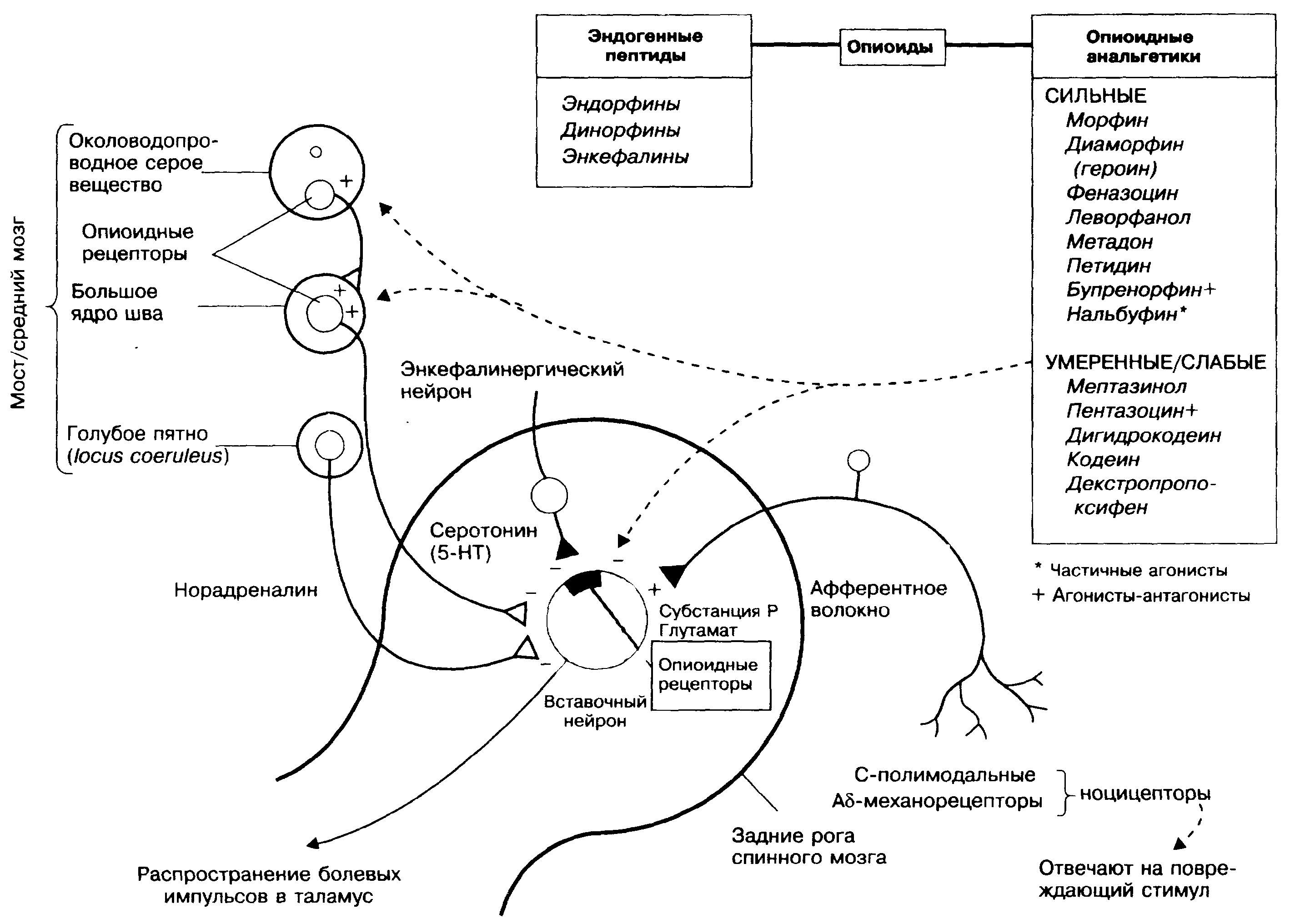
Болевые импульсы от ноцицепторов (болевых рецепторов) по первичным афферентным волокнам передаются в задние рога спинного мозга (пластинки 1 и II), где происходит их переключение на первый вставочный нейрон. Отсюда возбуждение распространяется через таламус к сенсорным зонам коры головного мозга. Практически ничего не известно о медиаторах, участвующих в проведении болевых импульсов, однако выявлено, что в окончаниях первичных афферентных волокон высвобождаются некоторые пептиды (например, субстанция Р, кальцитониноподобный пептид) (показано в нижней части рисунка).
Активность вставочных нейронов задних рогов спинного мозга регулируется несколькими ингибиторными механизмами. К ним относятся промежуточные нейроны, высвобождающие опиоидные пептиды (например, мет-энкефалины), окончания норадреналинергических и серотонинергических волокон, идущих от различных образований головного мозга (показаны в верхней части рисунка слева), которые активируются опиоид-ными пептидами. Опиоидные пептиды, высвобождающиеся как в головном, так и спинном мозге, понижают активность вставочных нейронов задних рогов спинного мозга и вызывают анальгезию (обезболивание). Каким образом осуществляется торможение болевых импульсов, неясно, известно лишь, что действие опиоидных пептидов опосредовано их влиянием на опиоидные рецепторы.
Опиоидные (наркотические) анальгетики — это средства (на рисунке справа), которые воспроизводят эффекты эндогенных опиоидных пептидов, активируя опиоидные рецепторы (в основном ц-рецепторы), что сопровождается развитием анальгезии, эйфории, ссдативного эффекта и угнетением дыхательного центра. Действуя на опиоидные рецепторы нервных сплетений кишечника, наркотические анальгетики могут вызвать запор (что в ряде случаев требует применения слабительных средств; см. главу 13). Действие опиоидов часто сопровождается появлением тошноты и рвоты (вследствие чего может возникнуть необходимость использования противорвотных средств). Длительное использование препаратов этой группы вызывает формирование лекарственной зависимости и развитие толерантности. Лечение болевого синдрома у безнадежно больных пациентов требует постоянного увеличения дозы наркотических анальгетиков, что, как правило, связано не с развитием толерантности, а с усилением боли. Развитие лекарственной зависимости в данной ситуации не имеет клинического значения. К сожалению, перестраховка в использовании опиоидов может быть причиной недостаточного контроля над болью.
Некоторые наркотические анальгетики (например, кодеин) обладают меньшей обезболивающей активностью, чем морфин. Применение этих препаратов в дозах, вызывающих выраженную анальгезию, сопровождается серьёзными побочными эффектами. Слабые наркотические анальгетики менее выражено угнетают дыхательный центр, лекарственная зависимость к этим средствам формируется реже. Слабые наркотические анальгетики применяют при болях средней интенсивности.
Специфическим антагонистом опиоидных рецепторов является налоксон, он устраняет угнетение дыхательного центра, вызванного наркотическими средствами. Налоксон может спровоцировать синдром отмены у пациентов с опийной лекарственной зависимостью. Препарат устраняет также обезболивающий эффект электроакупунктурной анальгезии и анальгезии, связанной с приёмом плацебо, что свидетельствует об участии эндогенных опиоидных пептидов в этих вядах обезболивания.
Опиоиды — это вещества, эффекты которых устраняются на-локсоном. Известно 3 семейства опиоидных пептидов, являющихся производными крупномолекулярных предшественников, кодирующихся отдельными генами. Проопиомеланокортин (ПОМК) является предшественником р-эндорфинов и некоторых неопиоидных пептидов, включая адренокортикотропный гормон (АКТГ). Проэнкефалин даёт начало лей-энкефалинам и мет-энкефалинам. Продинорфин является предшественником опиоидных пептидов, содержащих в своих окончаниях лей-энкефалины (например, динорфина А). Опиоидные пептиды, являющиеся производными различных предшественников, различаются по локализации в ЦНС и сродству к разным подтипам опиоидных рецепторов. Функции опиоидных пептидов в ЦНС точно не известны.
Опиоидные рецепторы. Опиоидные рецепторы широко распространены в ЦНС и подразделяются на 3 группы (ц-мю, к-каппа и 5-дельта). ц-рецепторы участвуют в процессах формирования боли; взаимодействие опиоидов с этими рецепторами вызывает развитие анальгезии. Концентрация ^-рецепторов в головном мозге невелика. Агонистами 5- и к-рецепторов являются, соответственно, энкефалины и динорфины. Активация к-рецепторов вызывает анальгезию, которая обычно сопровождается чувством дисфории (например, при применении пента-зоцина, нальбуфина), тогда как активация ц-рецепторов (например, морфином) вызывает анальгезию, сопровождающуюся эйфорией. Некоторые опиоидные анальгетики (например, пентазоцин) действуют на о-рецепторы, вызывая психостимулирующий и психозомиметический (галлюциногенный) эффекты (известно, что галлюциноген фенциклидин является агони-стом этих рецепторов), которые не устраняются введением на-локсона. Этот факт свидетельствует о том, что о-рсцспторы не являются опиоидными. Активация ц- и Й-рецепторов при участии G-белков приводит к увеличению проницаемости К^-ка-налов и вызывает гиперполяризацию мембран нейронов. Активация к-рецепторов уменьшает проницаемость Са^-каналов мембран нейронов. Опиоидные пептиды угнетают синаптичес-кую передачу в ЦНС и кишечнике.
Сильные опиоидные (наркотические) анальгетики
Эти наркотические анальгетики используют при сильных слабо локализованных болях со стороны внутренних органов. При локализованных болях меньшей интенсивности применяют слабые наркотические или ненаркотические анальгетики (не-стероидные противовоспалительные средства; см. главу 32). Для устранения сильной боли морфин вводят парентерально, перо-ральное применение морфина показано в терминальных стадиях заболеваний.
Морфин и другие наркотические анальгетики оказывают множество центральных эффектов. Кроме выраженной анальгезии наркотические анальгетики вызывают состояние эйфории, угнетение дыхательного и сосудодвигательного центров (что может привести к ортостатической гипотензии), оказывают седа-тивное действие, стимулируют триггерную хеморецепторную зону (вызывая тошноту и рвоту). Опиоиды стимулируют центр глазодвигательного нерва, вызывая сужение зрачка — миоз (исключением является петидин, обладающий слабой м-холиноб-локирующей активностью). Препараты угнетают кашлевой центр, однако выраженность этого эффекта не коррелирует с их опиоидной активностью. При применении наркотических анальгетиков возможны запоры, спазм жёлчных протоков и сфинктера Одди. Морфин может вызвать либерацию гистами-на, что приводит к расширению сосудов и появлению кожного зуда. Морфин метаболизируется в печени путём конъюгации с глюкуроновой кислотой, образуя неактивный морфин-3-глю-куронид и высоко активный морфин-6-глюкуронид.
При продолжительном применении опиоидных анальгетиков к ним развивается толерантность (т.е. привыкание — уменьшение чувствительности организма к лекарству). Такие побочные эффекты наркотических анальгетиков, как сужение зрачка и запоры, не уменьшаются при длительном их применении.
К опиоидным а.нальгетикам развивается психическая и физическая лекарственная зависимость, резкая отмена препаратов вызывает абстинентный синдром (см. главу 31).
Диаморфин (героин, диацетилморфин) в два раза активнее, чем морфин. В организме быстро превращается в активный метаболит 6-ацетилморфин и более медленно в морфин. При применении героина отмечается выраженная эйфория; тошнота, запор и артериальная гипотензия выражены слабее, чем при использовании морфина.
Метадон хорошо всасывается при приёме внутрь, оказывает продолжительное действие. Его применяют перорально в комплексной терапии опийной наркомании для предупреждения абстинентного синдрома («ломки»).
Петидин по своим свойствам напоминает морфин, но действует короче. При применении в дозах, вызывающих анальгезию, угнетает дыхательный центр, оказывает слабое противо-кашлевое действие и практически не вызывает развития запоров. Препарат высоко липофилен, поэтому его эффект развивается быстро. В печени петидин превращается в норпетидин, который может вызывать целый ряд побочных эффектов (например, расширение зрачка, судороги). При комбинированном применении с ингибиторами МАО петидин может вызывать появление делирия, повышение температуры тела, судороги и угнетение дыхания.
Бупренорфин — это частичный агонист ц-рецепторов, липо-фильный, эффективный при сублингвальном применении. Препарат действует продолжительнее, чем морфин. При его использовании возможно появление продолжительной рвоты. Бупренорфин прочно связывается с опиоидными рецепторами, поэтому налоксон практически не устраняет угнетение дыхания, вызванное применением препарата.
Нальбуфин (агонист к-рецепторов и антагонист ц-рецепторов) соответствует морфину по анальгезирующей активности и способности угнетать дыхательный центр; тошнота и рвота при его применении отмечаются реже. При использовании в высоких дозах вызывает дисфорию.
Слабые наркотические (опиоидные) анальгетики
Слабые наркотические анальгетики используют при болях умеренной интенсивности. Эти препараты вызывают лекарственную зависимость и могут быть объектами для злоупотреблений. Однако они вызывают слабую эйфорию, поэтому являются менее привлекательными для наркоманов.
Пентазоцин является слабым наркотическим анальгетиком, неприятным на вкус. При парентеральном введении оказывает обезболивающее действие (среднее между обезболивающим эффектом морфина и кодеина). Пентазоцин является агонис-том к- и 5-опиоидных рецепторов, но антагонистом ц-рецепто-ров. Препарат часто вызывает галлюцинации, кошмарные сновидения, расстройство умственной деятельности из-за активации о-рецепторов. Преимуществом препарата является его слабая способность вызывать лекарственную зависимость.
Кодеин (метилморфин) хорошо всасывается при перораль-ном введении, обладает слабым сродством к опиоидным рецепторам. Около 10% препарата диметилируется в печени в морфин, с которым преимущественно и связан его обезболивающий эффект. Побочные эффекты (запоры, рвота, угнетение ЦНС) не позволяют увеличивать дозу для достижения более сильного болеутоляющего эффекта. Кодеин используют в основном как противокашлевое и противопоносное средство.
Анальгезирующая активность декстропропоксифена выражена в 2 раза слабее, чем у кодеина. Препарат часто используют в комбинации с аспирином или парацетамолом, однако доказательств более высокой эффективности подобных комбинаций по сравнению с использованием только ненаркотических анальгетиков нет. Более того, при совместном применении этих препаратов увеличивается количество побочных эффектов, так как дскстропропоксифен вызывает угнетение дыхания и оказывает кардиодепрессивное действие, а парацетамол гепатотоксичен.
