
- •Тема 1. Реакционная способность веществ: химия и периодическая система элементов
- •Тема 2. Химическая связь, комплементарность
- •Тема 3. Химическая термодинамика. Энергетика химических процессов
- •Тема 4. Химическая кинетика. Химическое равновесие. Колебательные реакции
- •Тема 5. Химические системы: дисперсные системы, фазовое равновесие
- •Способы выражения концентрации растворов
- •Коллигативные свойства растворов
- •Тема 6. Электрохимические системы
- •Тема 7. Полимеры и олигомеры
- •Тема 8. Химическая идентификация
Тема 4. Химическая кинетика. Химическое равновесие. Колебательные реакции
Химическая кинетика - это раздел химии, изучающий скорости химических реакций и их механизм. Все химические взаимодействия можно разделить на гомогенные и гетерогенные.
Гомогенные реакции - это процессы, протекающие по всему объему смеси реагирующих веществ. Любая реакция, идущая в смеси газов, смеси жидкостей или в смеси жидких растворов является гомогенной. Например, если смешать газообразные водород и хлор, а затем эту смесь нагреть, то пойдет гомогенное взаимодействие по уравнению Н2 + Сl2 = 2НСl.
Гетерогенные реакции - это процессы, протекающие на границе раздела между взаимодействующими веществами. Например, горение углерода в кислороде является гетерогенным процессом: C + O2 = CO2 . Эта реакция протекает на поверхности раздела двух фаз (твердый углерод - газообразный кислород).
Скорость химической реакции - это количество элементарных актов химического взаимодействия за единицу времени. Для гомогенной реакции скорость (v) можно определить как изменение концентрации одного из исходных веществ или продуктов за единицу времени:
v =
![]() ,
,
где: С - изменение концентрации одного из веществ (исходного или продукта); t - промежуток времени, за который произошло это изменение.
Для гетерогенных реакций в данном определении параметр С следует заменить на (изменение количества вещества одного из реагентов или продуктов реакции). В приведенном выше уравнении имеет место модуль, т.к. скорость химической реакции не может быть отрицательной величиной.
Величина скорости гомогенной реакции определяется 4 факторами:
1. Природой реагирующих веществ.
2. Концентрацией реагирующих веществ.
3. Температурой.
4. Наличием в системе того или иного катализатора.
Природа реагирующих веществ.
Это, пожалуй, самый главный параметр, который определяет не только скорость взаимодействия, но и саму возможность протекания реакции. Так, например, цезий при соприкосновении с горячей водой взрывается. Литий взаимодействует с горячей водой достаточно активно, но без взрыва. С той же горячей водой магний взаимодействует очень вяло, а медь - вообще не взаимодействует. К сожалению, математическая зависимость скорости химической реакции от природы реагентов в настоящее время неизвестна. Поэтому, здесь можно рассуждать только на качественном уровне.
Концентрация реагирующих веществ.
Зависимость скорости реакции от концентрации выражается законом действия масс:
cкорость химической реакции прямо пропорциональна произведению концентраций реагирующих веществ, возведенных в степени, равные стехиометрическим коэффициентам (т.е. тем коэффициентам, которые пишутся в уравнении реакции перед формулами веществ).
nA + mB = An Bm ;
v = k [A]n [B]m ,
где v - скорость реакции при постоянной температуре; [A] - концентрация исходного вещества А (моль/дм3); [B] - концентрация исходного вещества В (моль/дм3); k - константа скорости реакции.
Константа скорости в уравнении закона действующих масс является константой только по одному параметру - концентрации. Величина константы скорости реакции определяется природой веществ А и В, температурой и катализатором (если он введен в систему). Другими словами, в константе скорости ”спрятана” зависимость скорости реакции от всех факторов, кроме концентрации реагирующих веществ.
Следует учесть, что приведенное выше уравнение является верным, если данное взаимодействие протекает в одну стадию. Если реакция идет через ряд промежуточных стадий, общая скорость реакции равна скорости самой медленной стадии процесса (для этого необходимо знать реальный механизм данного взаимодействия). В дальнейшем, для простоты, будем считать все рассматриваемые процессы одностадийными.
Примеры: 1) H2(г) + J2(г) = 2 HJ(г) (гомогенная реакция)
v1 = k1 [H2] [J2] .
2) 2 СO(г) + O2(г) = 2 СO2(г) (гомогенная реакция)
v2 = k2 [CO]2 [O2] .
3) C(т) + O2(г) = CO2(г) (гетерогенная реакция)
v3 = k3 [O2] .
В последнем примере концентрацию твердого углерода изменить нельзя (по сути, это его плотность, выраженная в единицах моль/дм3). Поэтому величина [С(т)] входит в константу скорости k3 .
Температура.
Скорость химической реакции очень сильно зависит от температуры, при которой происходит взаимодействие веществ: чем выше температура, тем быстрее идет это взаимодействие. Математически эта зависимость может быть задана двумя способами: правилом Вант-Гоффа и уравнением Аррениуса.
Правило Вант-Гоффа: cкорости большинства химических реакций увеличиваются в 2 - 4 раза при увеличении температуры на каждые 10 С.
(t2 - t1) / 10
v (t2) = v (t1) ,
где v (t1) - скорость реакции при температуре t1 ; v (t2) - скорость реакции при температуре t2 ; - температурный коэффициент Вант-Гоффа (показывает, во сколько раз увеличивается скорость данной реакции при t = t2 - t1 = 10 C); t1 и t2 - начальная и конечная температуры, при которых измерялась скорость реакции.
Правило Вант-Гоффа найдено экспериментально и не является законом. Температурный коэффициент () для большинства химических реакций имеет постоянное значение только в довольно узком интервале температур (как правило, t не более 100 С), за пределами которого заметно изменяется (увеличивается или уменьшается).
Точная зависимость скорости реакции от температуры задается уравнением Аррениуса:
k = A
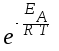 ,
,
где k - константа скорости реакции при температуре Т; A - постоянная, которая зависит только от природы взаимодействующих веществ; R - универсальная газовая постоянная; T - температура по шкале Кельвина (К); e - основание натурального логарифма (2,718); E A - энергия активации.
Уравнение Аррениуса является следствием теории активных соударений. По этой теории, не любое столкновение молекул взаимодействующих веществ приводит к образованию продуктов. Большинство частиц в момент соударения имеет суммарную кинетическую энергию меньше некоторого минимального значения, которое называется энергией активации (Е А). Столкновение частиц с энергией Е Е А не приводит к их взаимодействию и они разлетаются как упругие мячики после соударения друг с другом. Лишь малая часть молекул исходных веществ имеет суммарный запас энергии Е ЕА. В этом случае соударение будет неупругим (или активным) и в результате его могут появиться новые молекулы (продукты реакции).
Величина энергии активации зависит только от природы реагирующих веществ и наличия в системе какого-либо катализатора.
Катализ.
Допустим, взаимодействие между веществами А и В протекает со скоростью v0 по уравнению:
A + B = AB v0 .
Введем в данную систему некое вещество, которое в дальнейшем будем называть катализатором (К). Катализатор взаимодействует с веществом А со скоростью v1 :
A + K = AK v1 .
Промежуточный продукт (АК) взаимодействует с веществом В со скоростью v2:
AK + B = AB + K v2 .
Итак, в присутствии катализатора процесс протекает более сложным образом:
A
![]() AK
AK
![]() AB v3.
AB v3.
Cкорость такого взаимодействия (v3) равна скорости самой медленной стадии процесса (v3 = v1 или v3 = v2). Если v1 v0 и v2 v0, то v3 v0, другими словами произошло увеличение скорости химической реакции в присутствии катализатора. В этом случае катализатор называют положительным катализатором. Если наоборот, v1 и v2 меньше v0, то катализатор называют отрицательным катализатором или ингибитором.
Катализатор - это вещество, изменяющее скорость реакции (увеличивающее или уменьшающее), но не входящее в состав продуктов взаимодействия. Реакции, протекающие в присутствии катализаторов называются каталитическими, а явление изменения скорости реакции в присутствии катализатора называется катализом.
По сути дела, катализатор изменяет энергию активации данной реакции. Положительный катализатор (часто его называют просто катализатором) уменьшает энергию активации, а отрицательный (ингибитор) - увеличивает.
Действие катализатора носит специфический характер. Так, например, оксид ванадия V2O5 ускоряет только процессы окисления с участием молекул кислорода (О2). Положительные катализаторы и ингибиторы широко используются в промышленности и технике.
ХИМИЧЕСКОЕ И ФАЗОВОЕ РАВНОВЕСИЕ
Любая химическая реакция в принципе обратима, то есть может протекать как в прямом направлении (по уравнению - слева направо), так и в обратном (справа налево):
H2(г)
+ J2(г)
![]() 2 HJ(г)
.
2 HJ(г)
.
Если прямая реакция
протекает очень сильно, а обратная - в
очень малой степени, то такие реакции
называют практически необратимыми и
знак обратимости (![]() )
не ставят:
)
не ставят:
C(т) + O2(г) = СO2(г) .
Разложение оксида углерода (IV) на простые вещества - маловероятный процесс в обычных условиях и при нагревании до температур порядка 2000 С и поэтому процесс можно считать (условно) необратимой реакцией.
Рассмотрим взаимодействие между водородом и азотом, которое является типичным случаем обратимой реакции:
3H2(г)
+ N2(г)
![]() 2 NH3(г)
.
2 NH3(г)
.
Допустим, в начальный момент времени были смешаны некоторые количества газообразных Н2 и N2. По закону действующих масс, скорость их взаимодействия ( v1) равна:
v1= k1 [N2] [H2]3 .
Причем, v1 в момент смешивания будет максимальна, а по мере расходования исходных веществ постепенно будет убывать (см. рисунок).
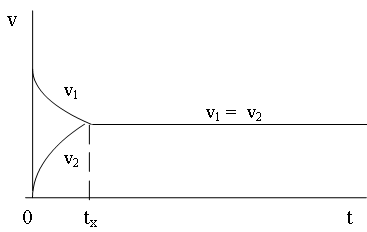
В начальный момент времени скорость обратной реакции (v2) равна нулю, т.к. аммиака в системе нет (концентрация его равна нулю):
v2 = k2 [NH3]2 .
Но по мере протекания реакции v2 начинает возрастать. Через некоторый промежуток времени tx скорости прямой и обратной реакции сравняются. Такое состояние системы называется химическим равновесием. При этом прямой и обратный процессы не прекращаются, хотя видимых изменений в системе нет. В течение 1 секунды из азота и водорода образуется N молекул аммиака, но за это же время N молекул аммиака распадается на азот и водород. Значит, концентрации [H2], [N2] и [NH3] остаются постоянными. Эти концентрации в состоянии равновесия называются равновесными концентрациями:
v1 = k1 [N2]р [H2] ,
v2 = k2 [NH3] .
v1 = v2 (состояние равновесия)
k1 [N2]р [H2] = k2 [NH3],
k1/
k2
=
Kp
=
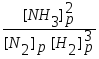 .
.
Отношение констант прямой и обратной реакции называется константой химического равновесия (Кр) .
Константа равновесия определяет соотношение концентраций исходных веществ и продуктов реакции в состоянии химического равновесия. Величина константы равновесия зависит только от природы реагирующих веществ и температуры. Константа равновесия не зависит от концентрации веществ, на нее не влияет катализатор (он изменяет энергию активации прямой и обратной реакции в одинаковой степени, поэтому отношение констант скоростей остается постоянным).
СМЕЩЕНИЕ ХИМИЧЕСКОГО РАВНОВЕСИЯ
Химическое равновесие является случаем устойчивого равновесия. Если система находится в состоянии устойчивого равновесия и на нее не оказываются внешние воздействия, она будет находиться в этом состоянии бесконечно долго.
Некоторые воздействия (изменение температуры, изменение концентрации одного из веществ, изменение давления) могут вывести систему из состояния равновесия. Но за счет того, что система находится в состоянии именно устойчивого равновесия, она самопроизвольно возвращается опять в состояние равновесия.
Принцип Ле-Шателье: если на систему, находящуюся в состоянии химического равновесия оказать какое-либо внешнее воздействие, выводящее ее из этого состояния, то в системе усилится тот процесс (прямая или обратная реакция), который возвратит систему в состояние равновесия.
Часто говорят о сдвиге (смещении) равновесия в системе: усиление прямой реакции приводит к смещению равновесия вправо (в сторону продуктов), а усиление обратной реакции смещает равновесие влево (в сторону исходных веществ).
Например, для обратимой реакции:
3H2(г)
+ N2(г)
![]() 2NH3(г)
+ Q .
2NH3(г)
+ Q .
Внешнее воздействие влияет на равновесие следующим образом:
|
Внешнее воздействие |
Смещение равновесия |
|
1. Увеличение концентрации одного из исходных веществ (Н2 или N2) |
1. Вправо |
|
2. Уменьшение концентрации одного из исходных веществ (Н2 или N2) |
2. Влево |
|
3. Увеличение концентрации продукта |
3. Влево |
|
4. Уменьшение концентрации продукта (NH3) |
4. Вправо |
|
5. Увеличение температуры |
5. Влево (т.к. эндотермической является обратная реакция) |
|
6. Уменьшение температуры |
6. Вправо (т.к. эндотермической является прямая реакция) |
|
7. Увеличение давления |
7. Вправо (т.к. в уравнении данной реакции слева 4 моль газообразных веществ, а справа только 2 моль). |
|
8. Уменьшение давления |
8. Влево (см. пункт 7) |
Любое смещение равновесия для данной системы можно доказать двумя способами: по принципу Ле-Шателье или исходя из понятия о константе равновесия.
Например: произошло увеличение концентрации молекул Н2 (в реакционный сосуд ввели некоторое дополнительное количество газообразного водорода).
1. По принципу Ле-Шателье должна усиливаться та реакция, в ходе которой концентрация Н2 уменьшается, то есть водород расходуется. Это прямая реакция, а значит равновесие смещается вправо.
2. До внешнего воздействия система была равновесной, то есть выполнялось равенство:
Kp
=
 .
.
После введения в систему дополнительного количества водорода концентрации всех веществ стали неравновесными, т.к.:
Kp
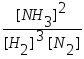 .
.
Чтобы система вернулась в состояние равновесия необходимо, чтобы увеличилась концентрация продукта (NH3) или уменьшились концентрации исходных веществ (H2 или N2). Если усилится прямая реакция, то произойдет и то и другое (концентрация NH3 увеличится, а концентрация H2 и N2 уменьшатся). Произойдет смещение равновесия вправо и концентрации веществ опять станут равновесными (но теперь уже будут иметь другие значения).
