- •400066, Волгоград, пл. Павших Борцов, 1
- •Правила по технике безопасности при работе в химической лаборатории
- •Глава 1. Номенклатура и изомерия органических соединений.
- •§ 1.1. Теория строения органических соединений а.М. Бутлерова.
- •Свойства вещества определяются не только их качественным и количественным составом, но и порядком соединения атомов в молекуле, т.Е. Химическим строением вещества.
- •Свойства органических соединений зависят не только от состава вещества и порядка соединения атомов в его молекуле, но и от взаимного влияния атомов и групп атомов друг на друга.
- •§ 1.2. Основы строения и реакционной способности оргаических соединений
- •§ 1.2.1. Общая характеристика органических соединений
- •§ 1.2.2. Классификация органических соединений
- •§ 1.2.3. Номенклатура.
- •§ 1.2.3.1. Заместительная номенклатура
- •Некоторые характеристические группы, обозначаемые только префиксами
- •Порядок старшинства характеристических групп, обозначаемых префиксами и суффиксами
- •Номенклатуре
- •§ 1.2.3.2. Радикально-функциональная номенклатура
- •Названия классов соединений, используемые в радикально-функциональной номенклатуре (в порядке убывания старшинства)
- •§ 1.3. Пространствеая структура биоорганических молекул. Виды изомерии
- •Глава 2. Электронное строение органических молекул. Кислотность и основность органических соединений.
- •§ 2.1. Пространственное строение органических соединений. Стереоизомерия
- •§ 2.2. Понятие о взаимном влиянии атомов в молекуле и электронные эффекты
- •Электронные эффекты заместителей
- •§ 2.3. Системы с замкнутой цепью сопряжения.
- •§ 2.4. Гетероциклические ароматические соединения.
- •§ 2.5. Кислотно-основные свойства органических соединений. Типы кислот и оснований. Определение понятий «кислота» и «основание».
- •§ 2.5.1. Кислоты и основания по Бренстеду
- •Значение рКа некоторых кислот Бренстеда
- •Основания Бренcтеда.
- •Величины рКа некоторых кислот и рКb сопряженных с ними оснований в разбавленных водных растворах
- •§ 2.5.2. Льюисовская кислотность и основность органических соединений.
- •§ 2.5.3. Концепция жестких и мягких кислот и оснований (принцип жмко)
- •Классификация кислот и оснований по Пирсону
- •Глава 3. Механизмы реакций органических соединений.
- •§ 3.1. Классификация органических реакций и их компонентов.
- •§ 3.2. Основные типы органических реакций
- •§ 3.3. Механизмы реакций в органической химии
- •§ 3.3.1. Реакции радикального замещения - sr
- •§ 3.3.2. Реакции нуклеофилъного замещения у тетрагонального атома углерода (sn)
- •§ 3.3.3. Реакции элиминирования ( е1 и е2).
- •§ 3.3.4. Реакции электрофильного присоединения, электрофильного замещения.
- •§ 3.3.5. Реакции нуклеофильного замещения, нуклеофильного присоединения ( реакции присоединения-отщепления).
- •Глава 4. Оксосоединения (альдегиды и кетоны).
- •§ 4.1. Общая характеристика реакционной способности
- •Альдегиды и кетоны
- •§4.2. Химические свойства альдегидов и кетонов.
- •§ 4.3. Альдегиды и их производные
- •§ 4.3. Лабораторный практикум.
- •Ход работы.
- •Глава 5. Карбоновые кислоты. Вопросы к занятию.
- •§ 5.1. Строение, номенклатура и физико-химические свойства карбоновых кислот
- •§ 5.2. Химические свойства предельных кислот и их производных
- •§ 5.3. Кислотно-основные свойства.
- •§ 5.4. Карбоновые кислоты как ацилирующие реагенты
- •Реакции декарбоксилирования
- •§ 5.5. Производные карбоновых кислот, их свойства и взаимные превращеия
- •Функциональные производные карбоновых кислоты
- •Сложные эфиры, имеющие приятный аромат
- •§ 5.6. Отдельные представители амидов кислот.
- •§ 5. 7. Дикарбоновые кислоты
- •Некоторые дикарбоновые кислоты, их названия и кислотные свойства
- •§ 5.8. Ненасыщенные карбоновые кислоты
- •Содержание высших ненасыщенных кислот в растительных маслах, % по массе
- •§ 5.9. Лабораторный практикум.
- •Инструкция по технике безопасности.
- •Ход работы.
- •Глава 6. Биологически активные гетерофункциональные соединения.
- •§ 6.1. Классификация поли- и гетерофункциональных соединений
- •§ 6.2. Общая характеристика реакционной способности
- •Специфические реакции.
- •§ 6.3. Аминоспирты
- •§ 6.4. Гидроксикарбоновые кислоты
- •§ 6.5. Оксокарбоновые кислоты
- •§ 6.6. Фенолокислоты. Особенности строения, свойства и биологическая роль.
- •Отдельные представители фенолокислот.
- •§ 6.7. Лабораторный практикум.
- •Ход работы.
- •Глава 7. Биологически активные гетероциклические соединения.
- •§ 7.1. Понятие о гетероциклических соединениях
- •§ 7.1.1. Пятичленные гетероциклы.
- •§ 7.1.2. Шестичленные гетероциклы.
- •§ 7.1.3. Бициклические гетероциклы.
- •§7.2. Лабораторный практикум.
- •Ход работы.
- •Глава 8. Аминокислоты, пептиды, белки
- •§ 8.1.Строение и свойства аминокислот.
- •§ 8.2. Пептиды.
- •§ 8.3. Качественные реакции на аминокислоты и белки.
- •§ 8.4. Физиологическая роль и применение в медицине некоторых аминокислот
- •§ 8.5. Белки
- •1. Каталитическая функция
- •7. Защитная функция
- •§ 8.6. Лабораторный практикум.
- •Ход работы:
- •Глава 9. Углеводы.
- •§ 9.1. Строение и свойства углеводов.
- •§ 9.1. 1. Классификация углеводов.
- •§9.1.2. Изомерия моносахаров.
- •§9.1.3. Химические свойства моносахаридов.
- •§ 9.2. Производные моносахаридов (дезоксисахара и аминосахара)
- •§ 9.3. Олиго- и полисахариды.
- •§ 9.3.1. Полисахариды.
- •§ 9.4. Гетерополисахариды
- •§ 9.5. Функции углеводов и их обмен
- •§ 9.6. Роль углеводов в развитии кариеса зубов
- •Контрольные вопросы
- •§ 9.7. Лабораторная работа «Свойства простых и сложных углеводов»
- •Глава 10. Нуклеиновые кислоты, их структура и свойства. Вопросы к занятию:
- •§ 10.1. Нуклеиновые основания, нуклеозиды, нуклеотиды.
- •§ 10.2. Нуклеотидный состав и структура днк и рнк.
- •§10.3. Биологические функции нуклеиновых кислот.
- •Контрольные вопросы
- •§ 10.4. Лабораторная работа. «Гидролиз нуклеиновых кислот»
- •Глава 11. Омыляемые и неомыляемые липиды.
- •§ 11.1. Липиды. Строение и классификация липидов
- •§ 11.2. Простые липиды
- •§ 11.2.1. Жиры
- •Константы некоторых жиров животного и растительного происхождения
- •§ 11.2.2. Воски
- •§ 11.2.3. Стериды. Стероиды и стероидные гормоны.
- •§11.2.4.Желчные килоты
- •Стероидные гормоны
- •§ 11.3. Сложные липиды
- •§ 11.4. Лабораторный практикум «Омыляемые и неомыляемые липиды. Терпеноиды и стероиды»
- •II. Некоторые свойства скипидара.
- •III. Качественные реакции на холестерин и жёлчные кислоты.
- •IV. Качественная реакция на витамин d2 (кальциферол).
- •Глава 12. Адсорбция на подвижной границе раздела фаз.
- •§ 12.1. Поверхностная энергия и поверхностное натяжение.
- •Поверхностное натяжение жидкостей на границе с воздухом (298 к)
- •§ 12.2. Поверхностная активность веществ.
- •§ 12.3. Адсорбция.
- •2. Изотерма Ленгмюра:
- •§12.4. Лабораторный практикум «Адсорбция поверхностно-активного вещества на границе раздела жидкость-воздух или жидкость-жидкость».
- •Ход работы.
- •Глава 13. Адсорбция на неподвижной границе раздела фаз. Изотерма адсорбции уксусной кислоты на угле.
- •§ 13.1. Адсорбция на границе твердое тело — раствор. Влияние различных факторов на величину адсорбции.
- •§ 13.1.1. Молекулярная адсорбция.
- •§13.1.2. Адсорбция сильных электролитов.
- •§13.2. Адгезия и когезия.
- •Задание для самостоятельной подготовки
- •Контрольные вопросы
- •§13.3. Лабораторный практикум.
- •Ход работы.
- •Глава 14. Физикохимия дисперсных систем
- •§ 14.1. Дисперсные системы и их классификация.
- •По размерам частиц дисперсной фазы
- •По агрегатному состоянию дисперсной фазы и дисперсионной среды:
- •По характеру взаимодействия дисперсной фазы с дисперсионной средой:
- •§ 14.2. Получение и устойчивость дисперсных систем
- •§ 14.3. Строение мицелл.
- •§ 14.4. Слюна как дисперсная система.
- •§ 14.5. Лабораторный практикум.
- •Ход работы.
- •Литература основная литература
- •Дополнительная литература
§ 6.5. Оксокарбоновые кислоты
Оксокарбоновыми кислотами называют соединения, содержащие одновременно карбоксильную и карбонильную группы. Они подразделяются на альдегидо- и кетонокислоты. Наиболее часто встречающиеся в живых системах оксокарбоновые кислоты приведены в табл. 18.
Таблица 18
Некоторые биогенные оксокарбоновые кислоты и их биологическая роль
|
Формула |
Название кислоты |
Название солей |
Биологическая роль кислоты |
|
|
Глиоксиловая |
Глиоксилаты |
Это единственная α-альдегидокислота. Встречается в недозрелых фруктах |
|
|
Пировиноградная |
Пируваты |
Важнейший промежуточный метаболит в живых системах |
|
|
Ацетоуксусная |
Ацетоацетаты |
Образуются в организме при β-окислении жирных кислот; накапливается при сахарном диабете |
|
|
Щавелевоуксусная |
Оксалоацетаты |
Метаболит, участвующий в цикле Кребса |
|
|
α-Оксоглутаровая |
α-Оксоглутараты |
Метаболит, участвующий в цикле Кребса и в синтезе глутаминовой и γ-аминомасляной кислот |
Оксокарбоновые кислоты в организме образуются при окислении соответствующих гидроксикарбоновых кислот путем их дегидрирования с помощью дегидрогеназ с окисленной формой кофермента НАД+:
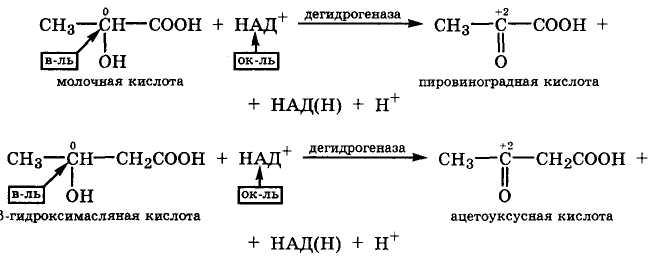
Оксокарбоновые кислоты сильнее, чем соответствующие гидроксикарбоновые кислоты. Поэтому в биосредах организма (рН ≈ 7) они обычно находятся в виде анионов.
Оксокарбоновые кислоты проявляют свойства, характерные и для кислот, и для карбонильных соединений. Специфические свойства этих кислот обусловлены взаимным влиянием карбонильной (>С=О) и карбоксильной (—СООН) групп. Наличие в их молекулах двух и более подобных электроотрицательных групп приводит к большей склонности этих соединений к реакциям окислительно-восстановительной дисмутации, как внутри-, так и межмолекулярным. В результате дисмутации происходит расщепление и образование различных связей, включая межуглеродные.
Реакции с расщеплением связи С—С. В растворе H2SO4 пировиноградная кислота подвергается внутримолекулярной дисмутации с расщеплением связи С—С: в разбавленной H2SO4 происходит декарбоксилирование, а в концентрированной — декарбонилирование:

Эти реакции наглядно демонстрируют различные окислительно-восстановительные свойства одних и тех же углеродных атомов в молекуле пировиноградной кислоты в зависимости от условий протекания реакции. По-видимому, в разбавленной H2SO4 в реакцию вступает ассоциат пировиноградной кислоты с Н3О+, а в концентрированной - катион этой оксокислоты.
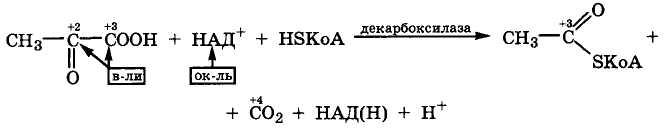
Аналогичная реакция окислительного декарбоксилирования превращает α-оксоглутарат в сукцинилкофермент А в цикле Кребса.
В отличие от α-оксокарбоновых кислот, декарбоксилирование β-оксокарбоновых кислот протекает легче. Так, ацетоуксусная кислота даже при комнатной температуре и в отсутствие H2SO4 самопроизвольно декарбоксилируется, превращаясь в ацетон:
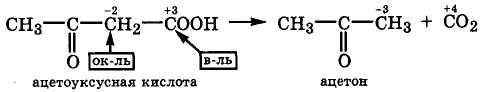
Этой реакцией заканчивается каждый цикл β-окисления жирных кислот.
Реакции с образованием связи С—С. Оксокарбоновые кислоты легко вступают в реакцию конденсации альдольного типа. При этом возникновение связи С—С происходит за счет присоединения (реакция AN) С-нуклеофила и протона (электрофила) по кратной связи карбонильной группы с образованием гидроксипроизводного дикарбоновой кислоты с разветвленным углеродным скелетом:
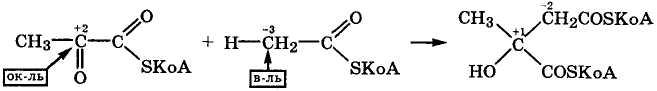
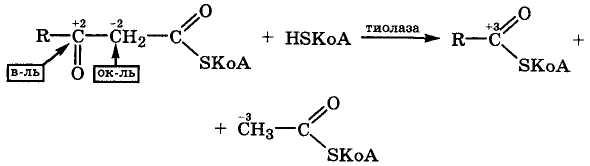
Как видно, это реакция межмолекулярной окислительно-восстановительной дисмутации, в которой углеродный атом карбонильной группы выступает окислителем. Подобная реакция протекает в цикле Кребса на стадии конденсации оксалоацетата с ацетилкоферментом А.
Образование связи С—С также происходит при карбоксилировании оксокарбоновых кислот. Так, в митохондриях гидрокарбонат-анион взаимодействует с пируватом при участии карбоксилазы и АТФ с образованием оксалоацетата и отщеплением воды:

Рассмотренные реакции свидетельствуют о том, что в оксокислотах углеродный атом карбонильной группы проявляет двойственность, выступая и восстановителем, и окислителем. Однако окислительные свойства для него более характерны, особенно в реакциях присоединения по карбонильной группе. Поэтому для оксокарбоновых кислот характерны реакции восстановления.
Реакция восстановления. Карбонильная группа оксокарбоновых кислот легко восстанавливается при реакциях гидрирования и трансаминирования.
Гидрирование. Пировиноградная кислота, возникающая в мышцах, при недостатке кислорода под действием гидрогеназы с коферментом в восстановленной форме гидрируется с образованием молочной кислоты:
![]()
Вследствие накопления молочной кислоты в работающих мышцах возникает характерная боль, которая проходит при отдыхе за счет накопления кислорода и окисления молочной кислоты обратно в пировиноградную. Подобное гидрирование оксокарбоновых кислот происходит при синтезе жирных кислот в организме.
Трансаминирование. Основным методом биосинтеза α-аминокислот из α-оксокислот является реакция трансаминирования, сопровождаемая межмолекулярной окислительно-восстановительной дисмутацией, при которой углеродный атом карбонильной группы выступает окислителем. Под действием трансаминазы с коферментом пиридоксальфосфатом α-оксокислота реагирует с α-аминокислотой, превращаясь в новую α-аминокислоту:

Трансаминирование в организме - обратимый процесс, за счет которого осуществляется взаимообмен оксо- и аминогрупп в биосубстратах.
Кето-енольная таутомерия. В оксокарбоновых кислотах и их производных значительно повышена протонная подвижность водородного атома, связанного с α-углеродным атомом относительно карбонильной группы. Это способствует переносу протона на кислородный атом соседней карбонильной группы с возникновением енольной формы, находящейся в равновесии с кетонной формой, т. е. прототропной таутомерии кето-енольного типа. Как уже говорилось, кето-енольная таутомерия сопровождается окислительно-восстановительной дисмутацией, при которой в кетотаутомере углеродный атом карбонильной группы выступает окислителем, а α-углеродный атом - восстановителем. В енольной форме эти углеродные атомы выполняют противоположные функции.
Оксокарбоновые кислоты в биологических средах (рН ≈ 7) находятся в виде анионов, поэтому кето-енольную таутомерию этих кислот в организме следует рассматривать на их анионах. И в этом случае кето-енольная таутомерия является сложным равновесием, включающим не только кетонный и енольный таутомеры анионов, но и их общий амбидентный анион, отрицательный заряд которого на единицу больше, чем у самих таутомеров. В соответствии с законами термодинамики таутомерное равновесие всегда смещено в сторону таутомера с более слабыми кислотными свойствами, а в присутствии сильного основания - в сторону амбидентного аниона. Следовательно, чем сильнее различаются по кислотности таутомеры, тем больше преобладает таутомер со слабыми кислотными свойствами. Так, для пирувата равновесие сильно (> 95 %) сдвинуто в сторону кетотаутомера:
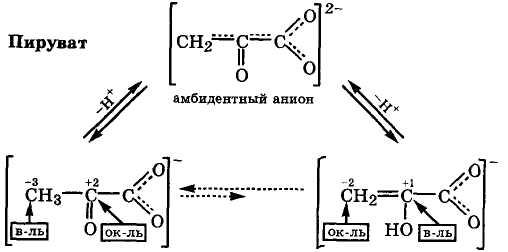
Напротив, для оксалоацетата енольный таутомер становится преобладающим (>80 %), поскольку он является устойчивым внутримолекулярным хелатом, образованным за счет водородной связи:
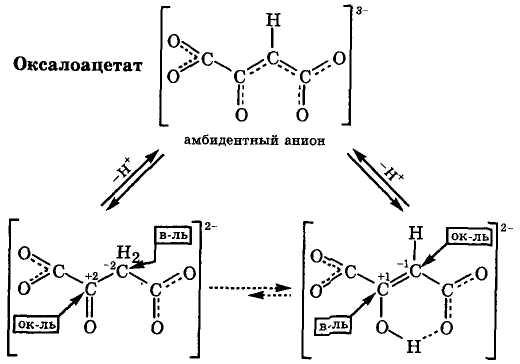
Перечисленные особенности реакционной способности таутомерных систем позволяют понять разнообразие химических свойств анионов оксокарбоновых кислот в условиях организма.
Анионы оксокарбоновых кислот и их производных легко ацилируются и алкилируются. При этом реакция может протекать и по углеродным, и по кислородным центрам, что широко используется при синтезе лекарственных препаратов.
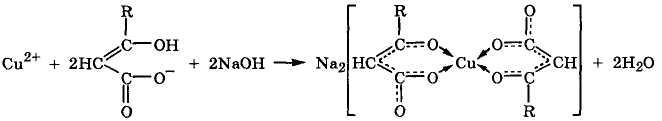
Комплексообразование. Оксокарбоновые кислоты являются активными ди- и полидентатными лигандами и поэтому образуют устойчивые хелаты с ионами-комплексообразователями: