
- •1.Материаловедение, как наука о строении и свойствах материалов, её основоположники
- •2.Кристаллическое состояние, типы кристаллических решеток, их параметры. Строение кристаллов. Анизотропия кристаллов, квазиизотропия свойств сплавов.
- •3.Металлографический метод изучения металлов.
- •4.Спец методы изучения сплавов (рентгеновский, микрорентгеноспектральный, фрактографический, радиографический).
- •5.Закономерности процесса кристаллизации
- •6.Строение слитка и факторы, на него влияющие
- •Превращения в твердом состоянии (аллотропические и магнитные превращения).
- •8.Типы структурных составляющих, присутствующих в металлических сплавах
- •9. Построение диаграмм состояния методом термического анализа.
- •10. Правила фаз и отрезков
- •11. Диаграмма состояния для сплавов, образующих механические смеси кристаллов двух компонентов
- •12. Диаграмма состояния для сплавов образующие неорганические твердые растворы.
- •18. Понятие о тройных диаграммах состояния.
- •19. Механические свойства материалов и методы их определения(твердость, прочность, пластичность, ударная вязкость).
- •20. Влияние деформации на структуру и свойства материала. Роль дефектов кристаллического строения в изменении прочности материала.
- •21. Процессы, происходящие при нагреве деформированных материалов( отдых, полигонизация, рекрестализация).
- •22. Диаграмма состояния железо – углерод, характеристики и свойства структурных составляющих.
- •23. Углеродистые стали, их классификация, маркировка. Влияние углерода и постоянных примесей на свойства сталей.
- •24.Конструкционные стали общего назначения ( стали обычного качества, качественные, высококачественные, листовые стали для холодной штамповки, автоматные стали).
- •25. Чугуны, их классификация, маркировка. Влияние углерода, постоянных примесей, скорости охлаждения на структуру и свойства чугунов.
- •26. Диаграмма состояния железо-графит, процесс графитизации.
- •27.Получение белого, серого, ковкого, высокопрочного чугунов, их структура, свойства применение.
- •28 Термическая обработка, ее параметры, методы осуществления.
- •29. Классификация видов термической обработки, их связь с диаграммами состояния.
- •30. Структурные превращения при термообработке стали и их классификация. Виды термообработки стали.
- •31. Превращение в стали при нагреве. Образование и рост аустенитного зерна.
- •32. Превращения в стали при охлаждении. Диаграмма изотермического превращения аустенита.
- •33.Мартенситное превращение и его особенности.
- •34. Превращение при отпуске закалённой стали.
- •35. Термомеханическая обработка стали.
- •36. Способы и параметры закалки стали. Прокаливаемость и закаливаемость. Поверхностная закалка сталей.
- •37. Отжиг и нормализация стали, их назначение и способы осуществления.
- •40. Классификация и маркировка легированных сталей.
- •41. Цементуемые и улучшаемые машиностроительные конструкционные стали, их термич-я обр-ка, св-ва и применения.
- •42. Рессорно-пружинные, шарикоподшипниковые стали, их термомобр-ка, св-ва и применение.
- •43. Инструментальные некрасностойкие стали для изготовления режущего инструмента, их обработка и св-ва. Быстрорежущие стали. Твердые сплавы.
- •44.Быстрорежущие стали. Твердые сплавы.
- •45. Инструментальные стали для оснастки холодного и горячего деформирования металлов, их термическая и химико – обработка, структура и свойства.
- •46. Жаропрочные, жаростойкие и нержавеющей стали, их термообработка, свойства и применение.
- •47. Высокопрочные мартенситно-стареющие стали.
- •48. Сплавы с заданным значением тепловых коэффициентов расширения и модуля упругости, магнитотвердые, магнитомягкие, немагнитные материалы.
- •49. Магнитотвердые, магнитомягкие, немагнитные материалы.
- •50. Алюминий и его сплавы, литейные и деформируемые алюминиевые сплавы, их назначение, термообработка и свойства.
- •51. Медь и ее сплавы. Латуни, бронза, их свойства,
- •52. Цинк, свинец олово, магний.
- •53. Тугоплавкие металлы, их использование в промышленных сплавах.
- •54. Полимерные материалы.
- •56. Силикатные материалы
- •Содержание
11. Диаграмма состояния для сплавов, образующих механические смеси кристаллов двух компонентов
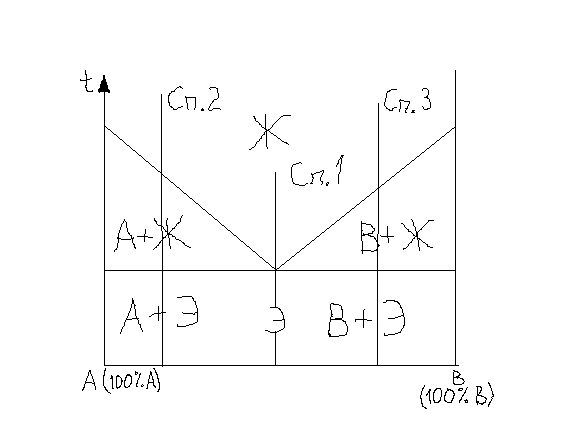 Ж
– жидкая фаза;
Ж
– жидкая фаза;
А и В – кристаллы чистых элементов;
Э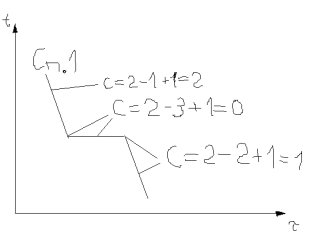 – эвтектика. Это механическая смесь
двух фаз. Смесь кристаллов А
и
В.
Кристаллы имеют мелкозернистое строение.
Эвтектика образуется в точке b
путем одновременного выделения кристаллов
этих двух фаз из жидкости.
– эвтектика. Это механическая смесь
двух фаз. Смесь кристаллов А
и
В.
Кристаллы имеют мелкозернистое строение.
Эвтектика образуется в точке b
путем одновременного выделения кристаллов
этих двух фаз из жидкости.
аbc – ликвидус; dbk – солидус (линия эвтектического превращения). По этой линии всегда для любых сплавов из жидкостей эвтектического состава выделяется эвтектика.
С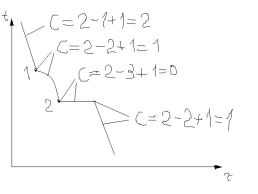 плавы,
лежащие левее точки b
наз доэвтектическими, правее –
заэвтектическими, а в точке b
– эвтектическими.
плавы,
лежащие левее точки b
наз доэвтектическими, правее –
заэвтектическими, а в точке b
– эвтектическими.
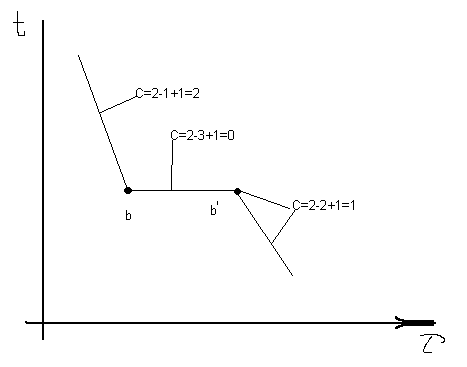
До точки b – охлаждение жидкой фазы. В точке b начинается процесс кристаллизации, при котором из жидкости выделяются кристаллы двух компонентов (A и B). Эта смесь наз эвтектикой. Идет процесс при пост t0С с выделением тепла на участке b-b’, так как С=0. В точке b’ жидкая фаза отсутствует. Появилась одна степень свободы, то есть t0C может уже уменьшаться. И ниже точки b’ равномерное охлаждение затвердевшего сплава на основе эвтектики.
В точке 1 начинается процесс кристаллизации с выделением кристаллов компонента А. На кривой охлаждения перегиб, так как изменяется число степеней свободы и процесс идет с выделением тепла. При охлаждении от точки 1 до точки 2 доля кристаллов А увеличивается, а состав жидкой фазы меняется по кривой 1b. В точке 2 оставшаяся жидкость имеет эвтектический состав. Из этой жидкости выделяется эвтектика. Эвтектическая кристаллизация на участке 2-2’ идет с выделением тепла при пост t0. В точке 2’ жидкой фазы уже нет, появляется одна степень свободы, сплав может охлаждаться при комн t0. При комн t0 сплав состоит из крупных кристаллов компонента A, образовавшихся между точкой 1 и 2, и эвтектики, в которую входят мелкие кристаллы компонента А и В.
Д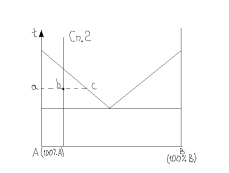 ля
сплава 3 такая же кривая охлаждения и
те же закономерности.
ля
сплава 3 такая же кривая охлаждения и
те же закономерности.
КЖ=(ab/ac)*100%; КА=(bc/ac)*100%;
12. Диаграмма состояния для сплавов образующие неорганические твердые растворы.
Линия ликвидус самая верхняя, после которой сплав в жидком состоянии. Линия солидус, ниже этой линии сплав в твердом состоянии.
Ж - жидкая фаза;
£ - неорганический твердый раствор. ( раствор замещения. Для реализации обр. неорг. тв. раст. Необходимы три условия:
Решетки одинаковые или очень близкие по строению.
атомные размеры -=-.одинаковая химическая природа.
С – число степеней свободы ( число внешних и внутренних факторов которые могут изменяться без изменения числа фаз в системе). Изменяется температура, состав при постоянном давлении. С=0. С=1. С=2(меняется и ŧ и состав.). К – число компанентов. Компоненты сплава это чистые химические элементы, или химические соединения.
Ф – число фаз. Фаза – часть системы (сплава) имеющая поверхность раздела при переходе через которую свойства меняются скачкообразно.
В данной диаграмме состояние закономерности могут рассматриваться через кривые охлаждения.
Д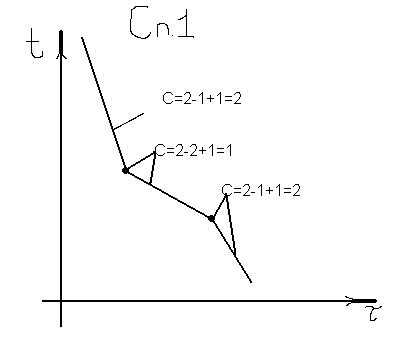 о
точки 1 равномерное охлаждение жидкой
фазы. В точке 1 начинается процесс
кристаллизации с выделением из жидкой
фазы кристаллов £ - фазы. Изменяется
число степеней свободы. На кривой
охлаждения появляется перегиб. Перегиб
свидетельствует о выделении тепла. От
точки 1 до точки 2 идет кристаллизация.
В точке 2 уже жидкой фазы нет. Следовательно
изменилось число степеней свободы –
опять перегиб на кривой охлаждения.
Процесс охлаждения идет быстрее так
как выделения Q.
Ниже точки 2 охлаждение сплава на основе
£ - фазы. Другой сплав аналогичное
описание.
о
точки 1 равномерное охлаждение жидкой
фазы. В точке 1 начинается процесс
кристаллизации с выделением из жидкой
фазы кристаллов £ - фазы. Изменяется
число степеней свободы. На кривой
охлаждения появляется перегиб. Перегиб
свидетельствует о выделении тепла. От
точки 1 до точки 2 идет кристаллизация.
В точке 2 уже жидкой фазы нет. Следовательно
изменилось число степеней свободы –
опять перегиб на кривой охлаждения.
Процесс охлаждения идет быстрее так
как выделения Q.
Ниже точки 2 охлаждение сплава на основе
£ - фазы. Другой сплав аналогичное
описание.
Применение правила отрезков:
Кж = вс/ас·100%; К£ = ав/ас·100%; состав жидкой фазы точка а. состав £ - фазы точка С. Если сплавы состоят из одной фазы то её 100% и отрезки применять не имеет смысла.
13. Диаграмма состояния для сплавов, образующие ограниченные твердые растворы с эвтектикой.
β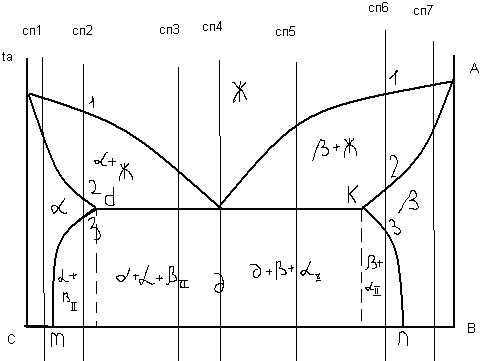
 и α ограниченные твердые растворы. dм
и Кn
– по этим линиям изменяется растворённость
элементов в твердых растворах. В связи
с этим выделяются вторичные фазы. По
линии dм
выделяется β фаза, по линии Кn
–выделяется £ фаза вторичная. Сплав 1
и сплав 7 имеют те же закономерности что
и рассмотренные.
и α ограниченные твердые растворы. dм
и Кn
– по этим линиям изменяется растворённость
элементов в твердых растворах. В связи
с этим выделяются вторичные фазы. По
линии dм
выделяется β фаза, по линии Кn
–выделяется £ фаза вторичная. Сплав 1
и сплав 7 имеют те же закономерности что
и рассмотренные.
Сп 2/СП 6
В точке 1 начинается процесс кристаллизации,
а в точке 2 заканчивается. От точки 2 до
точки 3 из £ фазы выделяются кристаллы
β фазы. При понижении температуры их
количество увеличивается. Для сплава
6 между точками 1 и точками 2 выделяются
кристаллы β фазы. Ниже точки 3 выделяются
кристаллы £ фазы.
точке 1 начинается процесс кристаллизации,
а в точке 2 заканчивается. От точки 2 до
точки 3 из £ фазы выделяются кристаллы
β фазы. При понижении температуры их
количество увеличивается. Для сплава
6 между точками 1 и точками 2 выделяются
кристаллы β фазы. Ниже точки 3 выделяются
кристаллы £ фазы.
Сп4. идет выделение как у чистого компонента.
В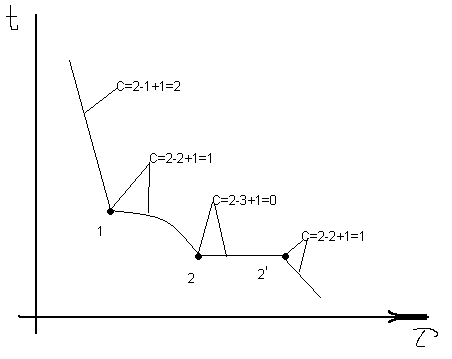 точке b
из из жидкости одновременно выделяются
кристаллы двух фаз β и £. Образующая
механическая смесь называется эвтектика,
а превращение называется эвтектическим.
(Превращение идёт с выделением тепла
при постоянном t
так как С=0). В точке b(штрих)
жидкой фазы нет и кристаллизация
закончилась. Появилась одна свобода и
температура может уменьшаться.
точке b
из из жидкости одновременно выделяются
кристаллы двух фаз β и £. Образующая
механическая смесь называется эвтектика,
а превращение называется эвтектическим.
(Превращение идёт с выделением тепла
при постоянном t
так как С=0). В точке b(штрих)
жидкой фазы нет и кристаллизация
закончилась. Появилась одна свобода и
температура может уменьшаться.
Сп 3 – доэвтектический.
В точке 1 начинается выделение кристаллов £ фазы, на кривой охлаждения перегиб свидетельствует о выделении тепла. Между точками 1 и 2 продолжается процесс кристаллизации с выделением £ фазы. При этом состав жидкой фазы имеет эвтектический состав. И эта остаточная жидкость претерпевает эвтектическое превращение, которое идет на участке 2-2(штрих) при постоянной температуре с выделением тепла. В точке 2(штрих) кристаллизация закончилась, появляется одна степень свободы и сплав начал охлаждаться Ниже точки 2(штрих) из £ фазы выделяется β фаза вторичная. Сплав 5 имеет кривую охлаждения подобную сплаву 3. между точками 1 и 2 из жидкости β фаза. Ниже точки 2 из β фазы выделяется £ фаза вторичная.
При t=t1 в точке а в равновесии две фазы β и £
Количество £ фазы: К£=ас/вс·100%.
Количество Ж фазы: Кж=ва/вс·100%.
Состав жидкой фазы – точка С.
Состав £ фазы – точка в.
А в целом состав сплава точка а.
При t=t1 в точке а в равновесии две фазы β(вторичная) и £
t2 Кж=fe/eo·100%. К£=ео/fo·100%.
Состав β фазы – точка o.
Состав £ фазы – точка f.
14. Диаграмма состояния для сплавов, образующие ограниченные твердые растворы с перитектикой.
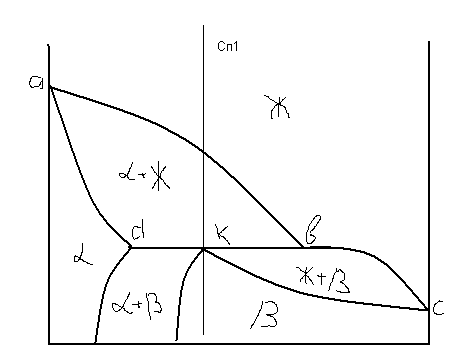
dkb – перитектическое превращение. Жидкая фаза в взаимодействии с ранее образовавшейся α фазой даёт образование β фазы.

15. Диаграмма состояния сплавов образующих химические соединения(без твердых растворов). 11
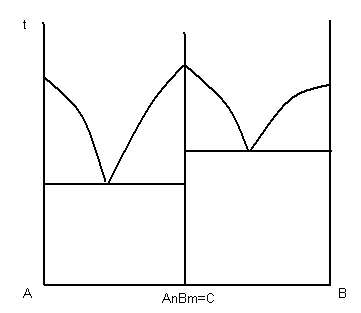
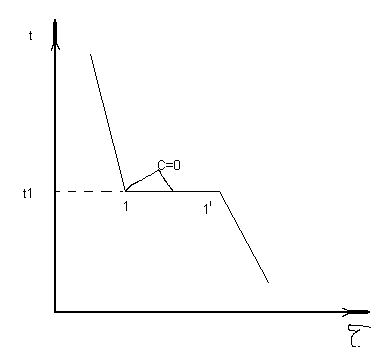
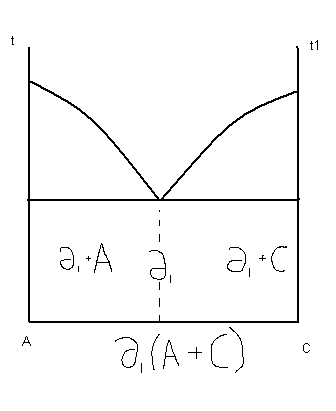
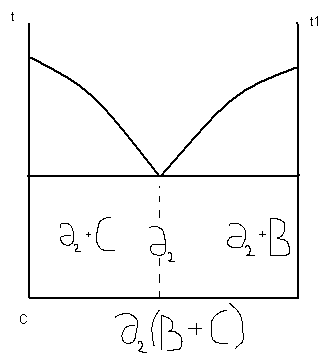
16. Диаграмма для сплавов с полиморфными превращенными .
Полиморфные превращения – при которых имеют место изменения кристаллической решетки в твердом состоянии. Магнитные превращения – изменения в строении электронных оболочек, в результате чего металл приобретает ферромагнитные свойства. Железо имеет и полиморфные превращения и магнитные.
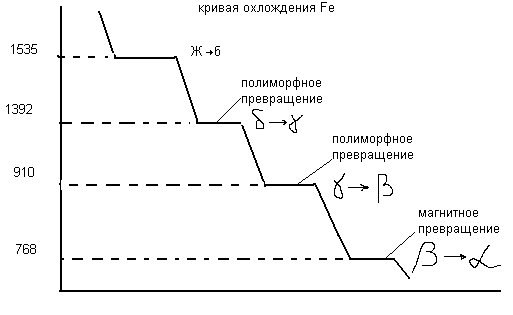
δ, β, £ - Fе с ОЦК решеткой.
γ – Fе с ГЦК решеткой.
Только £ - железо ферромагнитное.
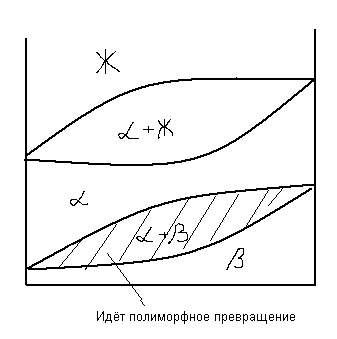
17. Связь между свойствами сплавов и типом диаграмм.
Как известно, вид диаграммы состояния зависит от того, какие фазы образуют оба компонента. Свойства сплава также зависят от того, какие соединения или какие фазы образовали компоненты сплава.
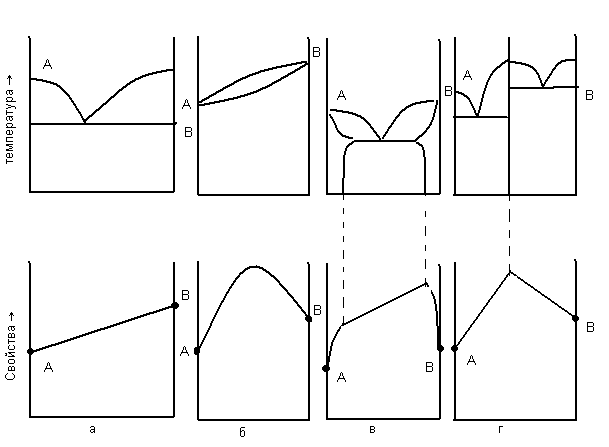
Поэтому очевидно, что между видом диаграммы состояния и свойствами сплава должна существовать определенная связь. На рисунке приведены четыре основных типа диаграмм состояния и соответствующие им закономерности изменения свойств сплава с изменением концентрации:
