
- •ПРЕДИСЛОВИЕ ПЕРЕВОДЧИКА
- •ПРЕДИСЛОВИЕ
- •СПИСОК СОКРАЩЕНИЙ
- •1. Введение
- •1.1. Освещение по Кёлеру
- •1.1.1. Принципы метода
- •1.1.2. Предварительная проверка оборудования
- •1.2. Установка света по Кёлеру
- •2.1. Преломление
- •2.1.1. Числовая апертура
- •2.2. Отражение, поглощение и пропускание
- •2.3. Флуоресценция/фосфоресценция
- •2.4. Поляризация
- •2.5. Дифракция
- •2.5.1. Тестовые пластинки Аббе
- •2.5.2. Формирование первичного изображения
- •2.5.3. Разрешающая способность
- •2.5.4. Роль конденсора в разрешении микроскопа
- •2.5.5. Увеличение
- •2.5.6. Увеличение и разрешение
- •4. Поле зрения
- •5. Резюме
- •6. Литература для дальнейшего чтения
- •1. Введение
- •1.1. Определение контраста
- •2. Светлопольная микроскопия
- •3. Фазовый контраст
- •3.2. Дифрагированный свет в фазовом контрасте
- •4. Темнопольная микроскопия
- •4.1. Освещение по Рейнбергу
- •4.2. Темнопольные конденсоры высокого разрешения
- •4.3. Темнопольное изображение
- •5. Поляризованный свет
- •5.1. Использование одиночного поляризатора
- •5.2. Использование скрещенных поляризаторов
- •5.2.2. Направление двулучепреломления
- •6.3. Интерференционная отражательная микроскопия
- •6.3.2. Физические основы метода
- •6.3.3. Интерпретация результатов
- •7.1. Красители
- •7.2. Использование светофильтров
- •7.3. Срезы
- •7.4. Качество препарата
- •8. Другие методы
- •8.1. Дисперсионное окрашивание
- •10. Благодарности
- •11. Литература
- •ФИКСИРОВАНИЕ ИЗОБРАЖЕНИЯ
- •1. Введение
- •2. Рисование
- •3. Фотомикрография
- •4.1. Разрешение
- •4.2. Разрешающая способность и размер отпечатка
- •4.4. Освещение
- •5. Микроскоп для фотомикрографии
- •5.1. Штатив микроскопа
- •5.2. Оптика
- •5.2.1. Числовая апертура и увеличение объективов
- •5.2.2. Исправление аберраций
- •5.2.4. Иммерсионные объективы
- •5.2.5. Глубина резкости
- •5.2.6. Кривизна поля зрения
- •5.2.7. Типы конденсоров
- •5.2.8. Чистка линз
- •6. Камера для фотомикрографии
- •6.1. Выбор размера пленки
- •6.3. Специальная фотомикрографическая камера
- •6.4. Микроскопы со встроенными фотосистемами
- •6.5. Камера с мехами
- •7. Наведение на фокус и определение экспозиции
- •7.1. Наведение на фокус
- •7.2. Определение экспозиции
- •7.3. Контроль экспозиции
- •8. Выбор условий для фотомикрографии
- •8.1. Фотографический процесс
- •8.1.1. Чувствительность пленки
- •8.1.2. Зернистость
- •8.1.3. Контрастность
- •8.2. Черно-белая фотомикрография
- •8.3. Цветная фотомикрография
- •8.3.1. Цветные отпечатки или слайды
- •8.3.2. Печать со слайдов
- •8.3.3. Цветовая температура
- •8.3.4. Коррекция цветовых искажений
- •8.3.6. Выбор чувствительности пленки
- •8.4. Поляроидные клетки
- •8.4.2. Камера Поляроид SX70
- •8.4.3. Поляроидные слайды
- •8.5. Хранение неэкспонированной пленки
- •9. Фотомакрография
- •9.1.1. Стереомикроскопы для фотомикрографии
- •9.1.2. Макроскопы
- •9.1.3. Фотомакрографические объективы
- •9.2. Освещение для фотомакрографии
- •9.3. Определение экспозиции при фотомакрографии
- •10. Завершение процесса фотомикрографии
- •10.1. Содержание записей
- •10.2. Хранение негативов
- •10.3. Хранение слайдов
- •10.4. Монтаж слайдов
- •10.5. Хранение отпечатков
- •10.6. Определение и указание увеличения
- •11. Практическое руководство
- •11.2. Начальная калибровка экспонометра
- •12. Литература для дальнейшего чтения
- •ИММУНОГИСТОХИМИЯ
- •1. Введение
- •2. Антитела
- •2.1. Структура иммуноглобулинов
- •2.2. Поликлональная антисыворотка
- •2.3. Моноклональные антитела
- •2.4. Очистка антител
- •2.5. Специфичность реакций антител
- •2.6. Хранение антител
- •3.1. Выбор условий обработки ткани
- •3.2. Выявление скрытых антигенов
- •4. Выбор способа мечения
- •4.1. Флуоресцентные метки
- •4.2. Ферментные метки
- •4.2.1. Пероксидаза хрена
- •4.2.2. Щелочная фосфатаза
- •4.2.3. Глюкозооксидаза
- •4.2.4. Галактозидаза
- •4.3. Коллоидное золото
- •4.4. Выбор метки
- •5. Методы окраски
- •5.1. Прямой метод
- •5.2. Непрямой метод
- •5.4. Системы с использованием биотин — авидина
- •5.5. Другие методы
- •6. Экспериментальные методы
- •6.1. Общее описание метода
- •6.2. Выбор правильного разведения антител
- •6.3. Флуоресцентные метки
- •6.4. Пероксидаза
- •6.4.1. Ингибирование эндогенного фермента
- •6.5. Щелочная фосфатаза
- •6.5.1. Блокирование эндогенного фермента
- •6.5.2. Мера предосторожности
- •6.6. Глюкозооксидаза
- •6.7. Галактозидаза
- •6.9. Некоторые общие процедуры
- •6.9.1. Покрытие предметных стекол
- •6.9.2. Дополнительное окрашивание
- •7.1. Контрольные препараты
- •7.2. Решение проблем
- •9. ДНК-зонды для гибридизации in situ
- •9.1. Принцип метода гибридизации
- •9.2. Экспериментальная процедура
- •9.2.1. Выявление Y-хромосомы
- •9.2.2. Выявление цитомегаловируса
- •10. Цитологические препараты
- •11. Количественная оценка
- •12. Оборудование
- •13. Благодарности
- •14. Литература
- •ГИСТОХИМИЯ И СВЕТОВАЯ МИКРОСКОПИЯ
- •1. Введение
- •1.1. Объекты для гистохимического окрашивания
- •1.1.1. Что такое окрашивание?
- •2. Приготовление и хранение срезов препаратов
- •2.1. Необходимые характеристики препарата
- •2.2. Методы приготовления и хранения препаратов
- •2.2.1. Получение тонких слоев
- •3. Что можно выявлять? Некоторые примеры
- •3.1. Выявление химических свойств
- •3.1.1. Химические фрагменты
- •3.1.2. Специфические вещества
- •3.1.3. Классы веществ
- •3.2. Выявление биологических объектов
- •3.2.1. Биологические объекты
- •3.2.2. Биологические процессы
- •3.3. Морфологические исследования
- •4. Выбор методов
- •5.1. Оценка селективности методов
- •5.2. Оценка локализации окрашивания
- •5.4. Оценка чистоты реагентов
- •5.5. Номенклатура реагентов
- •6. Что необходимо для гистохимической работы
- •6.1. Оборудование и материалы
- •6.2. Как научиться работать?
- •7. Почему используются гистохимические методы
- •8. Благодарности
- •ФЛУОРЕСЦЕНТНАЯ МИКРОСКОПИЯ
- •1. Введение
- •2. Флуорохромы
- •3. Флуоресцентный микроскоп
- •3.1. Способы освещения
- •3.1.1. Освещение проходящим светом
- •3.1.2. Освещение падающим светом
- •3.2. Источники света
- •3.3. Домики для ламп
- •3.4. Фильтры
- •3.4.1. Возбуждающие фильтры
- •3.4.2. Запирающие фильтры
- •3.4.3. Цветные светоделительные зеркала
- •3.5. Объективы и окуляры
- •4. Применение флуоресцентных красителей
- •4.1. Нуклеиновые кислоты
- •4.1.1. Прижизненное окрашивание флуорохромами
- •4.2. Иммунофлуоресценция
- •4.3. Флуоресценция нейромедиаторов
- •4.4. Двойное окрашивание
- •5. Микрофлуориметрия
- •5.1. Введение
- •5.2. Стандарты флуоресценции
- •5.3. Оборудование
- •5.3.1. Инвертированные микрофлуориметры
- •5.3.2. Сканирующие микрофлуориметры
- •5.4. Измерения содержания ДНК
- •5.4.1. Оборудование
- •5.4.2. Подготовка материала
- •5.4.3. Процедура окрашивания
- •5.4.4. Проведение измерений
- •6. Анализ изображения при флуоресценции
- •7. Сканирующая лазерная микроскопия
- •8. Литература
- •МИКРОМЕТРИЯ И АНАЛИЗ ИЗОБРАЖЕНИЯ
- •1. Введение
- •2. Простая микрометрия
- •2.1. Измерения длины
- •2.1.3. Окуляр-микрометр сдвига
- •2.1.4. Другие методы измерения длины
- •2.2 Измерения углов
- •2.3. Измерение толщины
- •2.4. Счетные камеры
- •2.4.2. Техника работы с гемоцитометром
- •3.1.1. Определение АA в двухфазном препарате
- •3.2. Принципы измерения площади поверхности
- •4. Измерения с использованием дигитайзера
- •5.2. Измерения с помощью компьютера
- •6. Приборы и математическое обеспечение работ
- •7. Литература
- •ВИДЕОМИКРОСКОПИЯ
- •1. Видеомикроскопия и оборудование для нее
- •1.1. Введение
- •1.1.1. Видеоусиление
- •1.1.2. Видеоинтенсификация
- •1.1.3. Цифровая обработка изображения
- •1.2.1. Условия ограниченного числа фотонов
- •1.3. Различные методы видеомикроскопии
- •1.3.1. Видеомикроскопия с усилением
- •1.3.2. Аналоговое усиление контраста
- •1.3.3. Цифровая обработка изображения
- •1.4.1. Камеры и контроллеры камер
- •1.4.5. Видеопроцессорные платы
- •1.4.6. Монофункциональные процессоры
- •1.4.7. Взгляд в будущее
- •1.5. Условия, налагаемые на микроскоп
- •1.6. Как соединить телекамеру с микроскопом
- •2.1. Различные виды VEC-микроскопии
- •2.2. Приготовление препаратов
- •2.3. Получение изображения
- •2.4. Интерпретация изображений
- •2.5. Типичные применения и ограничения метода
- •2.5.1. Светлопольная микроскопия
- •2.5.2. Темнопольная микроскопия
- •2.5.4. Фазовый контраст
- •2.5.5. Поляризационная микроскопия
- •2.5.7. Отражательная контрастная микроскопия
- •2.5.8. Флуоресцентная микроскопия
- •2.5.9. Примеры применения в биологии и биохимии
- •3.1. Введение
- •3.2. Процесс формирования изображения
- •3.2.1. Условия, касающиеся микроскопа
- •3.2.2. Получение статических изображений
- •3.2.3. Получение изображений подвижных объектов
- •3.3. Типичные приложения
- •3.3.2. Картирование отношений
- •3.3.4. Визуализация молекул
- •3.3.6. Люминесценция
- •3.3.7. Нейробиология
- •4.1. Пространственные измерения
- •4.2. Измерения по интенсивности
- •5.1. Видеозапись и редактирование
- •5.1.1. Стандарты видеотехники
- •5.1.2. Форматы видеопленок
- •5.1.3. Качество видеопленок
- •5.1.4. Видеомагнитофоны
- •5.1.5. Видеомагнитофоны с цейтраферной записью
- •5.1.6. Запись при видеомикроскопии
- •5.1.8. Копирование и редактирование видеозаписей
- •5.2.1. Оборудование
- •5.3. Перенос видеозаписей в видеофильм
- •5.4. Рисование с монитора
- •6. Благодарности
- •7. Литература
- •1. Введение
- •2. Классификация сегментов хромосом
- •2.1. Гетерохроматиновые сегменты
- •2.2. Эухроматиновые сегменты
- •2.3. Ядрышковые организаторы
- •2.4. Кинетохоры
- •4.2. G-окрашивание
- •4.2.1. ASG-метод
- •4.2.3. Метод Галлимора и Ричардсона
- •4.3. R-окрашивание
- •4.4. Q-окрашивание
- •4.4.1. Q-окрашивание с помощью акрихина
- •4.5.2. Процедура окраски
- •5.1. Окрашивание ДАФИ/дистамицином
- •5.2.1. Метод культивирования клеток
- •5.2.2. Методика окраски
- •5.3.2. Синхронизация с помощью БУДР [39]
- •5.3.3. Синхронизация с помощью ФУДР [13, 40]
- •6. Наблюдение и регистрация сегментов хромосом
- •6.3. Фотографирование сегментированных хромосом
- •6.4.1. Получение профилей сегментов
- •6.4.2. Отражательная микроскопия
- •6.4.3. Измерение полиморфизма хромосом
- •7. Благодарности
- •8. Литература
- •9. Литература для дальнейшего чтения
4.2.3. Ограничения конденсоров темного поля высокого разрешения
В некоторых случаях при работе с темнопольными конденсорами и заранее приготовленными препаратами возникают трудности. Причина, как уже должно быть ясно читателю, состоит в том, что расстояние до вершины конуса падающего света слишком мало для того, чтобы эта вершина могла оказаться внутри образца, который смонтирован на толстом стекле. В такой ситуации не остается ничего другого, как поискать относительно редкий тип фокусируемого темнопольного конденсора. В противном случае придется перезаключать препарат, используя более тонкое предметное стекло.
Другое ограничение метода темнопольной микроскопии состоит в том, что в поле зрения оказывается слишком много деталей, таких, как пузырьки воздуха или инородные частицы, которые ухудшают изображение. Таким образом, данный метод лучше всего использовать для изучения мелких дискретных структур, достаточно удаленных друг от друга.
4.3. Темнопольное изображение
Темнопольное изображение создается рассеянным светом и, таким образом, представляет собой карту изменений коэффициента преломления и других светорассеивающих параметров препарата.
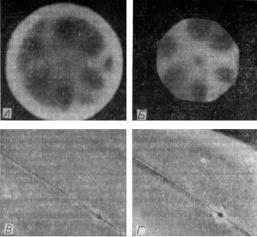
Рис. 2.2. Роль света нулевого порядка в формировании изображения: изображение P. angulatum в темном поле. А. З.ф.п. объектива с NA 1,3 при открытой диафрагме, когда яркий свет нулевого порядка участвует в формировании изображения. Б. Тот же объектив, что и в Л, но диафрагма закрыта, что исключает свет нулевого порядка. Обратите внимание на дифракционный спектр первого порядка, который имеет вид пересекающихся полукружий. В. Изображение, получающееся при установке света, как в случае Л. Детали разрешены, но трудно различимы. Г. Изображение, получающееся при установке света, как в случае Б. Детали вновь разрешены, но видны значительно лучше, чем в В. Заметьте, что детали разрешены и в A, и в Б но видны гораздо лучше в Б. Увеличение на В и Г Х900.
5. Поляризованный свет
Данный раздел познакомит вас с методами получения контраста, основанными на поляризации света. Однако его не следует рассматривать как введение в кристаллографию.
Световые волны колеблются во всех направлениях, перпендикулярных оси распространения луча. Плоскополяризованный свет представляет собой такой свет, колебания в котором происходят только в одной плоскости, перпендикулярной направлению распространения луча. Такой свет можно получить, отфильтровав от обычного света все колебания, за исключением происходящих вдоль одного разрешенного направления.
Таблица 2.9. Плеохроизм
1.Поместив поляризатор в ход лучей перед препаратом, получите плоскополяризованный свет.
2.Глядя на большинство образцов, освещенных таким образом, вы вряд ли заметите большие различия, если не считать некоторого снижения интенсивности света. Это происходит потому, что большинство биологических препаратов пропускают свет одинаково, вне зависимости от направления плоскости его колебаний. Такие материалы называются изотропными.
3.Поверните препарат, а если это невозможно — поверните поляризатор. Если препарат изотропный, то никаких изменений в интенсивности света или в окраске его в результате вращения не произойдет.
4.Если возможно, исследуйте пластинку слюды, достаточно тонкую для того, чтобы она была прозрачной (очень подходящим является также геологический шлиф турмалинового кварца). Вращайте препарат, как указано выше, и при этом отметьте изменения цвета каких-либо линейных структур в препарате (разд. 5.1).
27

Таблица 2.10. Проверка скрещения поляризаторов
1.Установите в микроскопе обычным образом освещение по Кёлеру.
2.Вставьте поляризатор.
3.Уберите препарат.
4.Поместите второй кусочек поляризатора поверх окуляра.
5.Вращая второй поляризатор, который теперь называется анализатором, добейтесь минимальной интенсивности света. Данное конкретное расположение поляризаторов является скрещенным. Отметьте каким-либо способом их относительное расположение и, если возможно, установите таким образом, чтобы разрешенная плоскость колебаний поляризатора была ориентирована в направлении восток — запад.
Для этих целей вполне подходит поляроид, который дает достаточное качество поляризации света для большинства приводимых здесь упражнений. В табл. 1.4 приведен метод для определения разрешенного направления колебаний в куске поляроида.
Некоторые простые упражнения, приведенные в табл. 2.9— 2.12, позволят вам понять на практике, как поляризованный -свет взаимодействует с веществом и как это взаимодействие может быть использовано для достижения контраста в световой микроскопии.
5.1. Использование одиночного поляризатора
Техника получения контраста при использовании плоскополяризованного света приводится в табл. 2.9 под заголовком «Плеохроизм».
Из табл. 2.9 вы можете видеть, что частичка слюды при одной ориентации будет слегка серой, а повернутая под прямым углом — темно-желтой.
Рис. 2.3. Получение контраста в микроскопии с помощью поляризованного света. Одиночный поляризатор и плеохроизм: А — молекула конго-рот и Б — молекула метиленового синего (стрелками указано направление колебаний света, вдоль которого поглощение света велико). Размеры даны в нм. Скрещенные поляризаторы и двулучепреломление: В — стержни (nr) и Г — пластинки (ni), лежащие в среде (nm), Д — изменение величины двулучепреломления (nε - nω) ПРИ изменении показателя преломления среды (nm), как в В и Г. Линии соответствуют: 1—положительной форме двулучепреломления; 2— положительной форме двулучепреломления и положительному двулучепреломлению на кристалле; 3 — отрицательной форме двулучепреломления и положительному двулучепреломлению на кристалле. Е. Отрицательный сферический крест. Ж. Положительный сферический крест с соответствующей эллипсоидальностью. 3. Зерно картофельного крахмала между скрещенными поляризаторами и при использовании чувствительной пластинки (ST — медленная ось пластинки). Видно, что дополнительное синее окрашивание (с) располагается параллельно ST, тогда как вычитаемое желтое окрашивание (ж) располагается под прямым углом к ней. Заметьте также, что изогиры не параллельны ни анализатору (линия АА), ни поляризатору (линия РР). Рисунки А и Б воспроизводятся из работы [6] с разрешения
Harvard University Press, а рисунки В—Ж — из работы [7] с разрешения Unwin Hyman.
Таблица 2.11. Исследование препарата между скрещенными поляризаторами для выявления контраста между двулучепреломляющими и изотропными областями
1.Установите в микроскопе освещение по Кёлеру.
2.Установите поляризатор в известном положении.
3.Положите несколько зерен картофельного крахмала в воду, накройте покровным стеклом и рассмотрите. За исключением контуров зерен вы вряд ли что-нибудь увидите. Некоторое повышение контраста может быть достигнуто путем опускания конденсора, при этом могут быть видны ядро и пористая структура. Вы можете убедиться в неадекватности использования освещения узким пучком света.
4.Установите анализатор, и вы увидите, что освещение фона сразу же упадет практически до нуля. Зерна крахмала, однако, будут сравнительно яркими, и в каждом из них будет видно нечто
28
