
- •Альдегиды и кетоны
- •Методы получения
- •Реакционная способность
- •I. Реакции присоединения по карбонильной группе
- •II. Реакции присоединения-отщепления (реакции с азотистыми нуклеофилами).
- •III. Реакции с участием атомов водорода при -углеродном атоме
- •2. Реакции альдольной и кротоновой конденсации
- •IV. Реакции окисления
- •Карбоновые кислоты
- •Методы получения
- •Реакционная способность
- •I. Он-кислотность карбоновых кислот
- •II. Реакции замещения он-группы
- •Сложные эфиры
- •Соли карбоновых кислот
- •Амиды карбоновых кислот
- •1. Гидролиз
- •2. Кислотно-основные свойства
- •Нитрилы карбоновых кислот
- •Жиры, масла
- •Общая формула жиров (масел)
- •Физические свойства
- •Реакционная способность
- •Дикарбоновые кислоты
- •Угольная кислота и ее производные
- •Синтез некоторых производных угольной кислоты и их свойства
- •1. Основные свойства мочевины
- •2. Реакции мочевины по амидному фрагменту
- •3. Поведение при нагревании
Сложные эфиры
Сложные эфиры вступают в реакции нуклеофильного замещения алкокси-группы в условиях кислого или щелочного катализа. Ниже изображено распределение электронной плотности в молекулах сложных эфиров.

1. Реакции нуклеофильного замещения алкоксигруппы
а) Гидролиз
Для гидролиза сложных эфиров и всех остальных производных кислот необходим кислый или щелочной катализ. При кислом гидролизе получают карбоновые кислоты и спирты (реакция обратная этерификации), при щелочном гидролизе образуются соли карбоновых кислот и спирты.
Кислый гидролиз сложных эфиров:

Механизм SN, нуклеофил - H2O, происходит замещение алкоксигруппы на гидроксил.
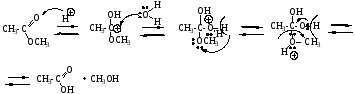
Щелочной гидролиз сложных эфиров: реакция идет в два этапа с 2-мя молями основания, образовавшаяся кислота превращается в соль.

Механизм SN, Nu = OH

б) Переэтерификация - превращение одного сложного эфира в другой сложный эфир (молекулярный вес спирта, который используют в качестве реагента должен быть выше для сдвига равновесия реакции вправо).

Механизм SN, нуклеофил - н-C3H7OH, аналогичен кислому гидролизу сложных эфиров.
в) Аммонолиз – взаимодействие с NH2X (X=H, NH2), синтез амидов и гидразидов кислот.

Механизм SN, нуклеофил = NH2-NH2 (NH2-X), идет замещение алкокси-группы на азотсодержащую группу.

Соли карбоновых кислот
Соли карбоновых кислот применяют в синтезе сложных эфиров, если карбоновые кислоты и спирты мало доступны. Из солей получают алканы (реакция Дюма) и кетоны.
1. Синтез сложных эфиров

Эта реакция используется, если кислоты и спирты труднодоступны.
2. Реакция Дюма (см. тему “Алканы”, синтез алканов)
3. Синтез кетонов пиролизом солей Ca+2 , Mg+2, Mn+2 карбоновых кислот (см. тему “Альдегиды, кетоны”).
Амиды карбоновых кислот
Амиды менее реакционноспособны в реакциях нуклеофильного замещения, чем сложные эфиры, что является следствием более сильного p, -сопряжения НПЭ атома азота аминогруппы и -связи карбонила. Следствием этого сопряжения является отсутствие основных свойств у амидов и более выраженная NH-кислотность по сравнению с аминами.
Амиды муравьиной кислоты получают из оксида углерода и аммиака (аминов).

Синтез амидов остальных кислот описан в теме «Карбоновые кислоты».
1. Гидролиз
При кислом гидролизе амидов получают карбоновые кислоты и аммиак или амины в случае N-алкил и N,N-диалкиламидов, при щелочном гидролизе образуются соли карбоновых кислот.
а) кислый гидролиз, SN-замещение амино-группы на гидроксил.

б) щелочной гидролиз

2. Кислотно-основные свойства
а) NH-Кислотность амидов

б) Основность амидов
Основные свойства у амидов в отличие от аминов практически отсутствуют, так как НПЭ атома азота находится в сопряжении с -связью карбонила.

3. Реакция с азотистой кислотой – образование карбоновых кислот, реакция аналогична взаимодействию первичных аминов с азотистой кислотой и является качественной.

5. Восстановление амидов - синтез аминов

6. Дегидратация амидов – синтез нитрилов карбоновых кислот (см. тему “Карбоновые кислоты”)
