
Фармацевтический анализ. Химические
.pdf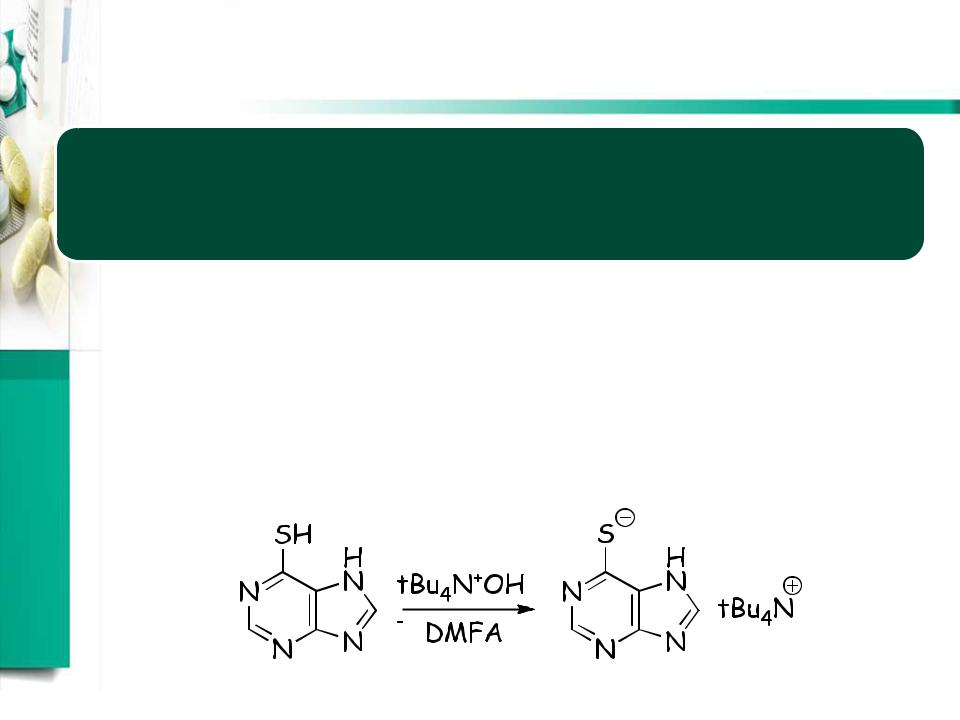
Кислотно-основное титрование
Алкалиметрическое титрование в неводной среде – определение меркаптопурина
•титрант: 0,1 М раствор тетрабутиламмония гидроксида (в толуоле!)
•среда: ДМФА
•потенциометрическое установление точки эквивалентности
pKa = 7.77

Кислотно-основное титрование
Метод Кьельдаля
•способ определения азота в органических соединениях
•при определении азота в нитро-, нитрозо-, азо-, гидразо- и диазосоединениях пробу предварительно
восстанавливают, используя HI, Zn, Na2S2O3, соединения Sn(II) и др.

1
2
3
4
Метод Кьельдаля
•Кипячение с серной кислотой (в присут. HgSO4
или CuSO4 и SeO2, K2SO4 или Na2SO4
•Подщелачивание раствора и отгонка аммиака
•Поглощение аммиака раствором хлороводородной кислоты
•Титрование избытка кислоты щелочью
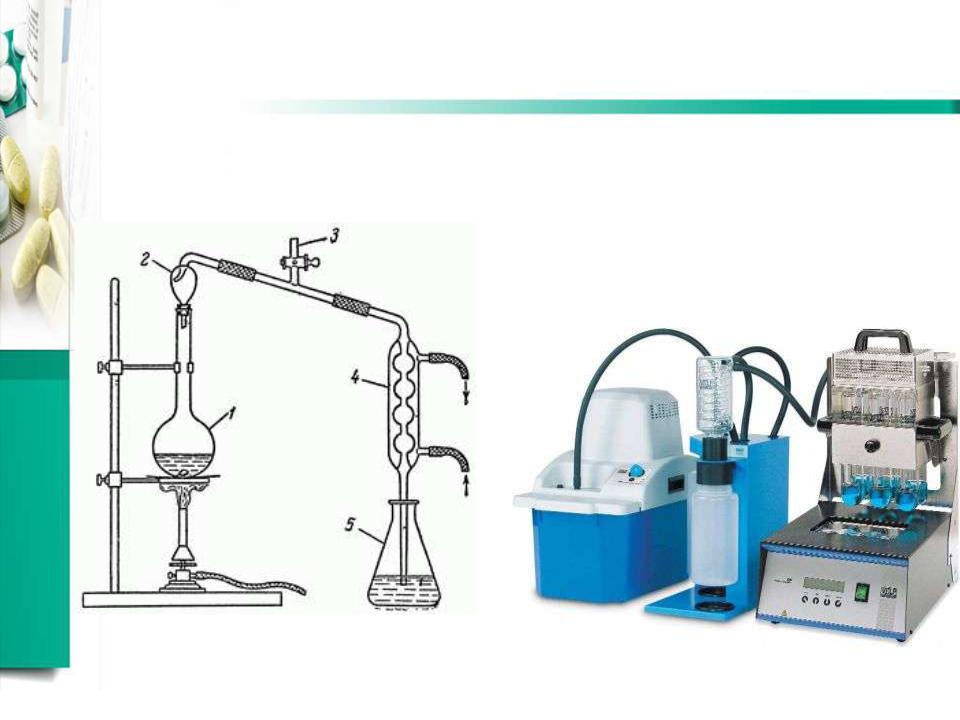
Метод Кьельдаля
Окислительно-восстановительное титрование

Окислительно-восстановительное
титрование
Виды:
•йодометрия
•хлориодометрия
•йодатометрия
•нитритометрия
•перманганатометрия
•дихроматометрия
•цериметрия
Окислительно-восстановительное
титрование
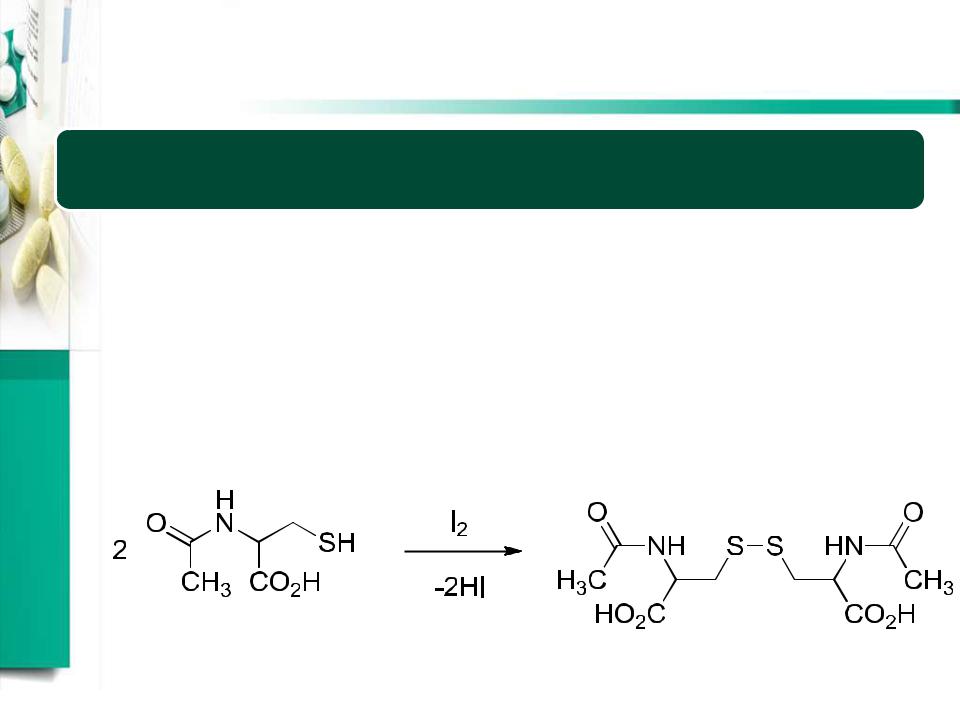
Йодиметрия
•Титрант: KI3 (KI+I2), pH=5-8
•Определяемое вещество – сильный восстановитель
•Т.э.: появление окраски I2, крахмал усиливает окраску
•Пример: определение ацетилцистеина

Окислительно-восстановительное
титрование
Йодометрия
•Предварительное восстановление с помощью KI
•Титрант: Na2S2O3 - оттитровываем образовавшийся I2
•Определяемое вещество – окислитель
•Т.э.: исчезновение окраски I2
•добавлять крахмал в конце титрования!
•титровать быстро!
2FeCl3+2KI = 2FeCl2 + I2 + 2KCl
I2 + 2Na2S2O3 = 2NaI + Na2S4O6
Окислительно-восстановительное
титрование
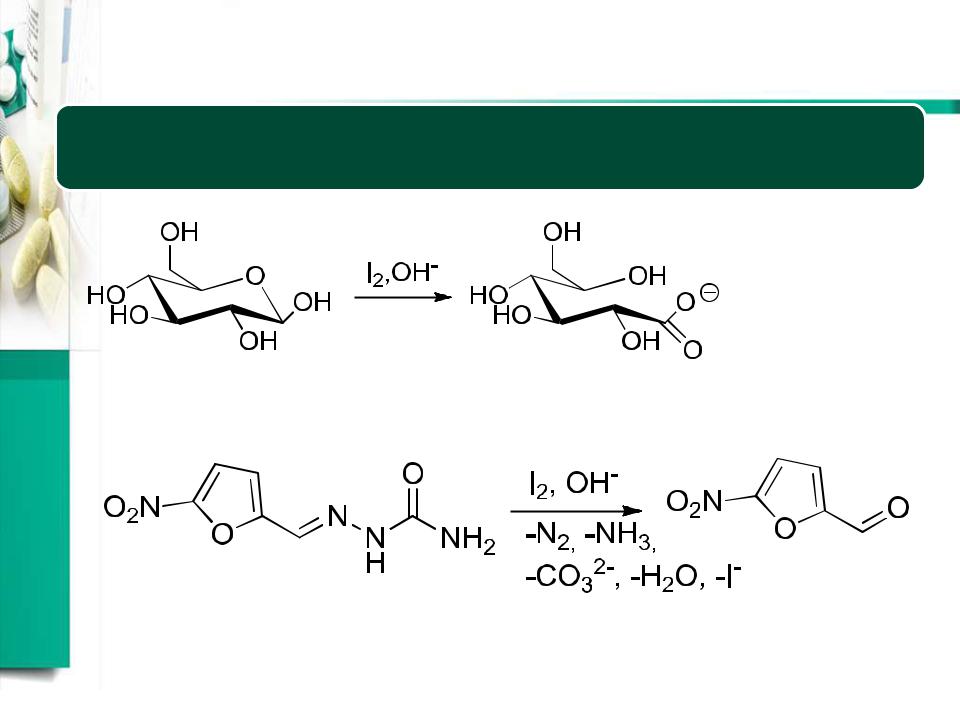
Йодометрия. Примеры
глюкоза
фурацилин
Окислительно-восстановительное
титрование
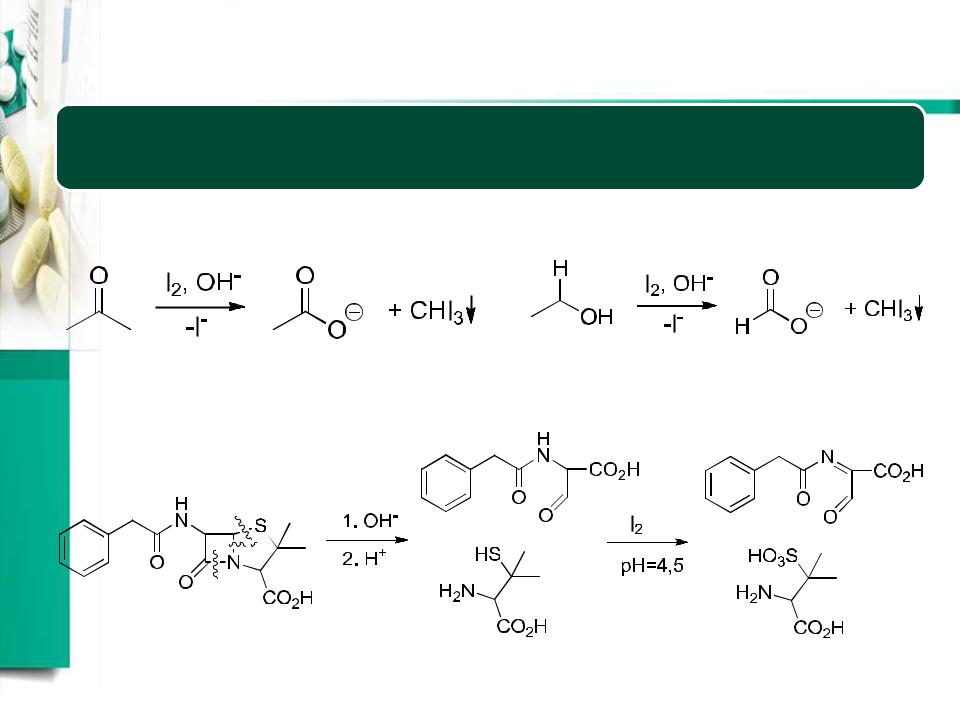
Йодометрия. Примеры
бензилпенициллин
