
МУ по лаб.р. 2013
.pdfПриложение 6
Интервалы перехода окраски некоторых кислотно-основных индикаторов
Индикатор |
Интервал |
Окраска |
|
|
|
перехода |
до интервала |
|
после |
|
индикатора |
перехода |
|
интервала |
|
в значениях pH |
|
|
перехода |
Метиловый |
3,1–4,4 |
красная |
|
желтая |
оранжевый |
|
|
|
|
Метиловый |
4,4–6,2 |
красная |
|
желтая |
красный |
|
|
|
|
Лакмус |
5,0–8.0 |
красная |
|
синяя |
Фенофталеин |
9,4–10,6 |
бесцветная |
|
розовая |
81

Приложение 7
Образец выполнения расчетной работы
Определение термодинамических функций химической реакции
1.Записать уравнение химической реакции и условия задания
всоответствии с номером варианта (табл. 3.3).
аА + вВ ↔ сС + dD
Температура:_______
Масса (или объем):_______
2. Выписать значения Н0обр и S0. для исходных реагентов и продуктов реакции (прил. 2):
Вещество |
Н0обр, кДж/моль |
S0, Дж/моль·K |
A
B
C
D
3. Применив следствие закона Гесса, рассчитать стандартное и з- менение энтальпии реакции
Hхр0 (с HC0 d HD0 ) (a HA0 b HB0 ).
4. Вычислить изменение энтропии реакции в стандартных условиях:
S0 |
(с S0 |
d S0 ) (a S0 |
b S0 ). |
||
хр |
C |
|
D |
A |
B |
5. Пользуясь соотношением |
GT |
Hхр |
T Sхр , вычислить из- |
||
менение потенциала Гиббса при стандартной температуре 298 К.
6. Вычислить ΔGТ при заданной температуре, полагая, что Н0 и S0 не зависят от температуры
GT Hхр T Sхр .
82

7. Используя полученные значения G0 |
и ΔG , рассчитать кон- |
298 |
Т |
станту химического равновесия (Kр) при 298 К и заданной температуре из уравнения
GT 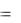 2,303
2,303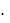 R T lgКp
R T lgКp
8. Определить температуру, при которой наступает состояние
химического равновесия при ΔGТ = 0. |
|
||
При химическом равновесии ΔG = 0, следовательно, | H 0 |
| = |T S 0 |. |
||
|
|
Т |
|
Таким образом, Тр |
Н |
. |
|
|
|
||
|
S |
|
|
9.Рассчитать количество теплоты, поглощенной или выделенной
входе реакции на заданный объем (массу или количество) вещества:
H |
Q ν |
, |
|
n |
|||
|
|
где Q – тепловой эффект реакции; n – стехиометрический коэффи-
циент (заданного вещества); ν – количество вещества, v |
m |
. Здесь m – |
|||
M |
|||||
|
|
|
|
||
заданная масса вещества, М – молярная масса вещества, или v |
V |
, |
|||
|
|||||
|
|
|
Vm |
||
где V – заданный объем газообразного вещества; Vm – молярный объем газа (22,4 моль/л).
10. Сделать вывод, является ли рассматриваемая реакция самопроизвольной в прямом направлении. Проанализируйте влияние величины ∆Нреак, ∆Sреак и изменения температуры на величину ΔGТ.
83
Приложение 8
Стандартные электродные потенциалы некоторых окислительно-восстановительных систем
Окисленная |
Восстанов- |
|
Уравнение реакции |
Е0, В |
|||
форма |
ленная |
|
|
|
|
|
|
|
форма |
|
|
|
|
|
|
SO32– |
S(тв) |
SO32– + 4e– + 3H2O |
S + 6OH– |
–0,90 |
|||
SO42– |
SO32– |
SO42– +2e– +H2O |
SO32– +2OH– |
–0,90 |
|||
NO3– |
NO2(г) |
NO3– + e– + H2O |
NO2 + 2OH– |
–0,85 |
|||
2H2O |
H2 + 2OH– |
2H2O + 2e– |
H2 +2OH– |
–0,83 |
|||
Fe(OH)3 |
Fe(OH)2 |
Fe(OH)3 + e– |
Fe(OH)2 + OH– |
0,56 |
|||
S |
S2– |
S + 2e– |
S2– |
|
|
|
–0,48 |
NO2– |
NH3 |
NO2– + 6e– + 6H2O |
NH4OH + 7OH– |
–0,16 |
|||
NO3– |
NO |
NO3– + 3e– + 2H2O |
NO + 4OH– |
–0,14 |
|||
CrO42– |
Cr(OH)3 |
CrO42– +2e– + 4H2O |
Cr(OH)2 + 5OH– |
–0,12 |
|||
2H+ |
H2 |
2H+ + 2e– |
H2 |
|
|
0,00 |
|
NO3– |
NO2– |
NO3– + 2e– + H2O |
NO2– + 2OH– |
+0,01 |
|||
S(т) |
H2S |
S + 2e– + 2H+ |
H2 S |
|
+0,14 |
||
Sn4+ |
Sn2+ |
Sn4+ + 2e– |
Sn2+ |
|
|
+0,15 |
|
Co(OH)3 |
Co(OH)2 |
Co(OH)3 + e– |
Co(OH)2 + OH– |
+0,20 |
|||
SO42– |
SO32– |
SO42– + 2e– + 4H+ |
H2SO32– + H2O |
+0,20 |
|||
Ni(OH)3 |
Ni(OH)2 |
Ni(OH)3 +e– |
Ni(OH)2 + 2OH– |
+0,51 |
|||
ClO4– |
Cl– |
ClO4– + 8e– + 4H2O |
Cl– + 8OH– |
+0,51 |
|||
I2 |
2I– |
I2 + 2e– |
2I– |
|
|
|
+0,53 |
MnO – |
MnO 2– |
MnO – + e– |
MnO 2– |
|
+0,54 |
||
4 |
4 |
4 |
|
|
4 |
|
|
MnO4– |
MnO2(тв) |
MnO4– + 3e– + 2H2O |
MnO2 + 4OH– |
+0,57 |
|||
MnO42– |
MnO2(тв) |
MnO42–+ 2e– + 2H2O |
MnO2 + 4OH– |
+0,58 |
|||
PbO2 |
Pb(тв) |
PbO2 + 4e– + 4H+ |
Pb +2H2 O |
+0,68 |
|||
O2 |
H2O2 |
O2 + 2e– + 2H– |
H2O2 |
|
+0,68 |
||
Fe3+ |
Fe2+ |
Fe3+ + e– |
Fe2+ |
|
|
+0,77 |
|
NO – |
NO (г) |
NO – + e– |
+ H + NO2 + H O |
+0,81 |
|||
3 |
2 |
3 |
|
|
|
2 |
|
Br2((ж) |
2Br– |
Br2 + 2e– |
2Br– |
|
|
+1,07 |
|
O2 + 4H+ |
2H2O |
O2 + 4H+ + 4e– |
2H2O |
|
+1,23 |
||
MnO2(тв) |
Mn2+ |
MnO2 + 2e– + 4H+ |
Mn2+ + 2H2 O |
+1,28 |
|||
ClO4– |
Cl– |
ClO4– +2e– + 8H+ |
Cl– + 4H2O |
+1,34 |
|||
Cl2(г) |
2Cl– |
Cl2 + 2e– |
2Cl– |
|
|
+1,36 |
|
Cr2O72– |
2Cr3+ |
Cr2O72– + 6e– + 14H+ |
2Cr3+ + 7H2O |
+1,36 |
|||
ClO3– |
Cl– |
ClO3– + 6e– + 6H+ |
Cl– + H2O |
+1,45 |
|||
PbO2(тв) |
Pb2+ |
PbO2 + 2e– + 4H+ |
|
Pb2+ + 2H2O |
+1,46 |
||
HClO |
Cl– |
HClO +2e– + H+ |
Cl– + H2O |
1,50 |
|||
84
|
|
|
|
|
|
Окончание прил. 8 |
|
|
|
|
|
|
|||
Окисленная |
Восстанов- |
|
Уравнение реакции |
Е0, В |
|||
|
форма |
ленная |
|
|
|
|
|
|
|
форма |
|
|
|
|
|
MnO4– |
Mn2+ |
MnO4– + 5e– + 8H+ |
MnO + 4H2O |
+1,52 |
|||
MnO4– |
MnO2(тв) |
MnO4– + 3e– + 4H+ |
MnO2 + 2H2O |
+1,67 |
|||
H2O2 |
H2O |
H2O2 + 2e– + 2H+ |
2H2O |
+1,77 |
|||
S O 2– |
SO 2– |
S O 2– + 2e– |
2SO 2– |
+2,05 |
|||
2 |
8 |
4 |
2 |
8 |
|
4 |
|
O3(г) |
O2(г) |
O3 +2e– + 2H– |
O2 + H2O |
+2,85 |
|||
F2(г) |
2F– |
F2 + 2e– 2F– |
|
|
+2,85 |
||
Условные обозначения: г – газ; ж – жидкость; тв – твердое вещество.
85
Приложение 9
Ряд стандартных электродных потенциалов металлов
Электродный |
Е0, В |
Электродный |
Е0, В |
Электродный |
Е0, В |
|
процесс |
|
процесс |
|
процесс |
|
|
|
|
|
|
|
|
|
Li = Li– + e– |
–3,045 |
Mn = Mn2+ + 2е– |
–1,179 |
H2 = 2H+ + 2e– |
0,000 |
|
K = K+ + e– |
–2,924 |
V = V2 + + 2e– |
–1,175 |
Ge = Ge2+ + 2e– |
+0,050 |
|
Cs = Cs+ + e– |
–2,923 |
Zn = Zn2+ + 2e– |
–0,763 |
Sb = Sb3+ + 3e– |
+0,150 |
|
Ba = Ba2+ + 2e– |
–2,905 |
Cr = Cr3+ |
+ 3e– |
–0,744 |
Bi = Bi3+ + 3e– |
+0,215 |
Sr = Sr2+ + 2e– |
–2,888 |
Fe = Fe2+ |
+ 2e– |
–0,440 |
Cu = Cu2+ + 2e– |
+0,337 |
Ca = Ca2+ +2e– |
–2,866 |
Cd = Cd2+ +2e– |
–0,403 |
Ru = Ru2+ + 2e– |
+0,450 |
|
Na = Na+ +e– |
–2,714 |
Co = Co2+ + 2e– |
–0,277 |
Ag = Ag+ + e– |
+0,799 |
|
Mg = Mg2+ + 2e– |
–,363 |
Ni = Ni2+ |
+2e– |
–0,250 |
Hg = Hg2+ + 2e– |
+0,850 |
Sc = Sc3+ + 3e– |
–,077 |
Mo = Mo3+ + 3e– |
–0,200 |
Os = Os2+ + 2e– |
+0,850 |
|
Be = Be2++ 2e– |
–,847 |
Sn = Sn2+ + 2e– |
–0,136 |
Pd = Pd2+ + 2e– |
+0,987 |
|
Al = Al3+ + 3e– |
–,663 |
Pb = Pb2+ + 2e– |
–0,126 |
Pt = Pt2+ + 2e– |
+1,188 |
|
Ti = Ti2+ + 2e– |
–,603 |
W = W3+ + 3e– |
–0.050 |
Au = Au3+ + 3e– |
+1,498 |
|
86
Учебно-практическое издание
Миронова Валентина Александровна Жереб Людмила Александровна Чижевская Марина Валерьевна
ХИМИЯ
Учебное пособие (практикум)
Редактор Т. А. Ермолаева
Оригинал-макет и верстка А. А. Ловчиковой
Подписано в печать 06.06.2013. Формат 60×84/16. Бумага офсетная. Печать плоская. Ул. печ. л. 5,1. Уч.-изд. л. 5,6.
Тираж 100 экз. Заказ |
С 87/13. |
Санитарно-эпидемиологическое заключение № 24.49.04.953.П.000032.01.03 от 29.01.2003 г.
Редакционно-издательский отдел Сиб. гос. аэрокосмич. ун-та. Отпечатано в отделе копировально-множительной техники Сиб. гос. аэрокосмич. ун-та.
660014, г. Красноярск, просп. и. газ. «Красноярский рабочий», 31.
87

Приложение 10
88
