
МУ по лаб.р. 2013
.pdf
примера электрохимической коррозии рассмотрим действие серной кислоты H2SO4 на технический цинк, содержащий примеси железа.
На поверхности такого цинка возникает множество микроскопических гальванических элементов Zn || H2SO4 || Fe.
При контакте двух металлов анодом всегда является тот, у которого меньше величина потенциала, т. е. цинк служит анодом, а железо – катодом. На цинке протекает анодный процесс:
Zn0 Zn+2 +2e– (окисление, коррозия цинка).
Катодный процесс протекает на железе и связан с выделением водорода (водородная деполяризация происходит в кислой среде,
если pH 7): |
|
2H+ +2e– |
2H0 H2 (восстановление, водородная деполяриза- |
ция). |
|
Обычно при электрохимической коррозии катодные процессы зависят от рН среды: если рН < 7 (кислая среда), то на катоде происходит водородная деполяризация (см. выше); при рН > 7 (нейтральная или основная среда) происходит ионизация (восстановление) кислорода или кислородная деполяризация. За катодный процесс отвечает вода и растворенный в ней кислород: они присоединяют электроны,
образуя гидроксогруппу: |
|
|
pH 7: 2Н О + О + 4e– |
4ОН– (катодный процесс). |
|
2 |
2 |
|
При описании коррозионных явлений окисляющийся металл называют анодом, а процесс окисления – анодным. Металл, на котором электроны переходят к окислителю, называют катодом, а процесс восстановления – катодным (по аналогии с гальваническими элементами).
В случае контакта разнородных металлов в результате различия стандартных электродных потенциалов этих металлов возникает разность потенциалов. При этом более активный электрохимический металл разрушается и становится анодом, а менее активный металл – катодом.
Однако даже на безукоризненно однородной поверхности металла, согласно уравнению Нернста:
Е Е |
0 |
RT |
ln |
C1 |
|
nF |
C2 |
могут образоваться анодные и катодные участки, если на различных частях поверхности разная концентрация электролита. Примером может служить электрохимическая коррозия вследствие неравномерной
61
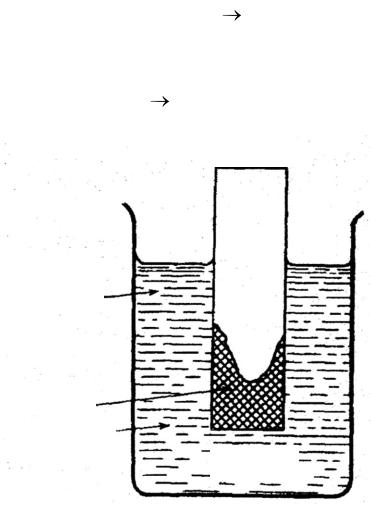
аэрации (насыщения воздухом). Замечено, что пластина металла, опущенная в воду, ржавеет вследствие неодинаковой доставки кислорода к различным участкам поверхности металла (рис. 7.1). Участки металла, соприкасающиеся с раствором, содержащим больше кислорода, становятся катодными: в них металл не растворяется, а на металле происходит катодная реакция:
2Н О + О + 4e– |
4ОН– |
|
2 |
2 |
|
Участки с меньшей концентрацией кислорода являются анодами, и там начинается коррозия:
Fe0 Fe2+ + 2e–
Воздух
Железо
Много
кислорода
Ржавчина |
|
Мало |
|
кислорода |
Раствор |
|
Рис. 7.1. Коррозия железа вследствие неравномерной аэрации
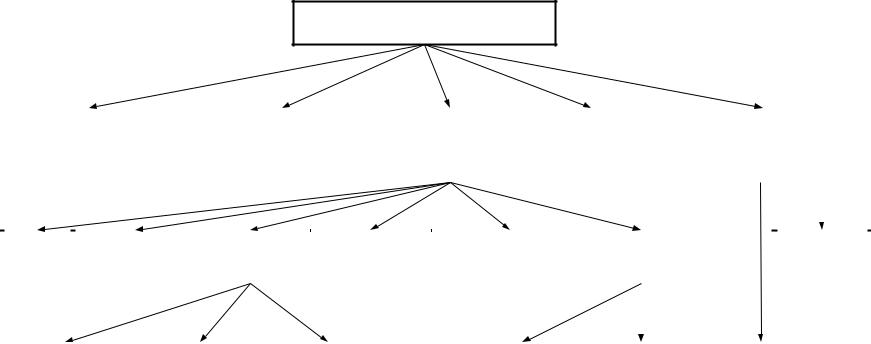
Способы защиты металлов от коррозии. Цель защитных мер – максимально затормозить скорость коррозионного процесса. Этого обычно достигают воздействием либо на металл, либо на среду, либо на поверхность раздела металл-среда (рис. 7.2).
Радикальным методом защиты от коррозии путем воздействия на металл является замена самого металла на его оксид или полимер либо создание коррозионно-стойких сплавов. К средствам воздействия на металл относится электрохимическая защита, когда защищаемый
62
Способы защитыы от коррозии от коррозии
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Изменение свойств |
|
|
|
Применение |
|
|
|
Защитные |
|
|
|
Замена |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Электрохимическая |
|
|||||
|
Изменение свойств |
|
|
|
Применение коррозионно- |
|
|
|
Защитные |
|
|
|
металлов |
|
|
|
|
||
|
коррозионной среды |
|
|
|
коррозионно-стойких |
|
|
|
ппокрытия |
|
|
|
|
|
|
Электрохимическая защита |
|
||
|
коррозионной среды |
|
|
|
стойких сплавов |
|
|
|
|
|
|
полимерами |
|
|
|
защита |
|
||
|
|
|
|
|
сплавов |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Смазки,, |
|
|
Эмалирование |
|
Химические |
|
|
Адсорбционные |
|
|
Полимерные |
|
|
|
Металличес- |
|
|
Протектор- |
|
лаки,, |
|
|
Эмалирование |
|
ззащитные |
|
|
Адсорбционные |
|
|
Полимерные |
|
|
|
Металлические |
|
|
Протекторная |
|
|
|
|
|
|
защитные |
|
|
покрытия |
|
|
|
кие покрытия |
|
|
ная защита |
||||
краски |
|
|
|
|
пленки |
|
|
защитные пленки |
|
|
|
|
|
покрытия |
|
|
защита |
||
|
|
|
|
|
|
пленки |
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Оксидирование |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Катодная |
|
|
|
|
|
Фосфатиро- |
|
|
|
Пассивиро- |
|
|
|
Катодные |
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
Оксидирование |
|
|
|
Фосфатирование |
|
|
|
Пассивирование |
|
|
|
|
|
|
Анодные |
|
|
Катодная и |
|
|
|
|
|
|
|
|
|
|
|
Катодные |
|
|
|
|
|
ианодная |
||||
|
|
|
|
|
вание |
|
|
|
вание |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Рис. 7.2. Схема способов защиты металлов от коррозии
63
металл подвергается катодной поляризации от внешнего источника (катодная защита) или созданием электрического контакта с более активным металлом (протекторная защита).
Воздействовать на среду можно путем удаления агрессивных агентов (окислителей). Если этого сделать нельзя, то для замедления процесса в жидкой и газовой среде следует применять специальные вещества – ингибиторы коррозии. Наиболее широко используются для защиты от коррозии средства воздействия на поверхность раздела металл – окружающая среда. Как правило, это защитные покрытия. Нанесение защитных покрытий механически изолирует поверхность металла от окружающей среды, а также изменяет ее электрохимические свойства.
Пассивирование металлов осуществляется путем образования на их поверхности пассивирующих пленок из оксидов или труднорастворимых солей.
При оксидировании происходит уплотнение защитной оксидной пленки. Оксидирование осуществляется химическим и электрохимическим способами.
Металлические покрытия из металлов, устойчивых к коррозии (Zn, Sn, Ni, Ag, Cr), наносят путем электролиза (гальваностегии).
По характеру защитного действия различают анодные и катодные металлические покрытия. Анодными называются такие покрытия, в которых покрывающий металл имеет более отрицательный потенциал. Например, анодным является цинковое покрытие на железо. При нарушении целостности покрытия возникают гальванопары, в которых роль анода будет выполнять цинк. Катодными являются такие покрытия, в которых покрывающий металл имеет более положительный электродный потенциал, например, железо покрыто оло-
вом (Sn на Fe).
Методика и порядок проведения работы
Опыт 1. Коррозия, возникающая при контакте двух различных металлов
Впробирку внесите 8–10 капель 1н раствора серной кислоты
ипоместите туда гранулу цинка. Наблюдайте медленное выделение водорода. Введите в раствор медную проволоку, не доводя ее до соприкосновения с цинком. Наблюдается ли выделение водорода на меди? Погрузите медную проволоку глубже, чтобы она контактировала
64
с цинком. Объясните выделение водорода на меди в этом случае. Составьте схему действия образовавшейся гальванопары. Как повлиял на коррозию цинка контакт с медью?
Опыт 2. Коррозия в результате различного доступа кислорода (аэрационная коррозия)
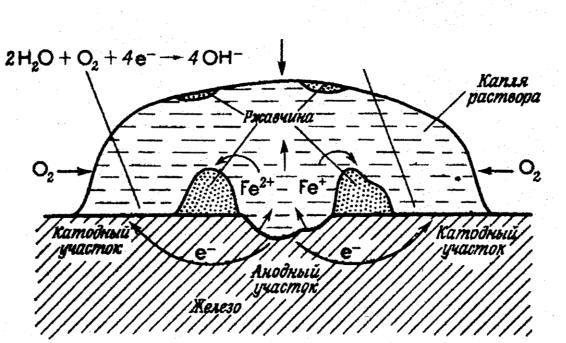
Очистите стальную пластинку наждачной бумагой, промойте и вытрите фильтровальной бумагой. На чистую поверхность нанесите каплю специального реактива, состоящего из 3%-го раствора хлорида натрия, к которому добавлен фенолфталеин и гексацианоферрат (III) калия K3[Fe(CN)6] (рис. 7.3). Наблюдайте появление синего окрашивания в центре капли и розового по ее окружности.
Составьте схему действия гальванопары, возникающей при различной аэрации металлической поверхности. Чем вызвано появление розовой окраски у краев капли?
Примечание. Гексацианоферрат (III) калия K3 [Fe(CN)6] добавлен как реактив на ионы Fe+2.
Опыт 3. Активирующее действие ионов хлора
Поместите в 2 пробирки по кусочку алюминиевой проволоки и прилейте к ним раствор сернокислой меди, слегка подкисленный серной кислотой.
В одну из пробирок добавьте 4, 5 капель 10%-го раствора хлорида натрия. В каком случае скорее протекает реакция? Объясните результат опыта и составьте схему действия образовавшихся гальванопар.
Опыт 4. Электрохимическая коррозия оцинкованного и луженого железа
Налейте в 2 пробирки на 0,5 ее объема специальный раствор, состоящий из гексацианоферрата (III) калия и 2н раствора серной кислоты. Две железные проволочки очистите наждачной бумагой. Концом одной проволочки плотно обмотайте кусочек цинка, другой – кусочек олова. Опустите каждую проволочку в одну из пробирок с приготовленным раствором.
65
О2
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2Н2О + О2 + 4е– → 4ОН– |
||||||
|
2Н2О + О2 + 4е– → 4ОН– |
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Капля |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
раствора |
|||
|
|
|
|
|
|
|
|
Ржавчина |
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
О2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
О2 |
|
||
|
|
|
|
|
|
|
|
|
Fe2+ |
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
Fe2+ |
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Катодный |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Катодный |
|
||||
|
|
|
участок |
|
|
е– |
|
|
|
|
|
|
|
|
|
|
е– |
|
участок |
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Анодный |
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
участок |
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
Железо |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Рис. 7.3. Коррозия железа под каплей раствора хлорида натрия
Через несколько минут наблюдайте появление окрашенного в синий цвет раствора, в который погружена проволочка с оловом. Объясните образование ионов Fe+2 в этом растворе, учитывая, что железо и олово образуют гальваническую пару. На поверхности какого металла выделяется в этом случае водород? Почему раствор не окрасился в синий цвет, когда была опущена проволочка с цинком? Приведите схему перехода электронов в гальванической паре железо-цинк. Ионы какого металла переходят в раствор в данном случае? Почему?
Составьте схему электрохимической коррозии луженого и оцинкованного железа, сопровождающейся образованием микрогальванопар. В каком случае при местном разрушении защитного покрытия (цинка или олова) будет проходить коррозия железа под остающимся неизменным защитным покрытием? В каком случае будет разрушаться защитное покрытие при относительной неизменности железного изделия?
Опыт 5. Оксидирование стали
Очистите наждаком две стальные пластинки. Одну из них нагрейте в пламени спиртовки до появления окисных пленок, которые из-за своей различной толщины вызывают различную интерференцию света и поэтому окрашены в разные цвета. Нанесите по капле раствора сульфата меди на оксидированный и неоксидированный образцы. По скорости появления темного пятна на образцах оцените защитные свойства нанесенной пленки.
66
Опыт 6. Электрохимическая защита
В пробирку внесите 5–10 капель 1н уксусной кислотой и прибавьте несколько капель раствора йодида калия KI, поместите цинк и свинец в контакте друг с другом. Другой образец свинца для сравнения поместите в другую пробирку с тем же раствором. Где скорее появится желтое окрашивание (йодид свинца имеет желто-золотистый цвет)? Составьте схему действия гальванопары. Объясните результаты опыта.
Опыт 7. Применение ингибиторов
В3 пробирки внесите по 7 капель 0,2н раствора серной кислоты
ипо 1 капле раствора гексацианоферрата (III) калия (индикатор на ионы Fe2+ – синее окрашивание). В первую пробирку добавьте микрошпатель уротропина. Опустите в первую и вторую пробирки железные проволоки, предварительно протравленные соляной кислотой,
а в третью – проволоку, покрытую ржавчиной. Отметьте время появления и интенсивность синей окраски в каждой пробирке. Почему они различны? Какова роль уротропина и ржавчины?
Контрольные вопросы
1.Дайте определение понятия «коррозия металлов».
2.Перечислите виды коррозии.
3.Как в случае нарушения целостности покрытия будет проте-
кать в кислой среде коррозия железа: а) покрытого медью; б) покрытого марганцем?
4.Коррозия железа будет протекать быстрее в случае а) луженого железа; б) оцинкованного железа. Приведите схему работы микрогальванопар.
5.Какие методы защиты металлов от коррозии существуют?
6.Какие покрытия называются катодными, а какие – анодными?
7.Напишите уравнения химических процессов, протекающих на электродах при электролитическом никелировании.
8.Какой процесс называется оксидированием? Приведите пример.
Библиографический список
1.Коровин, Н. В. Общая химия / Н. В. Коровин. – М. : Высш. шк.,
2000. – С. 310–340.
2.Фролов, В. В. Химия / В. В. Фролов. – М. : Высш. шк., 1979. –
С. 522–548.
67
Лабораторная работа 8
МЕТАЛЛЫ
Цель работы: ознакомиться с общими свойствами металлов.
Теоретические сведения
Свойствами металлов обладает большинство элементов, входящих в периодическую систему Д. И. Менделеева (прил. 9). Элементы с металлическими свойствами могут относиться к типу s-, p-, d- или f-элементов.
Все металлы обладают общими так называемыми металлическими свойствами, но каждый элемент проявляет их в соответствии с его положением в периодической системе Д. И. Менделеева, т. е. в соответствии с особенностями строения его атома. В зависимости от того, какой подуровень у атома металла заполняется электронами, проявляются общие химические свойства. Особенностью металлов является их способность к образованию металлической связи, которая определяет их физические свойства.
Металлы служат основным конструкционным материалом в машиностроении и приборостроении. Это объясняется тем, что они подвергаются механической обработке благодаря таким их свойствам, как прочность, пластичность, ковкость, тягучесть, обладают хорошей тепло- и электропроводностью. Металлам присущи также металлический блеск, обусловленный их способностью хорошо отражать свет, и непрозрачность. В высокодисперсном состоянии металлы обычно имеют черный цвет и не блестят. Атомы элементов, обладающих металлическими свойствами, содержат мало электронов на внешних электронных уровнях (1–3), и из-за сравнительно больших размеров атома они значительно удалены от ядра. Поэтому в химическом отношении все металлы характеризуются сравнительной легкостью отдачи валентных электронов:
Me0 Men+ +ne–
и, как следствие, способностью образовывать положительно заряженные ионы. В связи с этим металлы в свободном состоянии способны проявлять только восстановительные свойства, хотя и в различной степени.
Металлы проявляют в своих соединениях только положительную степень окисления, а низшая степень окисления, которой они обла - дают только в свободном состоянии, равна нулю.
68
Если металлу присущи несколько степеней окисления, то соединения, в которых он проявляет низшую из них, также обычно являются восстановителями, например соединения меди (I), олова (II), железа (II). Окислителями могут быть те соединения, металлов, в которых степень окисления металла велика: равна номеру группы, в которой находится металл, или близка к нему. На практике в качестве окислителей применяют аммиачный раствор оксида серебра, хлорид железа (III), диоксид свинца, диоксид марганца, хромат и дихромат калия, перманганат калия и др.
Восстановительная способность свободных металлов проявляется при взаимодействии их с элементарными окислителями, обладающими окислительными свойствами.
Большинство металлов легко взаимодействуют с галогенами с образованием высших галогенидов металлов. Металлы взаимодействуют с кислородом менее энергично. С образованием нормальных оксидов. С азотом многие металлы вообще не взаимодействуют, что объясняется очень большой энергией диссоциации окислителя.
Взаимодействие металлов с кислотами, щелочами и водой различно и зависит от активности металлов и их специфических свойств, определяемых положением в Периодической системе элементов Д. И. Менделеева.
Химически активные металлы вступают во взаимодействие с водой при комнатной температуре, выделяя водород:
Me + nH2O Me(OH)n + n/2H2 
Металлы менее активные взаимодействуют с водой лишь при нагревании:
Me + nH2O MeO + n/2H2 
Действие воды на металлы усиливается в присутствии растворенного в воде кислорода. Некоторые малоактивные металлы при этом окисляются по следующей схеме:
Me + n/2H2O + n/4O2 Me(OH)n
Со щелочами могут реагировать металлы, образующие амфотерные оксиды, или соединения металлов в высшей степени окисления, в присутствии сильных окислителей:
Me0 + H2O + OH– |
MeO2– + 3/2H2 |
||
2Me0 + 7Na O |
2 |
+ 6H O |
2NaMeO + 12NaOH |
2 |
2 |
4 |
|
Такие реакции характерны для V, Nb, W, Mn и других металлов, имеющих высшие степени окисления в соединениях.
69
Интенсивность действия водных растворов кислот на металлы соответствует положению металлов в ряду стандартных электродных потенциалов (прил. 8) и окислительным свойствам кислот. Чем больше разбавлена кислота и чем активнее металл, тем глубже идет восстановление.
Действие кислот на металлы, окислительная способность которых обусловлена окислительными свойствами недиссоциированных молекул и даже анионов, обладает определенными особенностями.
Особенность действия азотной кислоты на металлы состоит в том, что она окисляет металлы без выделения водорода даже из разбавленного раствора азотной кислоты. Степень окисления азота в азотной кислоте, равная +5, меняется до +4, +3, +2, +1 и 0 степени, и даже концентрированная азотная кислота действует на все металлы, кроме благородных.
Серная концентрированная кислота действует на металлы средней и малой активности только при нагревании, сера восстанавливается от степени +6 до степени +4 или до 0.
Концентрированные кислоты, анионы которых не обладают окислительными свойствами, как правило, с металлами не взаимодействуют.
Методика и порядок выполнения работы
Опыт 1. Взаимодействие металлов с водой
В 4 пробирки налейте по 6 капель дистиллированной воды, добавьте в каждую пробирку по 1 капле фенолфталеина и опустите
впервую пробирку кусочек магния, во вторую – кусочек железа,
втретью – кусочек алюминия, а в четвертую – кусочек меди. Наблюдаются ли какие-либо изменения? Нагрейте содержимое пробирок
впламени спиртовки до кипения. Отметьте наблюдаемые изменения
впробирке с магнием. Почему не появилось окрашивание в осталь-
ных пробирках? Чем оно вызвано?
Опыт 2. Взаимодействие металлов с кислотами
Рассмотрим некоторые случаи взаимодействия алюминия с кислотами.
Взаимодействие алюминия с разбавленной и концентриро-
ванной соляной кислотой. В две пробирки положите по кусочку алюминия и добавьте в одну 5–8 капель разбавленной, а в другую –
70
