- •Курсовая работа
- •1. Классификация терпеноидов
- •2. Физические свойства
- •3. Химические свойства
- •3.1 Гемитерпены
- •3.2 Монотерпены
- •3.2.1 Ациклические монотерпены
- •3.2.2 Моноциклические монотерпены
- •3.2.3 Бициклические монотерпены
- •3.3 Сесквитерпены
- •3.3.1 Ациклические сесквитерпены
- •3.3.2 Циклические сесквитерпены
- •3.3.2.1 Моноциклические сесквитерпены
- •3.3.2.2 Бициклические сесквитерпены
- •3.3.2.3 Трициклические сесквитерпены
- •3.4 Дитерпены
- •3.5 Тритерпены
- •3.6 Тетратерпены
- •3.7 Политерпены
- •4. Выделение терпенов и терпеноидов
- •5. Применение терпенов и терпеноидов
3.3.1 Ациклические сесквитерпены
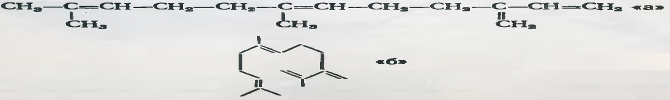
Можно рассматривать как ненасыщенные соединения жирного ряда с 4 двойными связями. Их структуру можно изобразить двояко: линейно или в виде незамкнутого бициклического соединения [1]:
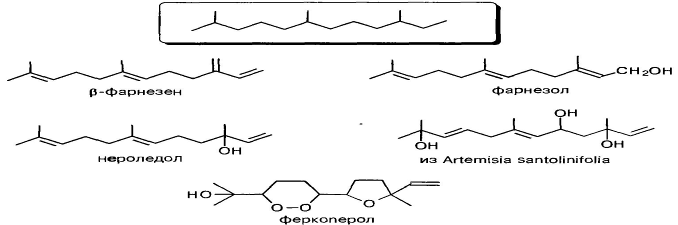
Важными ациклическими сесквитерпенами являются фарнезаны, производные 2,6,10-триметилдодекана. В природе найдены фарнезен (живицы хвойных семейства Pinaceae, масло хмеля), нероледол (широко распространен), фарнезол (эфирное масло липы и ландыша) и некоторые другие оксипроизводные этого ряда [5]:
3.3.2 Циклические сесквитерпены
Различают моноциклические, бициклические и трииклические сесквитерпены.
3.3.2.1 Моноциклические сесквитерпены
Представляют собой соединения с одним замкнутым гидроароматическим кольцом и с двумя двойными связями. Одна из связей находится в кольце, другая – в алифатической цепи. [1]
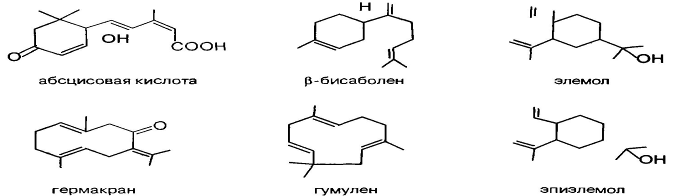
Моноциклические сесквитерпены представлены несколькими группами, различающимися по размеру цикла. Это соединения с циклогексановым фрагментом — циклофарнезаны, бисаболены, элеманы; соединения 1-изопропил-4,8-диметил-циклодекановой структуры — гермакраны; сесквитерпены гумуланового типа с 1,1,4,8-тетраметилциклоундекановым скелетом [5]:
Соединения гермакрановой группы интересны тем, что среди их функциональных производных на первое место выходят лактоны. Они многочисленны также во многих других группах сесквитерпенов, что и послужило причиной выделения их в отдельный класс природных соединений — сесквитерпеновые лактоны. Эти лактоны образуются взаимодействием спиртовой группы, находящейся в цикле и карбоксильной группой окисленного α-изопропильного фрагмента, формируя таким образом γ-лактоновое кольцо с разветвлением. В качестве разветвления выступают обычно метильная или метиленовая группа, последняя иногда функционализируется до эпоксидной, спиртовой или гликолевой. Сочленение углеводородного и лактонового циклов обычно имеет транс-конфигурацию, но иногда встречаются сесквитерпеновые лактоны цис-конфигурации [5]:

3.3.2.2 Бициклические сесквитерпены
Это соединения с двумя конденсированными неароматическими кольцами и двумя этиленовыми связями. [1] Бициклические сесквитерпены являются самой многочисленной группой терпенов по структурным типам. Наиболее распространенными из них являются: кадинаны, эудесманы, эремофиланы (4,4,0-бициклодекан); гваяны и каротаны (5,3,0-бициклодекан); кариофиланы (7,2,0-бициклодекан); спироциклические — ветиваны и шамиграны [5]:
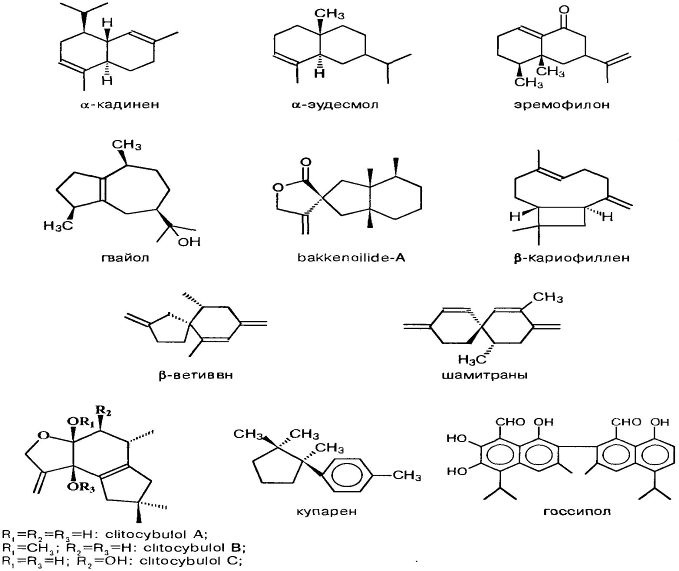
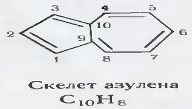
Особой группой среди бициклических сесквитерпенов являются производные азулена – высоконепредельного соединения с пятью двойными связями [1]:
Если проанализировать структурные формулы сесквитерпенов, приведенных выше, то можно достаточно однозначно предсказать целый ряд их химических превращений в соответствии со свойствами функциональных групп, у них имеющихся. Во-первых, это серия реакций олефиновых связей: электрофильное галогенирование, гидратация в присутствии кислот, различные реакции окисления — от способа Вагнера, ведущего к гликолям, до полного расщепления двойных связей до соответствующих кислот и т.д. Также для сесквитерпенов, содержащих гидроксильные, кетонные, альдегидные и карбоксильные группы, характерны реакции дегидратации, этерификации, окисления и т.д.
Структурное богатство сесквитерпенов делает их весьма лабильными соединениями. Конформационное и конфигурационное разнообразие их молекул, сочетание нескольких функциональных групп — все это служит предпосылкой для достаточно сложных и неоднозначных превращений сесквитерпеновых соединений.
Наиболее интересны и многогранны превращения сесквитерпенов, включающие образование промежуточных соединений и переходных состояний карбокатионного типа, провоцирующих рототропию и скелетные перегруппировки. Так, α-гумулен является неустойчивым соединением и легко изомеризуется на окиси алюминия в 3-изомер:

Прототропия имеет место и при дегидратации сесквитерпеновых спиртов: из эпиэлемола при отщеплении воды (в зависимости от используемого реагента) образуются изомерные эпи-элемены:
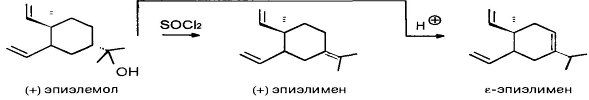
Некоторые реакции дегидратации сесквитерпеновых спиртов сопровождаются раскрытием циклов, особенно если исходная углеродная система существенно напряжена:
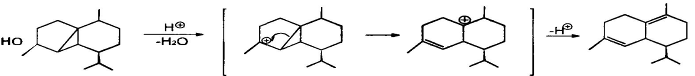
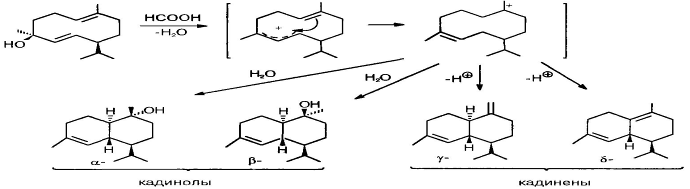
Часто при дегидратации сесквитерпеновых спиртов в кислых условиях происходят перегруппировки углеродного скелета. Так, гермакра-1,6-диен-5-ол при обработке муравьиной кислотой образует продукты трансаннулярной циклизации [5]: