
- •Курсовая работа
- •1. Классификация терпеноидов
- •2. Физические свойства
- •3. Химические свойства
- •3.1 Гемитерпены
- •3.2 Монотерпены
- •3.2.1 Ациклические монотерпены
- •3.2.2 Моноциклические монотерпены
- •3.2.3 Бициклические монотерпены
- •3.3 Сесквитерпены
- •3.3.1 Ациклические сесквитерпены
- •3.3.2 Циклические сесквитерпены
- •3.3.2.1 Моноциклические сесквитерпены
- •3.3.2.2 Бициклические сесквитерпены
- •3.3.2.3 Трициклические сесквитерпены
- •3.4 Дитерпены
- •3.5 Тритерпены
- •3.6 Тетратерпены
- •3.7 Политерпены
- •4. Выделение терпенов и терпеноидов
- •5. Применение терпенов и терпеноидов
3.2.3 Бициклические монотерпены
Представляют собой соединения с двумя конденсированными неароматическими кольцами и одной этиленовой связью, они наиболее интересны в плане химической реакционной способности. У углеводородов этой группы терпенов выделяются четыре типа соединений:
Карена;
Пинена;
Сабинена;
Камфена.
Эти четыре углеводорода, имеющие общую формулу С10Н16, отличаются друг от друга по положению малого цикла, или как еще иначе называют, «мостика». У карена он снаружи между С3 и С4; у всех остальных он внутренний между С2 и С4 – у пинена, С1 и С4 – у камфена и С6 – С4 – у сабинена.

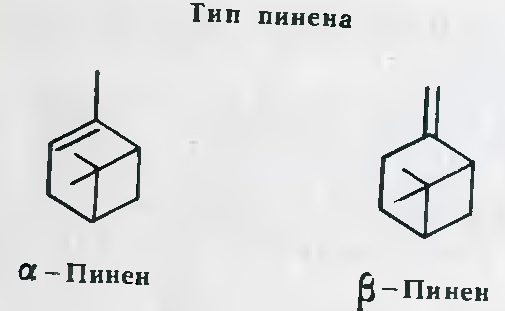
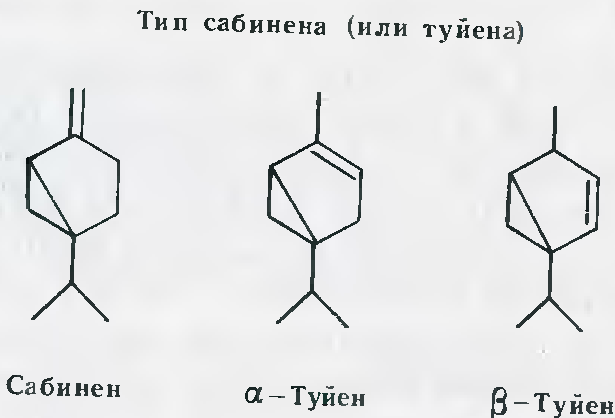
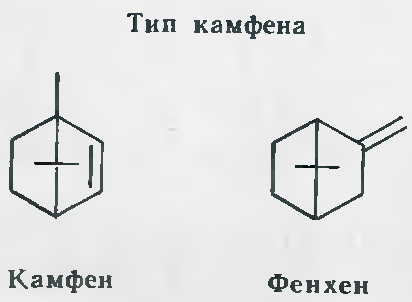
Кислородные производные в бициклических терпенах отличаются большим разнообразием. Из спиртов типичны сабинол, туйол, борнеол, миртенол, из кетонов – камфора, фенхон, туйон. [1]
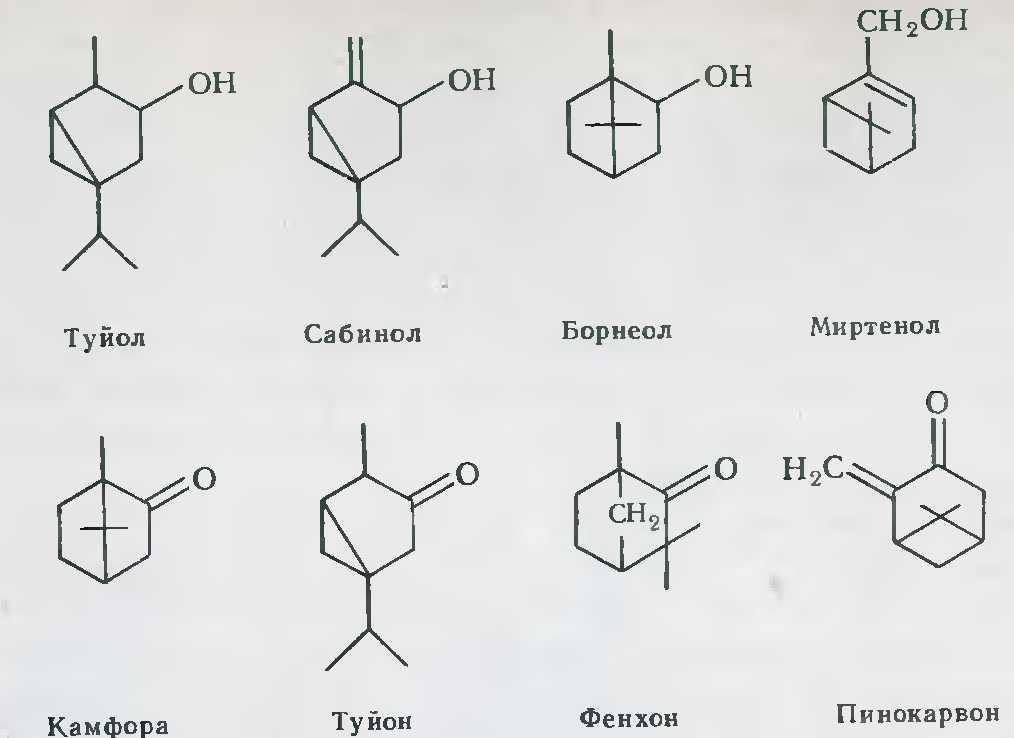
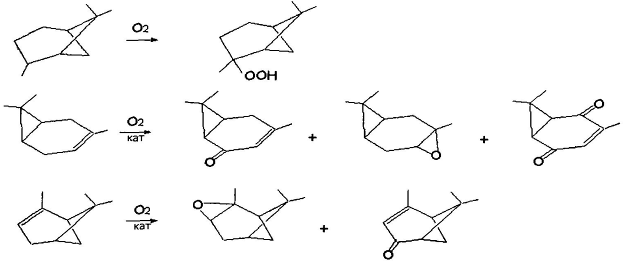
Бициклические монотерпены легко окисляются кислородом воздуха в присутствии различных катализаторов с образованием стабильных гидроперекисей в случае насыщенных соединений и карбонильных оксирановых производных в случае непредельных терпенов [5]:
α-Пинен (от лат. Pinus – сосна) – один из самых распространенных в природе терпенов, главный компонент скипидаров, получаемых из хвойных деревьев. α-Пинен находит широкое применение как растворитель и сырье для многих органических соединений, в частности в производстве тропина и камфоры.
Гидратация α-пинена протекает с разрывом π-связи и неустойчивого четырехчленного цикла и приводит к моноциклическому терпеноиду терпину [6]:
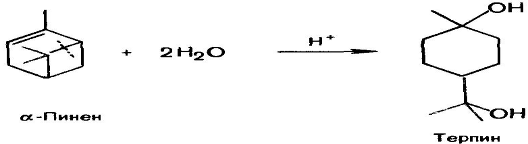
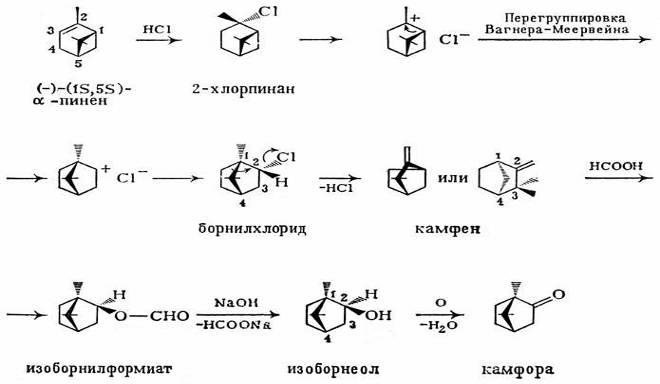
α-Пинен присоединяет хлористый водород с образованием неустойчивого 2-хлорпинана, которй претерпевает перегруппировку Вагнера-Меервейна с образованием борнилхлорида. Действием гидроксида щелочного металла от последнего отщепляют хлористый водород, при этом образуется камфен. Из него в результате присоединения муравьиной кислоты получают изоборнилформиат (эфир борнанола-2 с муравьиной кислотой) При омылении изоборнилового эфира муравьиной кислоты получается изоборнеол, который в заключение окисляют до камфоры [9]:
Камфора при нагревании в хлороформномрастворе взаимодействует с бромом с образованием бромкамфоры [2]:
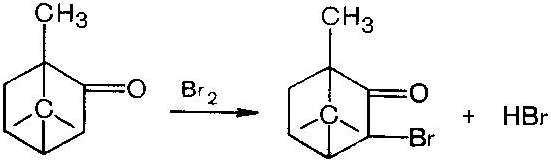
Замещение атома водорода на атом брома обусловлено подвижностью протона, находящегося в α-положении к карбонильной группе.
Благодаря наличию оксигруппы камфора способна реагировать с соединениями, содержащими аминогруппу. Например, с гидроксиламином камфора образует кристаллический оксим [6]:
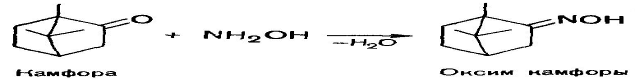
Идентификация.
Подвижный водород рядом с кетонногруппой камфоры может вступать в реакции конденсации с альдегидами. Продукты конденсации часто бывают окрашенными, поэтому эта реакция может быть использована для подтверждения подлинности камфоры. Например при конденсации с фрфуролом образуется сине-фиолетовое окрашивание:
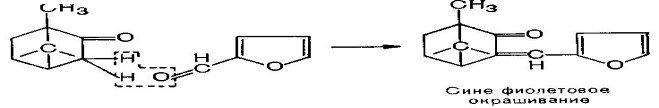
Аналогично с формальдегидом образуется красное окрашивание. [2]
3.3 Сесквитерпены
Сесквитерпены представляют собой самую обширную группу среди всех терпенов как по количеству соединений, обнаруженных в природе (их несколько тысяч), так и по множеству структурных вариантов и разнообразию типов углеродного скелета (их около двухсот). [5]
Развитие химии сесквитерпенов в значительной степени связано с трудами швейцарских ученых П.Ружички, А. Эшенмозера. Сесквитерпены содержатся в различных эфирных маслах растений и смолах. В эту же группу входят высокоактивные соединения, такие, как фитоалексины, защищающие растения от болезней, ихтиотоксины, обладающие высокой токсичностью для рыб, а также, многочисленные сесквитерпеновые лактоны, сходные, например, с глауколидом проявляющие высокий спектр биологической активности. Некоторые из сесквитерпенов (аналогично би - и тритерпенам) в качестве биохимических маркеров нефти используются для прогнозирования нефтяных запасов в недрах земли. [4]
Классификация сесквитерпенов, построена так же, как и у монотерпенов — по степени циклизации углеродного скелета. Но так как число соединений и структурных вариантов весьма велико в ряду сесквитерпенов, то в настоящее время при отнесении сесквитерпена к определенному типу учитывается не только углеродный скелет, но и пространственная структура молекулы.
