
- •Практическое занятие № 6
- •Основы молекулярно – кинетической теории идеального газа. Законы идеального газа.
- •Основные формулы Идеальные газы подчиняются уравнению состояния Менделеева - Клапейрона
- •1.2. Вопросы для повторения
- •Что надо уметь.
- •Примеры решения задач.
- •Анализ и решение.
- •Анализ и решение.
- •Поэтому дм3.
- •1.5. Задачи для самостоятельного решения
- •Литература
- •Что надо знать.
- •Средняя квадратичная скорость
- •Анализ и решение. Из основного уравнения молекулярно – кинетической теории газов
- •Анализ и решение.
- •Анализ и решение.
- •Анализ и решение.
- •Задачи для самостоятельного решения
- •Литература.
- •3.2. Вопросы для повторения.
- •Что надо знать.
- •Примеры решения задач.
- •3.5. Задачи для самостоятельного решения
- •Литература.
- •Практическое занятие № 9
- •4. Второй закон термодинамики. Энтропия.
- •4.1. Основные формулы
- •4.2. Вопросы для повторения.
- •Что надо знать.
- •Примеры решения
- •4.5. Задачи для самостоятельного решения
- •Литература.
- •5.2. Вопросы для повторения
- •5.3. Что надо знать.
- •5.4. Примеры решения задач.
- •5.5. Задачи для самостоятельного решения
- •Литература.
Задачи для самостоятельного решения
Какое количество молекул находится в комнате объемом 80 м3 при температуре 170С и давлении 750 мм рт. ст.?
Найти среднюю квадратичную скорость молекул воздуха при температуре 170С, считая воздух однородным газом, масса одного киломоля которого равна
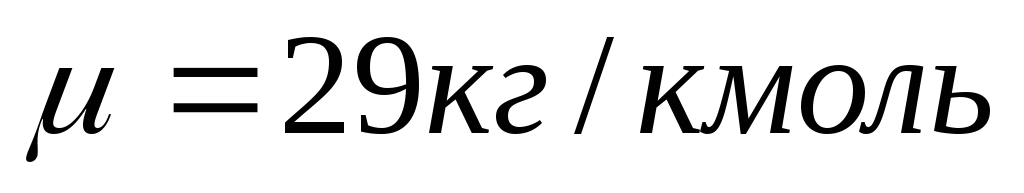
Плотность некоторого газа равна 6*10-2кг/м3, средняя квадратичная скорость молекул этого газа равна 500 м/сек. Найти давление, которое газ оказывает на стенки сосуда.
Найти внутреннюю энергию W массы m = 1 г воздуха при температуре t = 150С. Молярная масса воздуха
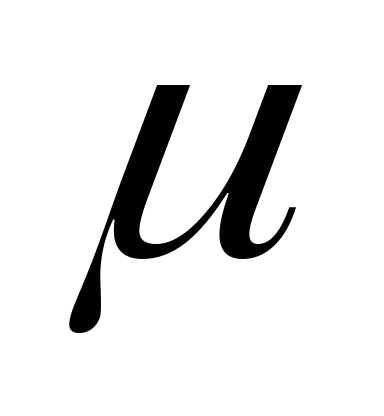 = 0,029 кг/моль.
= 0,029 кг/моль.
2.54. Найти энергию Wвр вращательного движения молекул, содержащихся в массе m = 1 кг азота при температуре t = 70С.
2.55.
1кг двухатомного газа находится под
давлением р = 8*104
н/м2
и имеет плотность
![]() =
4 кг/м3.
Найти энергию теплового движения молекул
газа при этих условиях.
=
4 кг/м3.
Найти энергию теплового движения молекул
газа при этих условиях.
2.56. Какое число молекул двухатомного газа занимает объем V = 10 см3 при давлении р = 40 мм рт. ст. и при температуре t = 270С? Какой энергией теплового движения обладают эти молекулы?
2.57. Найти удельную теплоемкость с кислорода для: а) V = const; б) p = const.
2.58.
Плотность некоторого двухатомного газа
при нормальных условиях
![]() =
1,43 кг/м3.
Найти удельные теплоемкости Сv
и Сp
этого газа.
=
1,43 кг/м3.
Найти удельные теплоемкости Сv
и Сp
этого газа.
2.59.
Найти удельные теплоемкости Сv
и Сp
некоторого газа, если известно, что
масса одного киломоля этого газа равна
![]() =
30 кг/к моль и отношение Сp
/Сv
= 1,4.
=
30 кг/к моль и отношение Сp
/Сv
= 1,4.
Литература.
И.В. Савельев. Курс общей физики. §101, §102. – М., Наука, 1973г.
М.А. Пак. Курс лекций по физике. Том 1. Классическая физика.
стр. 128-131. Алматы, 2000г.
В.С. Волкенштейн. Сборник задач по общему курсу физики. – М., Наука, 1986г.
4. Чертов А.Г., Воробьев Задачник по физике. – М., Высшая школа, 1981г.
Практическое занятие № 8
Первый закон термодинамики и процессы в газах.
3.1. Основные формулы
Первое начало термодинамики
dQ = dW + dA,
где dQ - количество теплоты, полученное газом, dW - изменение внутренней энергии газа, dA = PdV - работа, совершаемая газом при изменении его объема.
Изменения
внутренней энергии газа
![]() ,
где dT
- изменение температуры.
,
где dT
- изменение температуры.
Полная работа, совершаемая газом при изменении объема газа
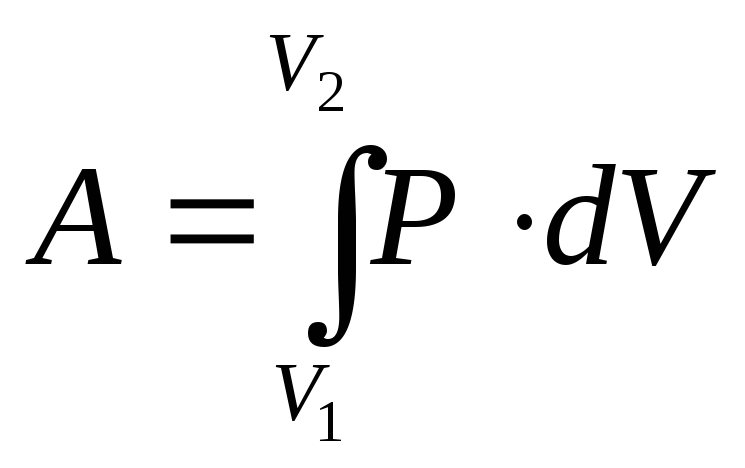
Работа, совершаемая при изотермическом изменении объема газа
![]()
Давление
газа и его объем связаны при адиабатическом
процессе уравнением Пуассона
![]() т.е.
т.е.
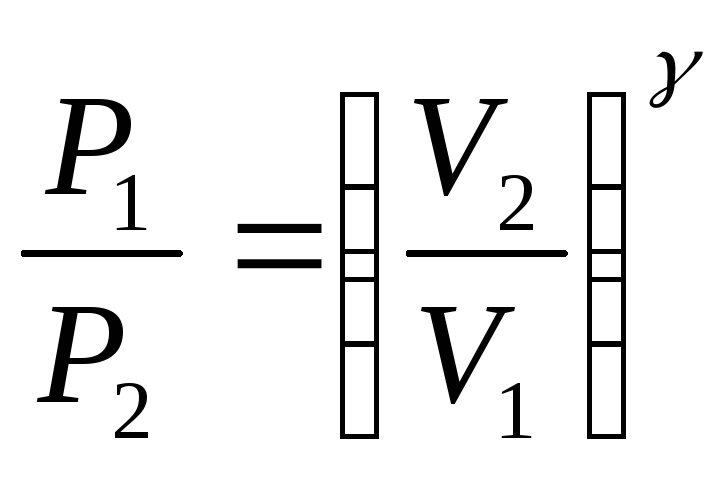 ,
где
,
где![]() ,
,![]() показатель
адиабаты.
показатель
адиабаты.
Уравнение Пуассона может быть записано еще в таком виде:
![]() ,
т.e.
,
т.e.
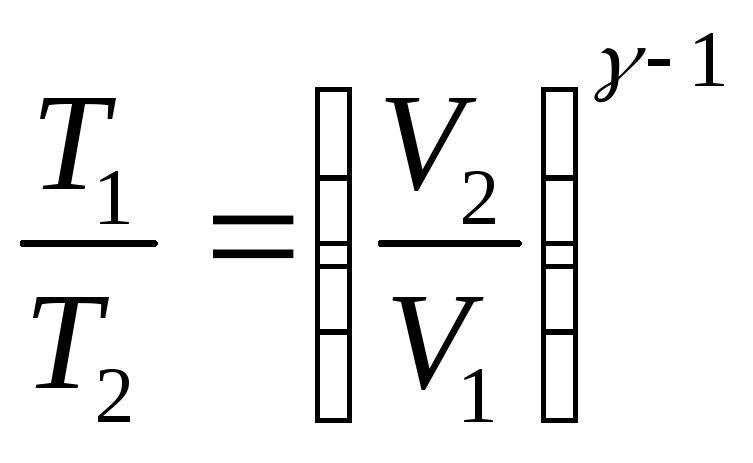
Работа, совершаемая при адиабатическом изменении объема может быть найдена по формуле:
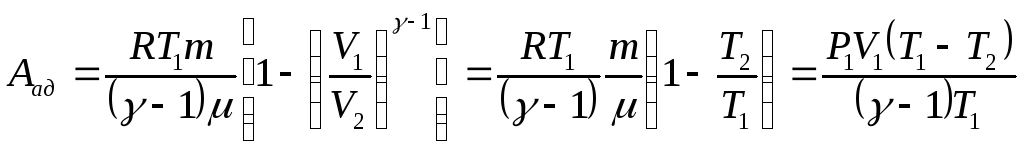
где P1 и V1 - давление и объем газа при температуре Т1.
3.2. Вопросы для повторения.
3.2.1. Сформулируйте первый закон термодинамики. Запишите его формулу.
3.2.2. Какие формы передачи энергии от одних тел к другим вы знаете?
3.2.3. Является ли работа и теплота функциями состояния системы.
3.2.4. Напишите формулы для расчета элементарной и полной работы, совершаемой при расширении газа.
3.2.5. Запишите первый закон термодинамики для изохорического процесса.
3.2.6. Запишите первый закон термодинамики для изобарического процесса.
3.2.7. Запишите первый закон термодинамики для изотермического процесса.
3.2.8. Какой процесс называется адиабатическим?
3.2.9. Запишите первый закон термодинамики для адиабатического процесса.
