
- •Теоретический курс
- •Раздел 1. Металловедение.
- •1.1. Общая характеристика металлов.
- •1.1.1. История познания металлов человеком
- •1.1.2. Кристаллическое строение
- •1.1.3. Типы кристаллических решеток
- •1.1.4. Анизотропия свойств кристаллов
- •1.1.5. Полиморфизм в металлах
- •1.1.6. Строение реальных кристаллов
- •Вопросы для самопроверки
- •2.2. Кристаллизация металлов
- •2.2.1. Теоретические основы
- •1.2.2. Механизм процесса кристаллизации
- •1.2.3. Основные явления кристаллизации слитков. Влияние формы кристаллов на служебные характеристики металла
- •Вопросы для самопроверки
- •1.3. Основы теории сплавов.
- •1.3.1. Внутреннее строение и свойства механических смесей, твердых растворов и химических соединений
- •1.3.2. Диаграммы состояния сплавов. Их типы и построение
- •Вопросы для самопроверки
- •1.4. Железоуглеродистые сплавы.
- •1.4.1. Железо
- •1.4.2. Углерод
- •1.4.3. Структурные составляющие системы железо-углерод
- •1.4.4. Диаграмма состояния железо – цементит (метастабильное равновесие)
- •Вопросы для самопроверки
- •1.5. Термическая обработка стали
- •1.5.1. Основы технологии термической обработки
- •1.5.2. Основные параметры процессов термической обработки
- •1.5.3. Основные виды термической обработки
- •1.5.4. Основные превращения в сталях в процессах термообработки
- •1.5.5. Химико-термическая обработка стали. Общая характеристика процессов
- •1.5.6. Термомеханическая обработка (тмо)
- •Вопросы для самопроверки
- •1.6. Физические основы пластичности и прочности металлов
- •1.6.1. Виды деформации
- •1.6.2. Механические свойства металлов
- •1.6.3. Влияние дефектов кристаллической решетки на прочность металла
- •1.6.4. Методы исследования строения, структуры и свойств металлов
- •Вопросы для самопроверки
- •1.7. Влияние температуры на структуру и свойства металлов
- •1.7.1. Диффузия ядер в металлах
- •1.7.2. Влияние повышения температуры на механические свойства
- •1.7.3. Возврат и рекристаллизация деформированного металла при нагреве
- •1.7.4. Сфероидизация и графитизация цементита в сталях
- •Вопросы для самопроверки
- •1.8. Углеродистые и легированные стали
- •1.8.1. Условия эксплуатации и требования к сплавам
- •1.8.2. Структура и основные свойства сталей
- •1.8.3. Принципы классификации и маркировки сталей
- •1.8.4. Конструкционные стали
- •1.8.5. Инструментальные стали
- •1.8.6. Легированные стали в энергетике
- •Вопросы для самопроверки
- •1.9. Чугуны
- •1.9.1. Классификация чугунов
- •1.9.2. Серые чугуны
- •1.9.3. Высокопрочные чугуны
- •1.9.4. Ковкие чугуны
- •1.9.5. Специальные чугуны
- •1.9.6. Маркировка чугунов
- •Вопросы для самопроверки
- •1.10. Сплавы на основе железа с различными металлами
- •Вопросы для самопроверки:
1.1.3. Типы кристаллических решеток
Для описания формы кристаллов пользуются системой кристаллографических осей аналогичной таковой в геометрических фигурах (х, у и z). Они представляют собой конечные отрезки и обозначаютсяа, b иc, углы между ними соответственно -,и. Величины данных отрезков - это расстояние между двумя соседними ядрами. Они называются параметрами или периодами кристаллической решетки и измеряются в нанометрах или ангстремах (1 нм = 0,1 Å = 10-9см). Для металлов величины периодов решеток лежат в интервале 2 - 6 Å.
Наименьшая часть объема кристаллической решетки, определяющая ее систему, называется элементарной ячейкой. Любое твердое тело построено из нескольких таких ячеек, которые расположены последовательно друг за другом в направлении осей координат.
Кристаллические решетки различаются по форме и размерам элементарных ячеек. Углы между координатными осями и длины параметров ячеек определяют их сингонию (систему). Практически все металлы кристаллизуются в основном в трех из семи существующих сингоний: кубической, гексагональной и тетрагональной (рис. 1.6). Кубические системы имеют простую кубическую, объемно- и гранецентрированные решетки.
В объемноцентрированной решетке ионы металлы расположены в узлах ячейки и один в центре объема куба (рис. 1.6, а). Ее имеют все щелочные металлы, -титан,-цирконий,-таллий, тантал,-железо, молибден, вольфрам, ванадий, хром, барий и др. В гранецентрированной решетке катионы металла находятся в узлах куба и в центре каждой грани (рис. 1.6, б). Они характерны для-кальция, германия,-стронция, тория, свинца, никеля, серебра, золота, палладия, платины, родия, иридия,-железа, меди и др. Гексагональная плотноупакованная решетка характеризуется расположением ионов металла в узлах ячейки и в центре шестигранных оснований, а также три катиона находятся в средней плоскости (рис. 1.6, в). В данной решетке кристаллизуются-гафний, магний,-таллий, кадмий, рений, осмий, цинк,-кобальт, бериллий,-таллий,-цирконий и др. Такие металлы как-олово и индий имеют тетрагональную решетку (рис. 1.6, г).
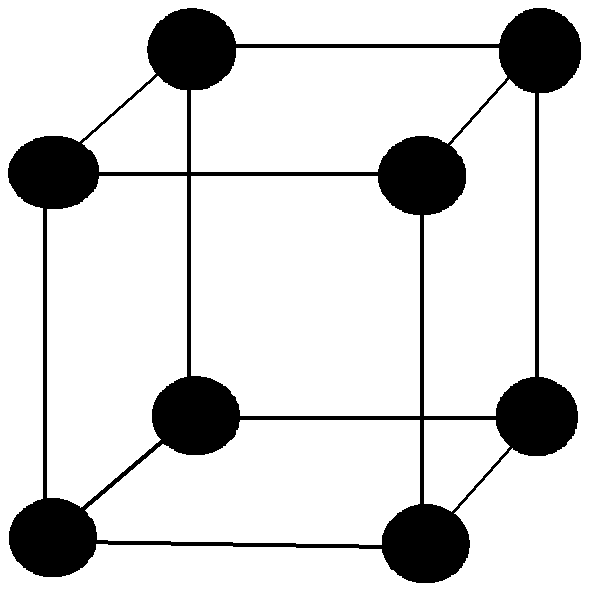
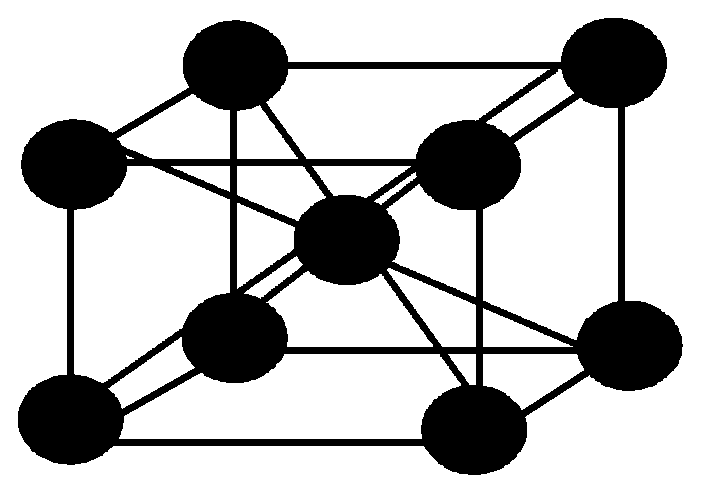
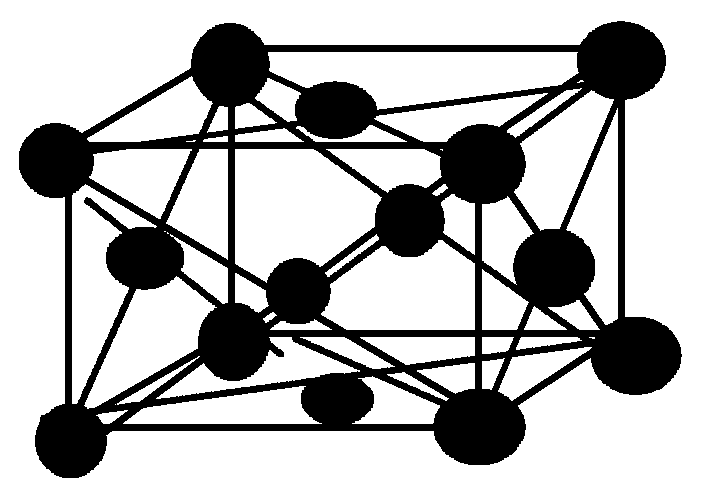
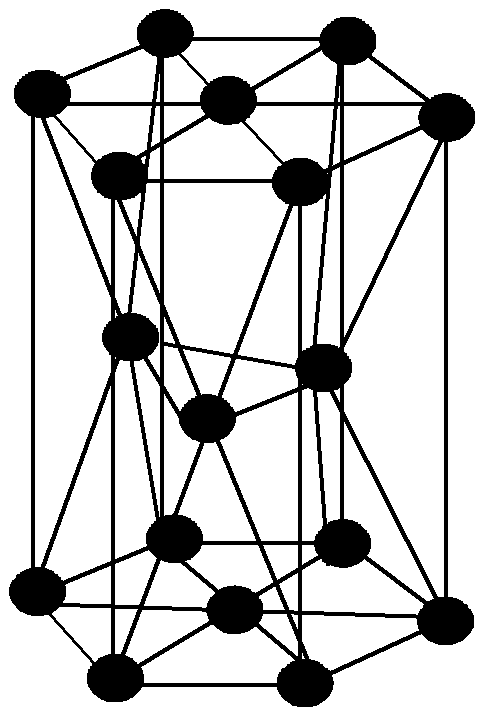
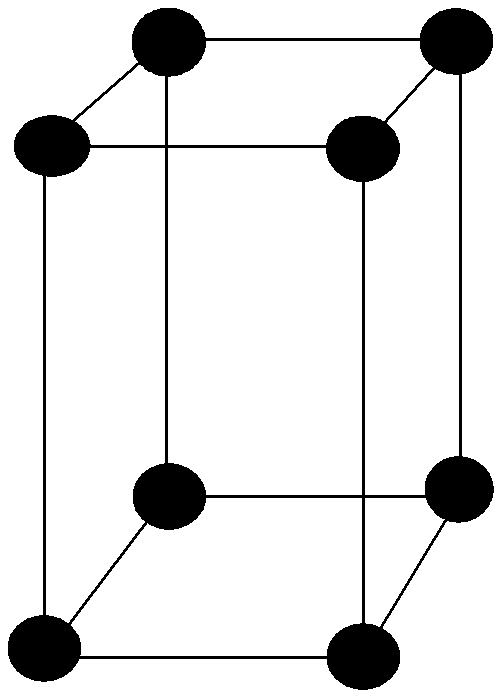
а б в г д
Рис. 1.6 - Кристаллические решетки металлов: а– кубическая,б– объемноцентрированная кубическая,в– гранецентрированная кубическая,г – гексагональная плотноупакованная,д - тетрагональная
Кристаллические решетки помимо типа определяются постоянной решетки и координационным числом. Постоянная решетки – размер ребра элементарной кристаллической решетки, представляющий собой расстояние между центрами двух ближайших соседних катионов. Для кубической решетки это ребро куба (а), его длина составляет10-8 см. В гексагональной решетке это два параметра:аис(рис. 1.6). Координационное число - количество соседних ядер, находящихся на одинаковом расстоянии от любого ядерного остова в решетке кристалла. Чем больше координационное число, тем выше плотность упаковки катионов в элементарной ячейке. В кубической объемноцентрированной решетке расстояние между ядрамиd= 0,5а3. На этом расстоянии от данного остова находятся 8 соседей, т. е. координационное число равно 8. Коэффициент заполнения ячейки катионами составляет 68 %. Для кубической гранецентрированной решетки координационное число равно 12 (12 соседей),d= 0,5а2. Для данной решетки характерна еще более плотная упаковка ядер в виде шаров. В гексагональной плотноупакованной решетке отношениес/а= 1,633; координационное число также равно 12. В данном случае плотность упаковки шаров тоже наибольшая. При отношениис/а= 1,57 - 1,64 упаковка атомов становится неплотной. Если это отклонение достаточно высокое, то координационное число в решетке приобретает значение 6. Эти две решетки более компактные, коэффициенты заполнения их объема ядрами составляет 74 %. При координационном числе равном 6 он уменьшается до 50 %, а при к.ч. 4 до 25 %.
Для описания направлений и плоскостей кристаллической структуры в кристаллографии применяется система индексов. Так, например, грань куба в элементарной ячейке имеет индексы (100), первая диагональная плоскость, проходящая через 2-е ребро куба – индексы (110), вторая плоскость, соединяющая 3-е ребро и вершины куба – (111). Обозначения индексов плоскостей пишутся в круглых скобках (рис. 1.7). Индексы направлений в кристаллической структуре совпадают с индексами плоскостей, перпендикулярных к этим направлениям, и записываются в квадратных скобках, например, [100], [110], [111] (рис. 1.8).
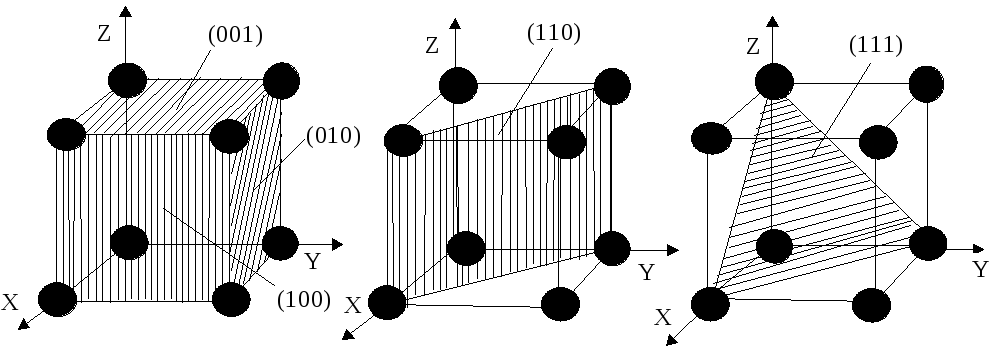
а б в
Рис. 1.7 - Индексы кристаллических плоскостей (а, б, в) в ОЦК
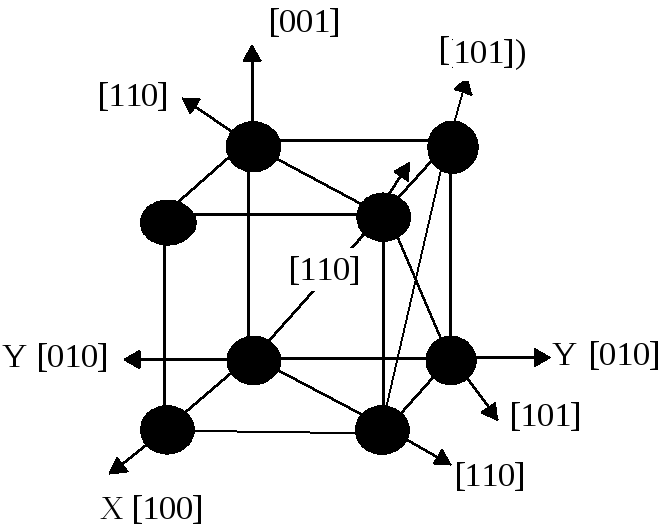
Рис. 1.8 - Индексы направлений в ОЦК
