
- •Контрольные работы общая химия
- •Часть 2
- •Оглавление
- •8. Электрохимические процессы
- •8.1. Степень окисления элемента
- •8.2. Окислительно-восстановительные реакции
- •8.3. Основные понятия электрохимических процессов
- •8.4. Ряд напряжений металлов
- •8.5. Гальванический элемент
- •8.6. Электролиз
- •8.7. Явление поляризации. Напряжение разложения
- •8.8. Примеры решения задач
- •8.9. Задачи для самостоятельного решения
- •Контрольные вопросы
- •9. Коррозия металлов
- •91.1. Классификация коррозионных процессов
- •Катодные процессы при коррозии
- •9.2. Методы защиты от коррозии
- •9.3. Примеры решения задач
- •9.4. Задачи для самостоятельного решения
- •Контрольные вопросы
- •10. Химия металлов
- •10.1. Металлическая связь
- •10.2. Зонная теория кристаллов
- •10.3. Химические свойства металлов
- •Продукты взаимодействия металлов с водой и некоторыми кислотами
- •Продукты пассивации некоторых металлов
- •10.4. Способы получения металлов
- •10.5. Способы очистки металлов
- •10.6. Сплавы металлов
- •10.6.1. Диаграммы состояния веществ, образующих механическую смесь
- •10.6.2. Диаграммы состояния веществ с неограниченной растворимостью
- •10.6.3. Диаграммы состояния веществ, образующих химическое соединение
- •10.7. Примеры решения задач
- •10.8. Задачи для самостоятельного решения
- •Контрольные вопросы
- •11. Химическая идентификация и анализ вещества
- •11.1. Качественный анализ
- •Кислотно-основная классификация катионов
- •Некоторые реагенты для идентификации катионов
- •11.2. Количественный анализ
- •11.3. Инструментальные методы анализа
- •11.4. Примеры решения задач
- •11.5. Задачи для самостоятельного решения
- •Контрольные вопросы
- •Библиографический Список Основная литература
- •Дополнительная литература
- •Перечень задач для выполнения контрольных работ
- •Стандартные электродные потенциалы металлов
Катодные процессы при коррозии
|
№ |
Электрохимический процесс |
Е, В |
рН |
|
1 |
2Н2О + 2е–= 2ОН–+ Н2 |
|
≈7 |
|
2 |
2Н++ 2е– = Н2 |
|
0 |
|
3 |
О2+ 2Н2О + 4е–= 4ОН– |
|
≈7 |
|
4 |
О2 +4Н++4е–= 2Н2О |
|
0 |
В соответствии с этими процессами по термодинамической неустойчивости металлы делят на пять групп.
1. Металлы повышенной термодинамической
нестабильности(![]() <
–0,413 В):Li,Rb,Cs,Ba,Sr,Ca,Na,Mg,Al,Ti,Zr,Mn,Cr,Zn,Fe. Эти металлы корродируют
даже в нейтральных средах в отсутствие
кислорода.
<
–0,413 В):Li,Rb,Cs,Ba,Sr,Ca,Na,Mg,Al,Ti,Zr,Mn,Cr,Zn,Fe. Эти металлы корродируют
даже в нейтральных средах в отсутствие
кислорода.
2. Металлы термодинамически нестабильные:Cd,In,Tl,Co,Ni,Mo,Pb,W(–0,413 В <![]() < 0
В). Водой не окисляются, но корродируют
в кислой среде, а также в нейтральной и
кислой средах, содержащих кислород.
< 0
В). Водой не окисляются, но корродируют
в кислой среде, а также в нейтральной и
кислой средах, содержащих кислород.
3. Металлы промежуточной
термодинамической стабильности
(0 В <
![]() <
0,816 В):Bi,
Sb,
Re,
Tc,
Cu,
Ag,
Rh.
Устойчивы в кислых и нейтральных средах
в отсутствие кислорода.
<
0,816 В):Bi,
Sb,
Re,
Tc,
Cu,
Ag,
Rh.
Устойчивы в кислых и нейтральных средах
в отсутствие кислорода.
4. Металлы высокой термодинамической
стабильности (0,816 В <![]() <
1,229 В):Hg,Pd,Ir,Pt. Могут
быть окислены в кислых средах при наличии
кислорода.
<
1,229 В):Hg,Pd,Ir,Pt. Могут
быть окислены в кислых средах при наличии
кислорода.
5. Металлы полной стабильности(![]() >1,229
В):Au. Такие металлы не
подвергаются коррозии.
>1,229
В):Au. Такие металлы не
подвергаются коррозии.
Так как катодный и анодный процессы проходят на разных участках поверхности, т. е. разделены пространственно и не мешают друг другу, то электрохимическая коррозия протекает значительно быстрее, чем химическая.
9.2. Методы защиты от коррозии
Для предупреждения коррозии используется комплекс противокоррозионных мероприятий, включающий защиту металлических поверхностей различными методами.
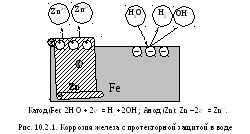
1. Протекторная защита – к защищаемому изделию присоединяют протекторы – более активные металлы. Защита будет действовать до тех пор, пока полностью не растворится анод – более электроотрицательный металл (рис. 10.2.1).
2. Катодная защита– защищаемое изделие соединяют с отрицательным полюсом источника постоянного тока, искусственно делают его катодом. Положительный полюс присоединяют к другому вспомогательному металлу, который помещают в ту же среду, что и защищаемое изделие.
3. Легирование.При легировании в состав сплава входят компоненты, вызывающие пассивирование металла.
4. Нанесение защитных покрытий. Неметаллические покрытия: лаки, краски, масла, полимеры, эмаль, восковые составы или кремнийорганические соединения.
Металлические покрытия: оцинковка, хромирование, лужение, никелирование, воронение, серебрение, позолота (обычно металлические пленки создают из металлов, образующих прочные оксидные пленки).
Различают анодные и катодные покрытия.
Анодныеболее электроотрицательны по отношению к защищаемому металлу, в электрохимическом ряду напряжений стоят левее защищаемого металла.
Катодныеболее электроположительны по отношению к защищаемому металлу, то есть в электрохимическом ряду напряжений металлов стоят правее защищаемого металла.
5. Удаление растворенного кислорода(применяется только в ограниченных объемах жидкости).
6. Введение ингибиторов – замедлителей коррозии. Ингибиторы создают на поверхности металлов защитную пленку либо уменьшают агрессивность среды. В качестве ингибиторов коррозии применяют многие неорганические и органические вещества и разнообразные смеси веществ.
