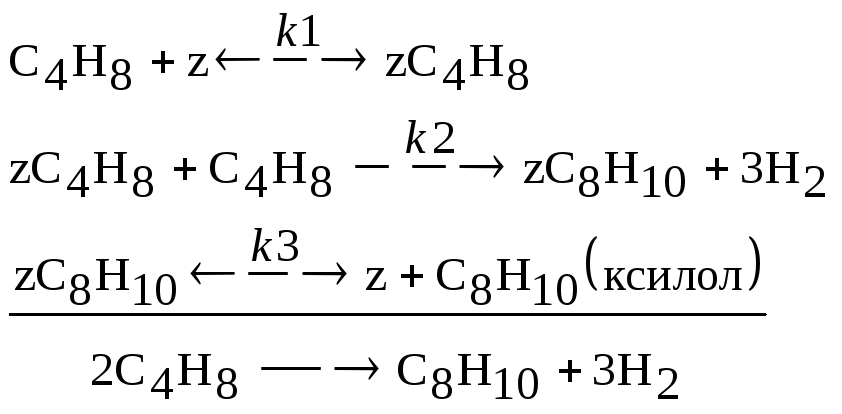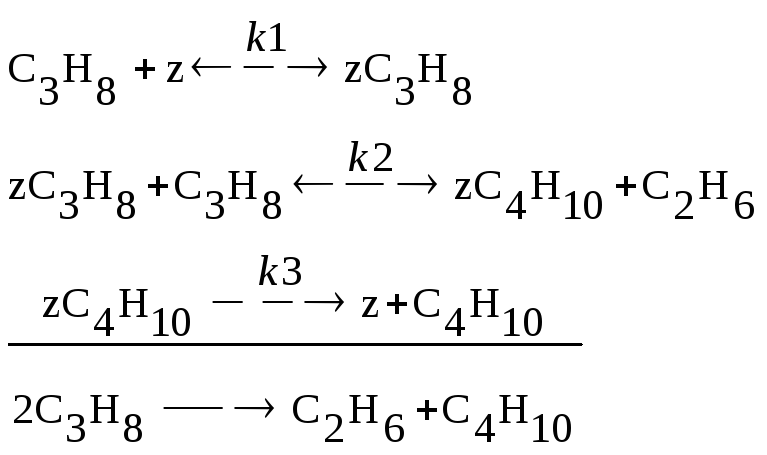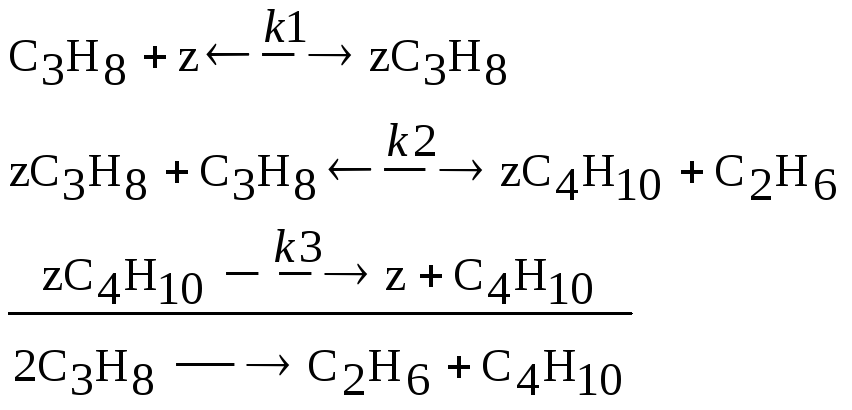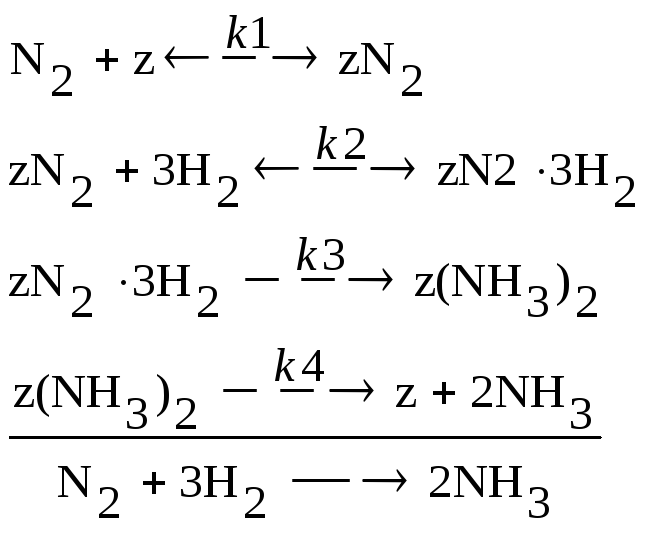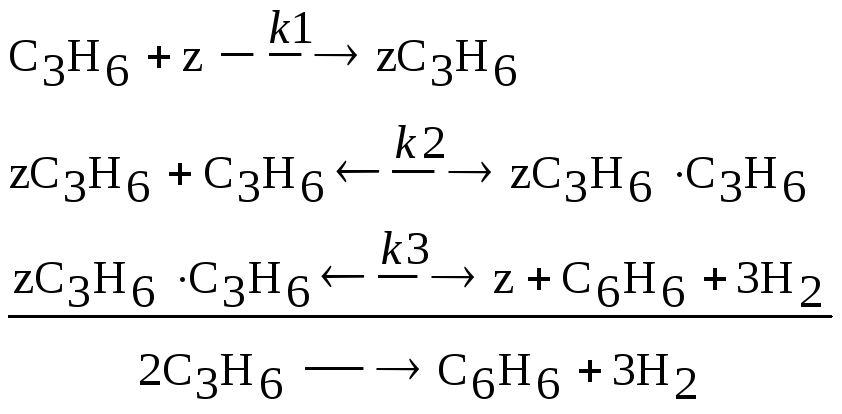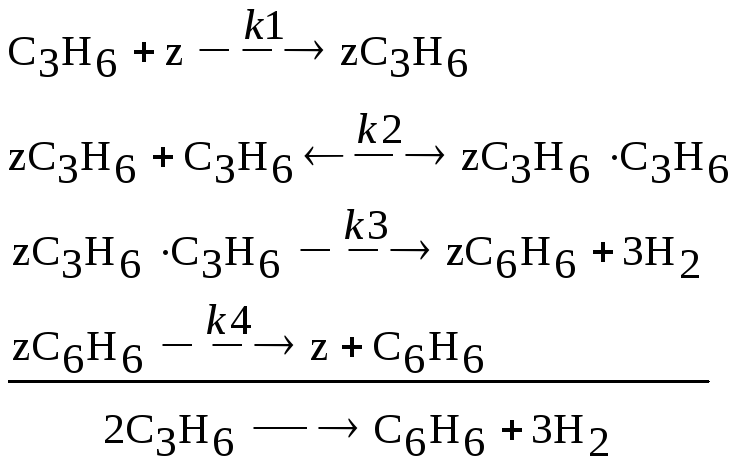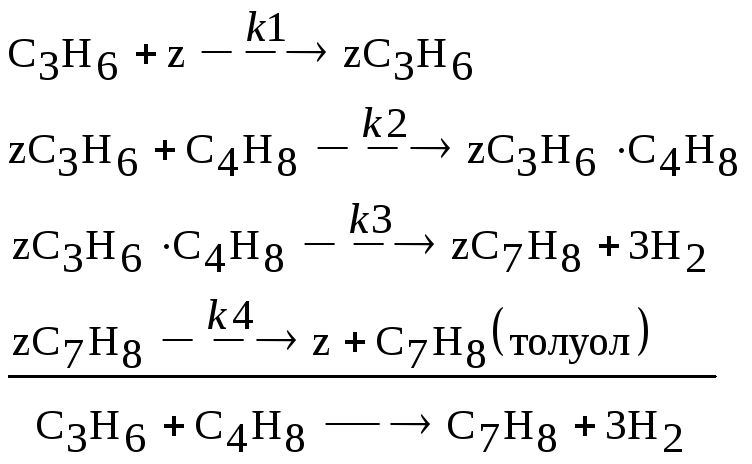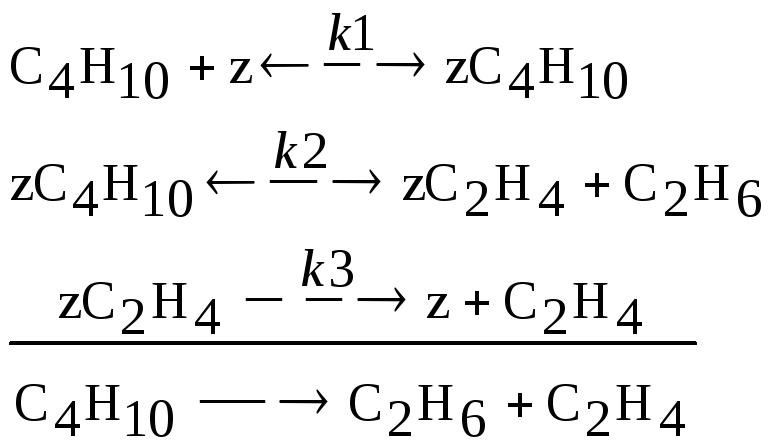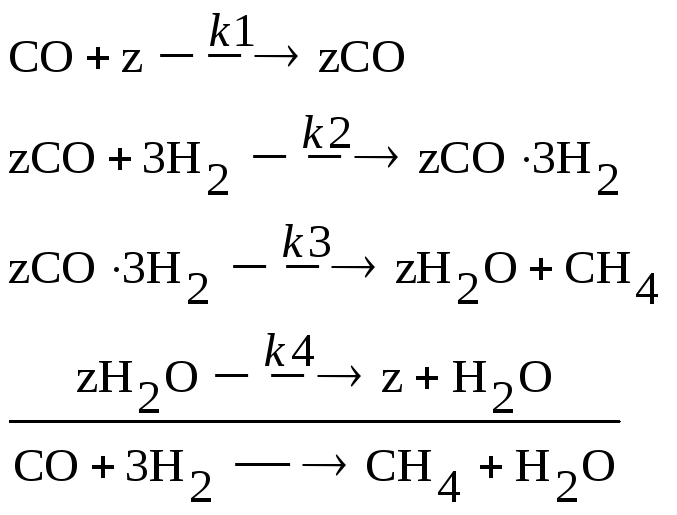- •А.В. Кравцов, н.В. Ушева, е.А. Кузьменко,
- •1. Моделирование кинетики химических реакций
- •1.1. Лабораторная работа №1 Моделирование кинетики гомогенных химических реакций
- •Этапы развития химической кинетики
- •Основные понятия химической кинетики
- •Общие представления одношаговых методов решения обыкновенных дифференциальных уравнений
- •Варианты заданий
- •1.2 Лабораторная работа №2 Моделирование кинетики гетерогенных химических реакций
- •Кинетика гетерогенных химических реакций
- •Варианты заданий
- •2. Моделирование структуры потоков в аппаратах
- •2.1. Лабораторная работа №3 Исследование гидродинамики насадочного абсорбера
- •Типовые математические модели структуры потоков в аппаратах
- •М f tатематическое описание гидродинамики насадочного абсорбера
- •Варианты заданий
- •Содержание отчета
- •2.2. Лабораторная работа №4 Моделирование процесса смешения технологических потоков нефтехимического производства
- •Математическое описание процесса смешения
- •Варианты заданий
- •3. Моделирование тепловых процессов химической технологии
- •3.1. Лабораторная работа №5 Моделирование теплообменных аппаратов в стационарном режиме
- •Моделирование и интенсификация работы теплообменной аппаратуры
- •Моделирование теплообменных процессов
- •Варианты заданий
- •Пример результатов расчетов
- •4. Моделирование массообменных процессов химической технологии
- •4.1. Лабораторная работа №6 Исследование процесса разделения многокомпонентной смеси в газовом сепараторе
- •Разделение газожидкостных потоков в химико-технологических процессах
- •Расчет однократного испарения многокомпонентной углеводородной смеси
- •Варианты заданий
- •4.2 Лабораторная работа №7 Математическое моделирование процесса ректификации
- •Описание объекта моделирования
- •Основные уравнения модели
- •Варианты заданий и исходные данные для расчета процесса ректификации
- •5. Моделирование химических реакторов
- •5.1. Лабораторная работа №8 Моделирование гомогенных химических реакторов
- •Классификация реакторов
- •Математическая модель реактора идеального перемешивания
- •Математическая модель реактора идеального вытеснения
- •Исследование химического процесса, протекающего в гомогенном реакторе идеального смешения
- •Исследование химического процесса, протекающего в реакторе идеального вытеснения в стационарном режиме
- •Литература
- •Приложения Приложение а Программы расчета кинетики гомогенных химических реакций
- •Расчет кинетики химических реакций методом Эйлера
- •Расчет температурной зависимости скоростей химических реакций с использованием метода Эйлера
- •Расчет кинетики химических реакций методом Рунге-Кутта
- •Приложение б Программа расчета кинетики гетерогенных химических реакций
- •Приложение в Программа расчета гидродинамики насадочного абсорбера
- •Приложение г Программа расчета смесителя
- •Приложение д Программа расчёта теплообменника
- •Приложение е Программы расчета гомогенных химических реакторов
- •Программа расчёта реактора идеального вытеснения
- •Файл с исходными данными
- •Программа расчёта реактора идеального смешения
- •Файл с исходными данными
- •Приложение ж
- •1. Моделирование кинетики химических реакций 3
- •Математическое моделирование химико-технологических процессов
Варианты заданий
Таблица 1.2
|
№ зада-ния |
Уравнение химической реакции |
Начальные концентрации, мольн. доли |
Значения констант скоростей |
|
1 |
2 |
3 |
4 |
|
1 |
|
СС5Н12(0)=0,64; CС2Н6(0)=0; CС3Н6(0)=0; Z(0)=1;
ZС5Н12(0)=0;
|
k1=0,43; k2=0,33; k3=0,21; k-1=0,07; k-2=0,12 |
|
2 |
|
СC4H8(0)=0,72; CC8H10(0)=0; CH2(0)=0; Z(0)=1;
Z
Z |
k1=0,38; k2=0,33; k3=0,29; k-1=0,13; k-3=0,07 |
|
3 |
Реакция диспропорционирования
|
СC3H8(0)=0,73; CC2H6(0)=0; СС4Н10(0)=0; Z(0)=1;
Z |
k1=0,48; k2=0,32; k3=0,30; k-1=0,12; k-2=0,08 |
Продолжение табл. 1.2
|
1 |
2 |
3 |
4 | |
|
4 |
Реакция изомеризации пентана
|
СC5H12(0)=0,64; Cизо-С5Н12(0)=0; Z(0)=1; Zн-С5Н12(0)=0; Zизо-С5Н12(0)=0 |
k1=0,32; k2=0,18; k3=0,14; k-1=0,09; k-2=0,08 | |
|
5 |
Реакция диспропорционирования
|
СC3H8(0)=0,73; CС2H6(0)=0; CC4H10(0)=0; Z(0)=1;
Z
Z |
k1=0,54; k2=0,48; k3=0,38; k-1=0,02; k-2=0,11 | |
|
6 |
Реакция диспропорционирования
|
СС3H8(0)=0,73; CС2H6(0)=0; CC4H10(0)=0; Z(0)=1;
Z |
k1=0,54; k2=0,43; k-1=0,0; k-2=0,11 | |
|
7 |
|
CN2(0)=0,2; CH2(0)=0,8; CNH3(0)=0; Z(0)=1; ZN2(0)=zN2 3H2(0)= =Z(NH3)2(0)=0 |
k1=0,32; k2=0,29; k3=0,44; k4=0,25; k-1=0,32; k-2=0,29 | |
|
8 |
Реакция олигомеризации
|
СC3H6(0)=0,5; CC6H6(0)=0; CH2(0)=0; Z(0)=1; ZС3Н6(0)=0; ZС3Н6С3Н6(0)=0 |
k1=0,15; k2=0,10; k3=0,08; k-2=0,01; k-3=0,005 | |
|
9 |
Реакция олигомеризации
|
СC3H6(0)=0,5; ZC6H6(0)=0; CH2(0)=0; Z(0)=1; ZС3Н6(0)=0; Z С3Н6*С3Н6(0)=0 |
k1=0,15; k2=0,10; k3=0,08; k4=0,12 | |
Окончание таблицы 1.2
|
1 |
2 |
3 |
4 |
|
10 |
Реакция олигомеризации
|
СС4Н8(0)=0,5; СС3Н6(0)=0,5; СС7Н8(0)=0; СН2(0)=0; Z(0)=1; ZС3Н6(0)=0; ZС4Н8(0)=0; zC7H8(0)=0 |
k1=0,2; k2=0,10; k3=0,08; k4=0,1
|
|
11 |
Реакция крекинга
|
C СС2Н6(0)=0; СС2Н4(0)=0; Z(0)=1; ZC4H10(0)=0;
Z |
k1=0,17; k2=0,12; k3=0,095; k-1=0,051; k-2=0,043 |
|
12 |
|
ССО(0)=0,26; СН2(0)=0,85; ССН4(0)=0; СН2О(0)=0; Z(0)=1; ZCO(0)=ZCO3H2(0)= =zH2O=0 |
k1=0,23; k2=0,41; k3=0,44; k4=0,25 |
П орядок
выполнения работы
орядок
выполнения работы
1. Составить кинетическую модель гетерогенной химической реакции.
2. Выбрать метод решения системы дифференциальных уравнений.
3. Разработать программу расчета и провести расчеты на ЭВМ.
4. Обсудить результаты. Сделать выводы по работе.
5. Составить отчет.
Контрольные вопросы и задания
Для каких реакций применим ЗДП?
Что такое гетерогенная химическая реакция?
Сформулируйте понятие скорости гетерогенной химической реакции.
Что такое механизм химической реакции?
Чем отличается кинетическая модель гетерогенной и гомогенной химических реакций?