
- •А.В. Кравцов, н.В. Ушева, е.А. Кузьменко,
- •1. Моделирование кинетики химических реакций
- •1.1. Лабораторная работа №1 Моделирование кинетики гомогенных химических реакций
- •Этапы развития химической кинетики
- •Основные понятия химической кинетики
- •Общие представления одношаговых методов решения обыкновенных дифференциальных уравнений
- •Варианты заданий
- •1.2 Лабораторная работа №2 Моделирование кинетики гетерогенных химических реакций
- •Кинетика гетерогенных химических реакций
- •Варианты заданий
- •2. Моделирование структуры потоков в аппаратах
- •2.1. Лабораторная работа №3 Исследование гидродинамики насадочного абсорбера
- •Типовые математические модели структуры потоков в аппаратах
- •М f tатематическое описание гидродинамики насадочного абсорбера
- •Варианты заданий
- •Содержание отчета
- •2.2. Лабораторная работа №4 Моделирование процесса смешения технологических потоков нефтехимического производства
- •Математическое описание процесса смешения
- •Варианты заданий
- •3. Моделирование тепловых процессов химической технологии
- •3.1. Лабораторная работа №5 Моделирование теплообменных аппаратов в стационарном режиме
- •Моделирование и интенсификация работы теплообменной аппаратуры
- •Моделирование теплообменных процессов
- •Варианты заданий
- •Пример результатов расчетов
- •4. Моделирование массообменных процессов химической технологии
- •4.1. Лабораторная работа №6 Исследование процесса разделения многокомпонентной смеси в газовом сепараторе
- •Разделение газожидкостных потоков в химико-технологических процессах
- •Расчет однократного испарения многокомпонентной углеводородной смеси
- •Варианты заданий
- •4.2 Лабораторная работа №7 Математическое моделирование процесса ректификации
- •Описание объекта моделирования
- •Основные уравнения модели
- •Варианты заданий и исходные данные для расчета процесса ректификации
- •5. Моделирование химических реакторов
- •5.1. Лабораторная работа №8 Моделирование гомогенных химических реакторов
- •Классификация реакторов
- •Математическая модель реактора идеального перемешивания
- •Математическая модель реактора идеального вытеснения
- •Исследование химического процесса, протекающего в гомогенном реакторе идеального смешения
- •Исследование химического процесса, протекающего в реакторе идеального вытеснения в стационарном режиме
- •Литература
- •Приложения Приложение а Программы расчета кинетики гомогенных химических реакций
- •Расчет кинетики химических реакций методом Эйлера
- •Расчет температурной зависимости скоростей химических реакций с использованием метода Эйлера
- •Расчет кинетики химических реакций методом Рунге-Кутта
- •Приложение б Программа расчета кинетики гетерогенных химических реакций
- •Приложение в Программа расчета гидродинамики насадочного абсорбера
- •Приложение г Программа расчета смесителя
- •Приложение д Программа расчёта теплообменника
- •Приложение е Программы расчета гомогенных химических реакторов
- •Программа расчёта реактора идеального вытеснения
- •Файл с исходными данными
- •Программа расчёта реактора идеального смешения
- •Файл с исходными данными
- •Приложение ж
- •1. Моделирование кинетики химических реакций 3
- •Математическое моделирование химико-технологических процессов
Исследование химического процесса, протекающего в реакторе идеального вытеснения в стационарном режиме
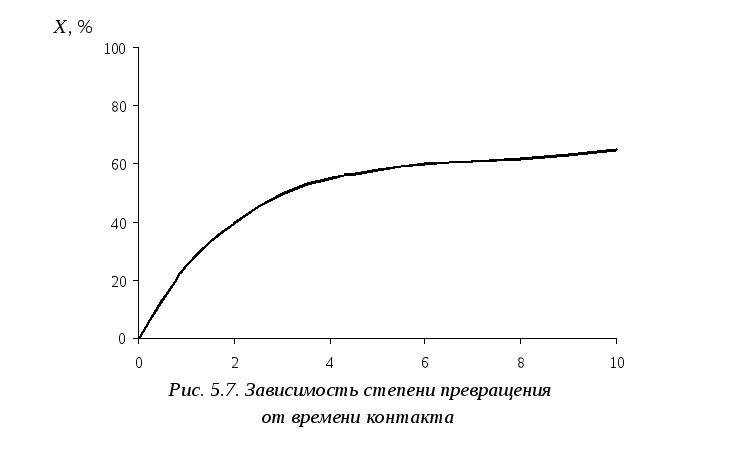
Исследование закономерностей протекания химической реакции в реакторе идеального вытеснения методом математического моделирования заключается в определении концентраций реагирующих веществ на выходе из реактора и температуры потока в зависимости от времени контакта.
Пусть в реакторе идеального вытеснения (РИВ) протекает химическая реакция
![]() .
(5.18)
.
(5.18)
Так как в реакторе вытеснения состав реагентов и температура потока изменяются по длине (или времени контакта) аппарата, процесс в нём описывается системой дифференциальных уравнений (5.11, 5.12).
Тогда математическая модель химического процесса может быть записана в виде следующей системы уравнений материального и теплового балансов (режим работы реактора – стационарный):
![]() ;
;
![]() ;
(5.19)
;
(5.19)
![]() ;
;
![]() ;
;
![]() ,
,
где k1, k2– константы скоростей реакций;
СA, СB, СC, СD– концентрации компонентов, кмоль/м3.
Значения тепловых эффектов реакций и теплоёмкость смеси рассчитываем с использованием справочных данных [8].
Систему дифференциальных уравнений (5.19) решим с использованием метода Эйлера.

![]() ,
c
,
c

![]() ,
c
,
c
![]() ,
c
,
c
Варианты заданий
Таблица 5.1
|
№ п/п |
Тип реакции |
Исходная концентрация, кмоль/м3 |
Констан-ты скорости |
Энергии активации, кДж/моль |
Темпе-ратура, К |
|
1 |
|
СC8H18 = 0,0388 |
k1=0,12; k2=0,80 |
E1=94,2; E2=81,2 |
610 |
|
2 |
|
Сн-С7Н1 =0,0343 |
k1=0,18; k2=0,29 |
E1=95,11; E2=122,76 |
690 |
|
3 |
|
СC2H4 = 0,0296 |
k1=0,38; k2=0,14; k3=0,11 |
E1=59,48; E2=162,57; Е3=157,12 |
800 |
|
4 |
k1
C k2 |
СC2H6 =0,0175; СC4H10=0,0117 |
k1=0,54; k2=0,12 |
E1=96,14; E2=83,60 |
810 |
Продолжение табл. 5.1
|
5 |
k1
С
i- C5H12 |
CС5Н10=0,0166; СН2=0,0166 |
k1=0,5; k2=0,2 |
E1=101,21; E2=115,05 |
710 |
|
|
k1
С k2 2,3-диметилбутан |
СС6Н14=0,0338 |
k1=0,4; k2=0,2 |
E1=75,13; E2=94,18 |
700 |
|
7 |
k1 С6Н14
2,3-диметилбутан |
СС6Н14=0,0394 |
k1=0,2; k2=0,4 |
E1=95,31; E2=76,17 |
600 |
|
|
k1
С k2 k3 2,3-диметилбутан |
СС6Н14=0,0328 |
k1=0,3; k2=0,2; k3=0,1 |
E1=79,64; E2=83,23; E3=107,11 |
720 |
|
9 |
k1
С
2,3-диметилбутан |
СС6Н14=0,0358 |
k1=0,25; k2=0,10; k3=0,25 |
E1=87,23; E2=104,75; E3=78,61 |
660 |
|
10
|
|
СC8H18 = 0,036 |
k1=0,12; k2=0,80 |
E1=94,2; E2=81,2 |
620
|
|
11
|
|
СС7Н16 =0,028 |
k1=0,18; k2=0,29 |
E1=95,11; E2=122,76 |
650
|
|
12 |
|
СC2H4 = 0,0316 |
k1=0,38; k2=0,14; k3=0,11 |
E1=59,48; E2=162,57; Е3=157,12 |
760
|
|
13 |
k1
C k2 |
СC2H6 =0,016; СC4H10=0,016 |
k1=0,54; k2=0,12 |
E1=96,14; E2=83,60 |
790
|
Окончание табл. 5.1
|
14 |
k1
С
i- C5H12 |
CС5Н10=0,017; СН2=0,014 |
k1=0,5; k2=0,2 |
E1=101,21; E2=115,05 |
710
|
|
|
k1
С k2 2,3-диметилбутан |
СС6Н14=0,0286 |
k1=0,4; k2=0,2 |
E1=75,13; E2=94,18 |
680
|
|
16 |
k1 С6Н14
2,3-диметилбутан |
СС6Н14=0,0283 |
k1=0,2; k2=0,4 |
E1=95,31; E2=76,17 |
580 |
Коэффициенты ai, bi, ci, di для расчета теплоемкостей компонентов и термодинамические функции индивидуальных углеводородов приведены в табл. 4, Приложение Ж.
Порядок выполнения работы
В соответствии с заданием составить математическое описание химического реактора.
Разработать алгоритм и программу расчёта.
Провести расчёты изменения концентраций веществ, температуры, степени превращения от времени и времени контакта.
Полученные результаты оформить в виде таблиц и графиков.
Составить отчёт о проделанной работе.
Содержание отчета
Представить математическую модель реактора со всеми параметрами, алгоритм и описание программы.
Обосновать выбор численного метода решения математической модели.
Представить таблицы и графики, обсуждение результатов, сделать выводы по проделанной работе.
Контрольные вопросы и задания
Какие основные типы химических реакторов вы знаете?
Поясните причины многообразия классификаций химических реакторов.
Какие математические модели химических реакторов вы можете назвать?
Какие составляющие входят в математическую модель гомогенного химического реактора?
В чем отличие уравнений теплового баланса адиабатического и политропического реакторов?
Дайте определение времени контакта и напишите расчетную формулу.
Что такое стационарный и динамический режимы работы химического реактора?
Какие параметры влияют на продолжительность выхода реактора на стационарный режим?
Какие численные методы можно применить, если математическая модель химического реактора представляет собой систему дифференциальных уравнений первого порядка?
Приведите примеры гомогенных химических промышленных процессов.








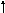

 2H6+C4H10
2C3H8
2H6+C4H10
2C3H8 5Н10
+ Н2
C5H12
5Н10
+ Н2
C5H12 k2
k2 6
6 6Н14
2-метилпентан
6Н14
2-метилпентан 2-метилпентан
2-метилпентан k2
k2
 8
8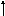
 6Н14
2-метилпентан
6Н14
2-метилпентан

 6Н14
2-метилпентан
6Н14
2-метилпентан k3
k2
k3
k2





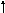


 2H6+C4H10
2C3H8
2H6+C4H10
2C3H8 5Н10
+ Н2
C5H12
5Н10
+ Н2
C5H12 k2
k2 15
15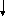 6Н14
2-метилпентан
6Н14
2-метилпентан 2-метилпентан
2-метилпентан k2
k2