
- •Химия Учебное наглядное пособие
- •Содержание
- •Раздел 1. Основные понятия и законы химии
- •1.1. Атомно-молекулярное учение
- •1.2. Законы химии
- •Закон сохранения массы вещества
- •Способы выражения количества вещества эквивалентов
- •Раздел 2. Классификация неорганических веществ
- •2.1.Оксиды
- •Химические свойства оксидов
- •2.2. Гидроксиды металлов
- •Химические свойства гидроксидов
- •Доказательство амфотерности
- •2.3. Кислоты
- •2.4. Соли
- •Средние кислые основные
- •Получение солей
- •2.5. Комплексные соединения
- •Раздел 3. Растворы
- •3.1. Способы выражения концентрации растворов
- •3.2. Растворы неэлектролитов
- •3.3. Растворы электролитов. Электролитическая диссоциация
- •3.4. Ионно-молекулярные уравнения реакций
- •3.5. Гидролиз
- •Раздел 4. Элекрохимические системы
- •Законы Фарадея
- •4.1. Степень окисления
- •4.2. Окислительно-восстановительные реакции (овр)
- •Направление овр
- •4.3. Гальванический элемент Даниэля-Якоби
- •4.4. Электродвижущая сила (эдс)
- •Стандартный водородный электрод
- •4.5. Электролиз
- •Электролиз с инертным анодом
- •Электролиз с растворимым анодом
- •4.6. Коррозия и защита металлов от коррозии
- •Защита металлов от коррозии
- •Раздел 5. Периодический закон д.И.Менделеева
- •5.1. Строение атома
- •Состав ядра
- •5.2. Модель состояния электрона в атоме Квантовые числа
- •Возможные значения квантовых чисел
- •5.3.Основные положения строения электронных оболочек атома
- •Ряд последовательного заполнения электронами орбиталей
- •Раздел 6. Химическая связь
- •Раздел 7. Химическая кинетика и равновесие
- •Раздел 8. Химическая термодинамика
- •8.1. Параметры состояния системы
- •8.2. Закон Гесса
- •Раздел 9. Химия элементов
- •Углерод c
- •Физические свойства аллотропных модификаций c
- •Химические свойства с
- •Соединения с
- •Кремний Si
- •Соединения Si
- •Соединения n
- •Соли аммония
- •Особые химические свойства
- •Разложение нитратов: фосфор p
- •Соединения р
- •Халькогены
- •Кислород
- •Соединения s
- •Галогены f, Cl, Br, I хлор Cl2
- •Соединения Cl
- •Подгруппа хрома
- •Хром Cr
- •Подгруппа железа
- •Железо Fe
- •Раздел 10. Органическая химия
- •10.1.Углеводороды Предельные углеводороды. Алканы
- •Непредельные углеводороды. Алкены
- •Диеновые углеводороды
- •Ароматические углеводороды. Ряд бензола. Арены
- •Нефть и ее переработка
- •10.2. Кислородсодержащие органические соединения Спирты
- •Альдегиды
- •Формальдегид
- •Ацетальдегид
- •Поликонденсация
- •Кетоны r – c – r
- •Карбоновые кислоты
- •Определение строения веществ
- •11.1. Методы качественного анализа (реакции обнаружения) Окрашивание пламени (предварительная проба)
- •Реакции осаждения
- •Реакции с выделением газа
- •Качественный элементный анализ
- •Цветные реакции
- •Обнаружения газов
- •Реакции обнаружения органических соединений
- •Индентификация синтетических материалов
- •11.2. Методы количественного анализа Титриметрический анализ (объемный анализ)
- •Кондуктометрическое титрование
- •Потенциометрия
- •Окислительно-восстановительное титрование
- •Комплексонометрия
- •Осадительное титрование
- •Аргентометрия
- •Гравиметрия
- •11.3. Спектроскопические методы анализа
- •Ультрафиолетовая спектроскопия и абсорбционная спектроскопия в видимой области
- •Характерные инфракрасные полосы поглощения
- •Спектроскопия ядерного магнитного резонанса
- •11.4. Дифрактометрический метод анализа
- •Дифракция рентгеновых лучей для определения типа кристаллической решетки
- •Дифракция рентгеновых лучей для определения электронной плотности
- •Раздел 12. Химия окружающей среды Глобальные аспекты
- •Загрязнение окружающей среды
- •Охрана окружающей среды
- •Атмосфера как область окружающей среды
- •Загрязнение воздуха
- •Влияние вредных веществ на окружающую среду
- •Методы очистки воздуха
- •Гидросфера как область окружающей среды
- •Вредные примеси питьевой воды
- •Жёсткость воды
- •Сточные воды
- •Вредные вещества в сточных водах
- •Поступления сточных вод
- •Литосфера как область окружающей среды
- •Удобрения
- •Загрязнение стойкими биоцидами
- •Заражение ядовитыми тяжелыми металлами
- •Методы санации зараженных почв
- •Отходы в окружающей среде
- •Вторичное использование
- •Продовольствие и питание
- •Углеводы в качестве пищевого продукта
- •Жиры в качестве пищевого продукта
- •Протеины как продукт питания
- •Витамины
- •Минеральные вещества
- •Микроэлементы
- •Пищевые добавки
- •Консерванты
- •Раздел 13. Коллоидная химия
- •Адсорбция, ее виды
- •Дисперсные системы
- •Коллоидные растворы
- •Строение коллоидных частиц
- •Приложение а Физико-химические постоянные
- •Групповые названия химических элементов
- •Растворимость веществ в воде при температуре 25 °с
- •Эбуллиоскопические (Кэ) и криоскопические (Ккр) константы некоторых растворителей
- •Произведения растворимости некоторых малорастворимых электролитов при 25 °с
- •Возможные степени окисления элементов
- •Электронное строение атомов в основном состоянии
- •Стандартные термодинамические функции образования
- •Нормальные (стандартные) окислительно-восстановительные потенциалы е0 в водных растворах при 25 0с по отношению к нормальному водородному электроду
- •Рыбалкин Евгений Михайлович Ковалик Ольга Юрьевна химия
- •654007, Г. Новокузнецк, ул. Кирова, 42
Коллоидные растворы
|
Коллоидные растворы (золи) – дисперсные системы занимающее промежуточное положение между истинными растворами и грубодисперсными системами. |
![]()
|
Методы получения | |
|
Диспергирование |
Конденсация |
|
Дробление крупных частиц до коллоидной дисперсности. |
Соединение атомов, ионов или молекул в более крупные частицы (агрегаты). |
Строение коллоидных частиц



























а грегат
грегат
я дро
дро
ч астица
астица
мицелла

|
Мицелла – это структурная коллоидная единица. |
|
Для золя AgI со стабилизатором AgNO3 формула мицеллы: {m [AgI] n Ag +(n–x)NO3–} xNO3– |
Приложение а Физико-химические постоянные
|
Постоянная Планка |
h = 6,626176·10–34 Дж·c |
|
Скорость света в вакууме |
с = 2,99792458·10 м·с–1 |
|
Гравитационная постоянная |
G = 6,6720·10–11 H·м2·кг–2 |
|
Атомная единица массы, а.е.м. |
mu ≈ 1,6605655·10–27 кг |
|
Масса покоя электрона |
me = 9,109534·10–31 кг |
|
Масса покоя протона |
mp = 1,6726485·10–27 кг |
|
Масса покоя нейтрона |
mп = 1,6749543·10–27 кг |
|
Элементарный электрический заряд |
е = 1,6021892·10–19 Кл |
|
Масса атома изотопа 1Н |
1Н = 1,673559·10–27 кг |
|
Масса атома изотопа 2Н(D) |
2Н(D) = 3,344548·10–27 кг |
|
Постоянная Авагадро |
NA = 6,022045·1023 моль–1 |
|
Постоянная Фарадея |
F = 9,648456·104 Кл/моль |
|
Универсальная газовая постоянная |
R = 8.31441 Дж/(К·моль) |
|
Постоянная Больцмана |
k = 1,380662·10–23 Дж/К |
|
Коэффициент перехода от массы к энергии |
931,5016 МэВ·(а.е.м.)–1 |
|
Нормальные физические условия | |
|
Нормальное атмосферное давление |
Р = 1,01325·105 Па = = 101,325 кПа = 760 мм рт. ст. |
|
Нормальная термодинамическая температура |
Т = 273,15 К t = 0 °C |
|
Молярный объем идеального газа при нормальных физических условиях |
Vм = 22,4 л/моль |
ПРИЛОЖЕНИЕ Б
Относительные электроотрицательности элементов
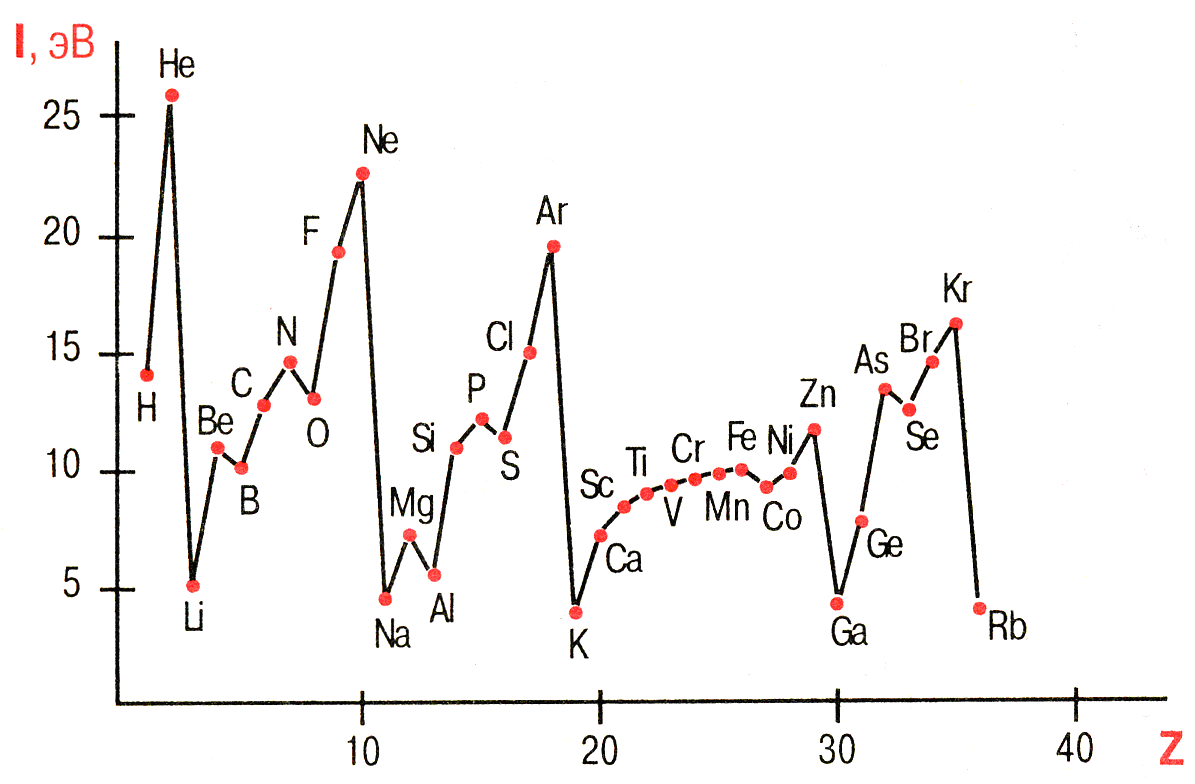

Изменение
энергии ионизации в зависимости от порядкового
номера
элемента
ПРИЛОЖЕНИЕ В. Периодическая система элементов Д.И. Менделеева
|
Периоды |
Ряды |
Г Р У П П Ы Э Л Е М Е Н Т О В | |||||||||||||||||||||||||
|
I |
II |
III |
IV |
V |
VI |
VII |
VIII | ||||||||||||||||||||
|
а б |
а б |
а б |
а б |
а б |
а б |
а б |
а |
б | |||||||||||||||||||
|
1 |
1 |
Н 1 Водород 1,008 |
1 |
|
U
92 2 9 21 32 18 8 2 Уран 238,03
Атомный
номер Распределение
электронов по уровням Атомная
масса |
Нe 2 Гелий 4,003 |
2 | ||||||||||||||||||||
|
2 |
2 |
Li 3 Литий 6,941 |
1 2 |
Be 4 Бериллий 9,0122 |
2 2 |
B 5 Бор 10,811 |
3 2 |
C 6 Углерод 12,011 |
4 2 |
N 7 Азот 14,007 |
5 2 |
O 8 Кислород 15,999 |
6 2 |
F 9 Фтор 18,998 |
7 2 |
Ne 10 Неон 20,179 |
8 2 | ||||||||||
|
3 |
3 |
Na 11 Натрий 22,99 |
1 8 2 |
Mg 12 Магний 24,305 |
2 8 2 |
Al 13 Алюминий 26,092 |
3 8 2 |
Si 14 Кремний 28,086 |
4 8 2 |
P 15 Фосфор 30,974 |
5 8 2 |
S 16 Сера 32,064 |
6 8 2 |
Cl 17 Хлор 35,453 |
7 8 2 |
Ar 18 Аргон 39,948 |
8 8 2 | ||||||||||
|
4 |
4 |
K 19 Калий 39,0983 |
1 8 8 2 |
Ca 20 Кальций 40,078 |
2 8 8 2 |
21 Sс Скандий 44,956 |
2 9 8 2 |
22 Ti Титан 47,956 |
2 10 8 2 |
23 V Ванадий 50,941 |
2 11 8 2 |
24 Cr Хром 51,996 |
1 13 8 2 |
25 Mn Марганец 54,938 |
2 13 8 2 |
26 Fe Железо 55,845 |
2 14 8 2 |
27 Co Кобальт 58,933 |
2 15 8 2 |
28 Ni Никель 58,6934 |
2 16 8 2 |
| |||||
|
5 |
29 Сu Медь 63,546 |
1 18 8 2 |
30 Zn Цинк 65,39 |
2 18 8 2 |
Ga 31 Галлий 69,72 |
3 18 8 2 |
Ge 32 Германий 72,59 |
4 18 8 2 |
As 33 Мышьяк 74,922 |
5 18 8 2 |
Se 34 Селен 78,96 |
6 18 8 2 |
Br 35 Бром 79,904 |
7 18 8 2 |
|
Kr 36 Криптон 83,8 |
8 18 8 2 | ||||||||||
|
5 |
6 |
Rb 37 Рубидий 85,468 |
1 8 18 8 2 |
Sr 38 Стронций 87,62 |
2 8 18 8 2 |
39 Y Иттрий 88,906 |
2 9 18 8 2 |
40 Zr Цирконий 91,22 |
2 10 18 8 2 |
41 Nb Ниобий 92,906 |
1 12 18 8 2 |
42 Mo Молибден 95,94 |
1 13 18 8 2 |
43 Tc Технеций [99] |
2 13 18 8 2 |
44 Ru Рутений 101,07 |
1 15 18 8 2 |
45 Rh Родий 102,906 |
1 16 18 8 2 |
46 Pd Палладий 106,42 |
0 18 18 8 2 |
| |||||
|
7 |
47 Ag Серебро 107,868 |
1 18 18 8 2 |
48 Cd Кадмий 112,41 |
2 18 18 8 2 |
In 49 Индий 114,82 |
3 18 18 8 2 |
Sn 50 Олово 118,69 |
4 18 18 8 2 |
Sb 51 Сурьма 121,75 |
5 18 18 8 2 |
Te 52 Теллур 127,6 |
6 18 18 8 2 |
I 53 Йод 126,905 |
7 18 18 8 2 |
|
Xe 54 Ксенон 131,3 |
8 18 18 8 2 | ||||||||||
|
6 |
8 |
Cs 55 Цезий 132,905 |
1 8 18 18 8 2 |
Ba 56 Барий 137,327 |
2 8 18 18 8 2 |
La57-Lu71 * |
72 Hf Гафний 178,49 |
2 10 32 18 8 2 |
73 Ta Тантал 180,948 |
2 11 32 18 8 2 |
74 W Вольфрам 183,85 |
2 12 32 18 8 2 |
75 Re Рений 186,207 |
2 13 32 18 8 2 |
76 Os Осмий 190,23 |
2 14 32 18 8 2 |
77 Ir Иридий 192,22 |
2 15 32 18 8 2 |
78 Pt Платина 195,08 |
1 17 32 18 8 2 |
| ||||||
|
9 |
79 Au Золото 196,967 |
1 18 32 18 8 2 |
80 Hg Ртуть 200,59 |
2 18 32 18 8 2 |
Tl 81 Таллий 204.37 |
3 18 32 18 8 2 |
Pb 82 Свинец 207,19 |
4 18 32 18 8 2 |
Bi 83 Висмут 208,98 |
5 18 32 18 8 2 |
Po 84 Полоний [210] |
6 18 32 18 8 2 |
At 85 Астат [210] |
7 18 32 18 8 2 |
|
Rn 86 Радон [222] |
8 18 32 18 8 2 | ||||||||||
|
7 |
10 |
Fr 87 Франций [223] |
1 8 18 32 18 8 2 |
Ra 88 Радий [226] |
2 8 18 32 18 8 2 |
Ac89-Lr103 ** |
104 Rf Резерфордий [261] |
2 10 32 32 18 8 2 |
105Db Дубний [262] |
2 11 32 32 18 8 2 |
106 Sg Сиборгий [263] |
2 12 32 32 18 8 2 |
107 Bh Борий [262] |
2 13 32 32 18 8 2 |
108Hn Хаccий [265] |
2 14 32 32 18 8 2 |
109 Mt Мейтнерий [266] |
2 15 32 32 18 8 2 |
110 (Uun) [271] |
2 16 32 32 18 8 2 |
| ||||||
Продолжение приложения В
|
Лантаноиды * |
La 57 Лантан 138, 91 |
2 8 18 18 8 2 |
Ce 58 Церий 140,12 |
2 8 18 18 8 2 |
Pr 59 Празеодим 140,91 |
2 8 18 18 8 2 |
Nd 60 Неодим 144,24 |
2 8 18 18 8 2 |
Pm 61 Прометий 144,91 |
2 8 18 18 8 2 |
Sm 62 Самарий 150,36 |
2 8 18 18 8 2 |
Eu 63 Европий 151,97 |
2 8 18 18 8 2 |
Gd 64 Гадолиний 157,25 |
2 8 18 18 8 2 |
|
Tb 65 Тербий 158,93 |
2 8 18 18 8 2 |
Dy 66 Диспрозий 162,50 |
2 8 18 18 8 2 |
Ho 67 Гольмий 164,93 |
2 8 18 18 8 2 |
Er 68 Эрбий 167,26 |
2 8 18 18 8 2 |
Tm 69 Тулий 168,93 |
2 8 18 18 8 2 |
Yb 70 Иттербий 173,04 |
2 8 18 18 8 2 |
Lu 71 Лютеций 174,97 |
2 8 18 18 8 2 |
|
| |
|
Актиноиды ** |
Ac 89 Атиний 227,03 |
2 8 32 32 18 8 2 |
Th 90 Торий 232,04 |
2 8 32 32 18 8 2 |
Pa 91 Протактиний 231,04 |
2 8 32 32 18 8 2 |
U 92 Уран 238,03 |
2 8 32 32 18 8 2 |
Np 93 Нептуний 237,05 |
2 8 32 32 18 8 2 |
Pu 94 Плутоний 244,06 |
2 8 32 32 18 8 2 |
Am 95 Америций 243,06 |
2 8 32 32 18 8 2 |
Cm 96 Кюрий 247,07 |
2 8 32 32 18 8 2 |
|
Bk 97 Берклий 247,07 |
2 8 32 32 18 8 2 |
Cf 98 Калифорний 251,08 |
2 8 32 32 18 8 2 |
Es 99 Эйнштейний 252,08 |
2 8 32 32 18 8 2 |
Fm 100 Фермий 257,10 |
2 8 32 32 18 8 2 |
Md 101 Менделевий 258,10 |
2 8 32 32 18 8 2 |
No 102 Нобелий 259,10 |
2 8 32 32 18 8 2 |
Lr 103 Лоуренсий 260,11 |
2 8 32 32 18 8 2 |
|
|




