- •Химия Учебное наглядное пособие
- •Содержание
- •Раздел 1. Основные понятия и законы химии
- •1.1. Атомно-молекулярное учение
- •1.2. Законы химии
- •Закон сохранения массы вещества
- •Способы выражения количества вещества эквивалентов
- •Раздел 2. Классификация неорганических веществ
- •2.1.Оксиды
- •Химические свойства оксидов
- •2.2. Гидроксиды металлов
- •Химические свойства гидроксидов
- •Доказательство амфотерности
- •2.3. Кислоты
- •2.4. Соли
- •Средние кислые основные
- •Получение солей
- •2.5. Комплексные соединения
- •Раздел 3. Растворы
- •3.1. Способы выражения концентрации растворов
- •3.2. Растворы неэлектролитов
- •3.3. Растворы электролитов. Электролитическая диссоциация
- •3.4. Ионно-молекулярные уравнения реакций
- •3.5. Гидролиз
- •Раздел 4. Элекрохимические системы
- •Законы Фарадея
- •4.1. Степень окисления
- •4.2. Окислительно-восстановительные реакции (овр)
- •Направление овр
- •4.3. Гальванический элемент Даниэля-Якоби
- •4.4. Электродвижущая сила (эдс)
- •Стандартный водородный электрод
- •4.5. Электролиз
- •Электролиз с инертным анодом
- •Электролиз с растворимым анодом
- •4.6. Коррозия и защита металлов от коррозии
- •Защита металлов от коррозии
- •Раздел 5. Периодический закон д.И.Менделеева
- •5.1. Строение атома
- •Состав ядра
- •5.2. Модель состояния электрона в атоме Квантовые числа
- •Возможные значения квантовых чисел
- •5.3.Основные положения строения электронных оболочек атома
- •Ряд последовательного заполнения электронами орбиталей
- •Раздел 6. Химическая связь
- •Раздел 7. Химическая кинетика и равновесие
- •Раздел 8. Химическая термодинамика
- •8.1. Параметры состояния системы
- •8.2. Закон Гесса
- •Раздел 9. Химия элементов
- •Углерод c
- •Физические свойства аллотропных модификаций c
- •Химические свойства с
- •Соединения с
- •Кремний Si
- •Соединения Si
- •Соединения n
- •Соли аммония
- •Особые химические свойства
- •Разложение нитратов: фосфор p
- •Соединения р
- •Халькогены
- •Кислород
- •Соединения s
- •Галогены f, Cl, Br, I хлор Cl2
- •Соединения Cl
- •Подгруппа хрома
- •Хром Cr
- •Подгруппа железа
- •Железо Fe
- •Раздел 10. Органическая химия
- •10.1.Углеводороды Предельные углеводороды. Алканы
- •Непредельные углеводороды. Алкены
- •Диеновые углеводороды
- •Ароматические углеводороды. Ряд бензола. Арены
- •Нефть и ее переработка
- •10.2. Кислородсодержащие органические соединения Спирты
- •Альдегиды
- •Формальдегид
- •Ацетальдегид
- •Поликонденсация
- •Кетоны r – c – r
- •Карбоновые кислоты
- •Определение строения веществ
- •11.1. Методы качественного анализа (реакции обнаружения) Окрашивание пламени (предварительная проба)
- •Реакции осаждения
- •Реакции с выделением газа
- •Качественный элементный анализ
- •Цветные реакции
- •Обнаружения газов
- •Реакции обнаружения органических соединений
- •Индентификация синтетических материалов
- •11.2. Методы количественного анализа Титриметрический анализ (объемный анализ)
- •Кондуктометрическое титрование
- •Потенциометрия
- •Окислительно-восстановительное титрование
- •Комплексонометрия
- •Осадительное титрование
- •Аргентометрия
- •Гравиметрия
- •11.3. Спектроскопические методы анализа
- •Ультрафиолетовая спектроскопия и абсорбционная спектроскопия в видимой области
- •Характерные инфракрасные полосы поглощения
- •Спектроскопия ядерного магнитного резонанса
- •11.4. Дифрактометрический метод анализа
- •Дифракция рентгеновых лучей для определения типа кристаллической решетки
- •Дифракция рентгеновых лучей для определения электронной плотности
- •Раздел 12. Химия окружающей среды Глобальные аспекты
- •Загрязнение окружающей среды
- •Охрана окружающей среды
- •Атмосфера как область окружающей среды
- •Загрязнение воздуха
- •Влияние вредных веществ на окружающую среду
- •Методы очистки воздуха
- •Гидросфера как область окружающей среды
- •Вредные примеси питьевой воды
- •Жёсткость воды
- •Сточные воды
- •Вредные вещества в сточных водах
- •Поступления сточных вод
- •Литосфера как область окружающей среды
- •Удобрения
- •Загрязнение стойкими биоцидами
- •Заражение ядовитыми тяжелыми металлами
- •Методы санации зараженных почв
- •Отходы в окружающей среде
- •Вторичное использование
- •Продовольствие и питание
- •Углеводы в качестве пищевого продукта
- •Жиры в качестве пищевого продукта
- •Протеины как продукт питания
- •Витамины
- •Минеральные вещества
- •Микроэлементы
- •Пищевые добавки
- •Консерванты
- •Раздел 13. Коллоидная химия
- •Адсорбция, ее виды
- •Дисперсные системы
- •Коллоидные растворы
- •Строение коллоидных частиц
- •Приложение а Физико-химические постоянные
- •Групповые названия химических элементов
- •Растворимость веществ в воде при температуре 25 °с
- •Эбуллиоскопические (Кэ) и криоскопические (Ккр) константы некоторых растворителей
- •Произведения растворимости некоторых малорастворимых электролитов при 25 °с
- •Возможные степени окисления элементов
- •Электронное строение атомов в основном состоянии
- •Стандартные термодинамические функции образования
- •Нормальные (стандартные) окислительно-восстановительные потенциалы е0 в водных растворах при 25 0с по отношению к нормальному водородному электроду
- •Рыбалкин Евгений Михайлович Ковалик Ольга Юрьевна химия
- •654007, Г. Новокузнецк, ул. Кирова, 42
Углерод c
|
В природе: 1) В свободном состоянии: алмаз, графит, карбин. 2) В ископаемых: каменный уголь, бурый уголь; природные карбонаты: CaCO3 – известняк, мел, мрамор; MgCO3 – магнезит; FeCO3 – железный шпат; MgCO3· CaCO3 – доломит. 3) В органических веществах. 4) В воздухе – CO2. |
Физические свойства аллотропных модификаций c
|
АЛМАЗ
sp3-гибридизация, тетраэдрические σ-связи, прочные ковалентные неполярные связи. Бесцветное кристаллическое вещество, очень твердое, плохо проводит тепло, не проводит ток. |
ГРАФИТ
sp2-гибридизация,
слоистая структура, большое расстояние
между слоями
|
КАРБИН С ≡ СС ≡ С sp-гибридизация, линейный полимер. Мелкий кристаллический порошок, черного цвета, более твердый, чем графит, полупроводник. |
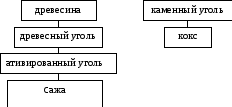
УГОЛЬ сухая
перегонка
Получение С
Адсорбция
–
свойство угля и других твердых или
жидких веществ удерживать на своей
поверхности пары, газы и растворенные
вещества.

Химические свойства с
|
С – окислитель |
С – восстановитель |
(карбид кальция)
|
2С + O2 = 2CO выше 900˚С
C+2H2O= CO2 + 2H2 ниже 1000˚С
|
Соединения с
|
Оксид углерода (II) :С=О: |
Оксид углерода (VI) O=С=О |
СО2 +С = 2СО
CO – восстановитель.
|
CaСО3 = CaO + СО2↑
CaСО3+2HCl=CaCl2+CO2↑+ H2O
бесцветный газ, тяжелее воздуха, не поддерживает дыхание; растворим в воде, при t = –76˚С – сухой лед.
а)
CO2
+ H2O б) CO2 + 2NaOH = Na2CO3 + H2O 2) CO2 – окислитель а) CO2 + С = 2СО б) CO2 + 2Mg = 2MgO + C IV. Применение: в производстве соды, сахара, газированных напитков; в жидком виде – в огнетушителях; сухой лед – для хранения продуктов.
|
|
Угольная кислота H2CO3 | |
|
Существует только в растворе, в свободном виде не устойчив, слабый электролит. H2CO3 = CO2↑ + 2H2О – при нагревании Диссоциация: H2CO3
|
|
Соли угольной кислоты | |
|
Карбонаты |
Гидрокарбонаты |
|
Карбонаты
щелочных металлов и
CaCO3 |
Гидрокарбонаты
щелочных, щелочноземельных металлов
и
Получение: CaCO3+ СО2 + Н2О = Ca(НCO3)2 Ca(НCO3)2 |
|
Na2CO3 – карбонат натрия: белый порошок; используется в производстве стекла, мыла, бумаги, моющих средств. K2CO3 – поташ: белый порошок; используется в производстве жидкого мыла, оптического стекла пигментов. СaCO3 – мел, мрамор, известняк; используется в строительстве. |
NaНCO3 – гидрокарбонат натрия или питьевая сода: белый порошок, плохо растворяется в воде; используется в пищевой промышленности, медицине. |
|
Качественная реакция на карбонат-ион:
Ca(OH)2 + СО2 = CaCO3↓ + Н2О – раствор мутнеет 3) при избытке СО2: CaCO3+СО2+Н2О=Ca(НCO3)2 – помутнение исчезает. |