
- •2 Трансаминирование аминокислот
- •Палф памф.
- •3 Дезаминирование аминокислот. Непрямое дезамини–рование
- •4 Декарбоксилирование аминокислот
- •5 Обмен аммиака. Биосинтез мочевины. Некоторые клинические аспекты
- •Генетические дефекты ферментов синтеза мочевины
- •Лекция 2
- •Фумарат
- •Сукцинил-КоА
- •2 Метаболизм глицина и серина
- •3 Метаболизм серусодержащих аминокислот. Синтез креатина
- •4 Метаболизм аминокислоты с разветвленной цепью
- •Вал, Иле, Мет
- •5 Метаболизм циклических аминокислот - фенилала–нина, тирозина, триптофана и гистидина
- •6 Наследственные нарушения обмена аминокислот
- •Тема. Метаболизм нуклеотидов План
- •2 Адф гдф
- •Регуляция синтеза пуриновых нуклеотидов
- •4 Биосинтез дезоксирибонуклеотидов
- •Список литературы
- •Гребеник л.И., Высоцкий и.Ю.
- •Ббк 28.072.511.1
- •Isbn 966-657-105-6
- •“Метаболизм аминокислот
- •И нуклеотидов”
- •Для студентов специальности 7.110101
- •Дневной формы обучения
2 Адф гдф

 АТФ
АТФ
АДФ
АТФ ГТФ
Регуляция синтеза пуриновых нуклеотидов
Синтез пуриновых нуклеотидов регулируется ключевыми ферментами, активность которых зависит от концентрации конечных и некоторых промежуточных продуктов, т.е. при контроле синтеза реализуется один из механизмов - регуляция по принципу отрицательной обратной связи:
1) АТФ, ГМФ ингибируют образование ФРПФ (угнетают активность 5–фосфорибозил–1–пирофосфатсинтазы);
2) ИМФ, АМФ, ГМФ – ингибируют образование фосфорибозиламина - это наиболее важный пункт контроля (угнетают активность глутамин–ФРПФ–амидотрансферазы);
3) АМФ ингибирует образование аденилосукцината, который является промежуточным продуктом его синтеза, а ГМФ - ксантинмонофосфата;
АМФ ингибирует образование ксантинмонофосфата при синтезе ГМФ, а ГМФ, в свою очередь, угнетает образование аденилосукцината, который является промежуточным продуктом синтеза АМФ. Т.о. изменения концентрации АМФ влияют на синтез ГМФ и наоборот;
АТФ может активировать процессы синтеза ГМФ также на этапе образования ксантинмонофосфата, а ГТФ - активировать образование аденилосукцината.
Указанные механизмы изображены на схеме, иллюстрирующей превращение ИМФ в АМФ и ГМФ (см. выше).
В клетках организма существует механизм синтеза нуклеотидов, которые обеспечивают повторное использование пуриновых азотистых оснований – это путь реутилизации, или «путь спасения» азотистых оснований.
Основные ферменты, участвующие в этих процессах:
1) аденинфосфорибозилтрансфераза, катализирует реакцию:
Аденин + ФРПФ АМФ + ФФ;
2) гипоксантин-гуанинфосфорибозилтрансфераза, катализирует реакции:
гуанин + ФРПФ ГМФ + ФФн,
гипоксантин + ФРПФ ИМФ + ФФн.
3 Биосинтез пиримидиновых нуклеотидов: реакции, регуляция, нарушение процесса
В отличие от последовательности реакций синтеза пуриновых нуклеотидов denovoсинтез пиримидиновых нуклеотидов начинается со сборки кольца азотистого основания, которое затем присоединяется к рибозо-5-фосфату. Донором рибозо-5-фосфата является ФРПФ. Предшественниками пиримидинового кольца служат карбамоилфосфат и аспартат.
Синтез начинается с образования карбамоилфосфата, который синтезируется в цитозоле (в отличие от карбомаилфосфата для биосинтеза мочевины, образование которого происходит в митохондриях). Донором азота при синтезе карбомаилфосфата является глутамин (а не NH+4). Реакцию катализируеткарбомаилфосфатсинтаза ІІ:
Глутамин + 2 АТФ + СО2
карбамоилфосфат + 2 АДФ + Фн+ глутамат.
Следующий этап – образование N–карбамоиласпартата
(фермент – аспартат–карбамоилтрансфераза – АТКаза)
H
 2N-CО-O-PO3H2
+ H2N-CH-COOH
H2N-CО-NH-CH-
СООН
2N-CО-O-PO3H2
+ H2N-CH-COOH
H2N-CО-NH-CH-
СООН
к арбамоилфосфат
- Фн
арбамоилфосфат
- Фн

 CH2
CH2
CH2
CH2
COOH COOH
аспартат N–карбамоиласпартата
В следующей последовательности реакций образуется предшественник всех пиримидиновых нуклеотидов - УМФ:
 Н2О
Н2О
N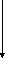
 –карбамоиласпартат
Дигидрооротат
–карбамоиласпартат
Дигидрооротат
дигидрооротаза
 дигидро–
дигидро–
НАД оротат–
НАДН++ Н дегидроге–
наза
Оротат
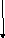
 ФРПФоротат–
ФРПФоротат–
фосфо–
ФФ н рибозил–
транс–
фераза
ОМФ
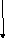
 оротидилат–
оротидилат–
Н+ декарбокси–
СО2 лаза
УМФ
С участием молекул АТФ под действием специфичес–ких киназ (УМФ–киназа, нуклеозид–фосфаткиназа) УМФ превращается в УТФ.
УТФ служит предшественником ЦТФ:
глутамин + глутамат +
АТФ + Н2О АДФ + Фн+ 2Н+

У ТФЦТФ
ТФЦТФ
Регуляция синтеза пуриновых нуклеотидов
Ключевыми ферментами процесса являются карбамоилфосфатсинтаза II(1) и АТКаза (2), схема регуляции которых изображена ниже:
(1)

С
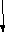 О2
+ глутамин + 2АТФ карбамоилфосфат
О2
+ глутамин + 2АТФ карбамоилфосфат
 аспартат
аспартат
УМФ, УТФ (2) ЦТФ
 карбамоиласпартат
карбамоиласпартат

 УМФ
УМФ
У ТФ
ТФ
ЦТФ
В регуляции 2 реакция – решающий этап. ЦТФ значительно снижает сродство фермента АТКазы к субстрату (степень ингибирования до 90%). Активация этого фермента происходит под действием АТФ, что позволяет координировать скорости образования пуринов и пиримидинов.
Известна наследственная патология, при которой нарушается синтез пиримидиновых нуклеотидов - это оротацидурия.Болезнь связана с недостаточностью ферментов, которые катализируют образование и декарбоксилирование оротовой кислоты при синтезе УМФ (две последние реакции синтеза) -оротатфосфорибозил–трансферазыиОМФ-декарбоксилазы. В результате наблюдается дефицит пиримидиновых нуклеотидов, в крови повышается концентрация оротовой кислоты, которая выводится с мочей. Образование оротовой кислоты при этом заболевании усилено, так как нет аллостерических ингибиторов синтеза - конечных продуктов - УМФ и УТФ. Лечение необходимо, так как может развиваться отставание в умственном или физическом развитии, тяжелая мегалобластическая анемия, резистентность к витаминам, лейкопения, иммунодефицит. Эти нарушения являются следствием «пиримидинового голода», а не токсического действия оротовой кислоты. Для лечения применяют уридин в дозах 0,5 - 1г в сутки. Такая терапия устраняет «пиримидиновый голод» и продолжается без перерывов на протяжении всей жизни.
Оротатацидурияможет также развиваться на начальных этапах лечения подагры аллопуринолом. Этот препарат в организме частично превращается в сильный ингибитор декарбоксилазы оротовой кислоты, вследствие чего происходит временное усиление образования оротовой кислоты.
