
- •Конспект лекций
- •Лекция 1
- •Основные определения
- •Лекция 2
- •Лекция 3
- •Лекция 4
- •Теплотворная способность
- •Добыча, потребление и значение ископаемого топлива
- •Лекция 5
- •Лекция 6
- •Классификация вв
- •Физико-химические характеристики вв Консистенция и структура
- •Физическая стабильность вв
- •Реакции взрывчатого превращения
- •Лекция 7
- •4.2. Общие сведения о взрывчатых веществах
- •Лекция 8
- •Физико-химические характеристики вв
- •Классификация вв
- •Инициирующие вв
- •Бризантные вв
- •Бризантные вв повышенной мощности
- •Лекция 9
- •Нитроглицериновые вв нормальной мощности
- •Вв, находящееся в стадии исследований
- •Жидкие вв и жидкие смесевые вв
- •Вв жидкие смеси
- •Оксиликвиты
- •Суррогатные вв
- •Лекция 10
- •Взрывная волна
- •Лекция 11
- •Лекция 12
- •Лекция 13
- •Лекция 14
- •Если нельзя применять диоксид углерода (например, при горении металлов
- •Лекция 15
- •Лекция 16
- •Лекция 17
- •Строительные материалы. Строительные конструкции. Сравнительная оценка пожарной опасности лакокрасочных покрытий. Эвакуация людей при пожаре
- •Библиографический список рекомендуемой литературы
Лекция 4
ПРОИСХОЖДЕНИЕ ГАЗА И НЕФТИ. ПРОИСХОЖДЕНИЕ ИСКОПАЕМЫХ ТВЁРДЫХ ТОПЛИВ. СОСТАВ ТОПЛИВА. ОСНОВНЫЕ ТЕХНИЧЕСКИЕ ХАРАКТЕРИСТИКИ ТОПЛИВА. ТЕПЛОПРОИЗВОДИТЕЛЬНОСТЬ ТОПЛИВА. ТЕПЛОТВОРНАЯ СПОСОБНОСТЬ
Существует несколько теорий происхождения нефти и газа. Их можно разбить на 2 группы:
– теории минерального происхождения,
– теории органического происхождения.
По теории минерального происхождения нефть произошла в результате воздействия морской воды на минералы под воздействием высоких температур и давления образовались первоначально газообразные продукты, далее под действием t и P и катализаторов происходило уплотнение газообразных углеводородных продуктов и образование сложных углеводородных соединений нефти.
Основную массу нефти составляют углеводороды различных классов – предельные, непредельные, ароматические.
Более признанной является теория органического происхождения нефти и газа. Согласно этой теории нефть и газ образовались вследствие скопления и последующего разложения животных организмов в условиях высоких t и P без доступа воздуха. Однако проблематичным является сама возможность скопления в громадных количествах трупов животных.
Наиболее популярной теорией является теория смешанного происхождения нефти и газа, согласно которой в образовании их принимали участие и растительные и животные остатки. Эти остатки вначале превращались в их и далее под воздействием t и P → смолы → сложные углеводородные соединения → другие смеси.
Протекающие химические и биохимические процессы, связанные с деятельностью бактерий и приводило к образованию газообразных продуктов – H, CH4 и др. Далее при наличии t и P, воздействия среды происходили реакции между H и органическими остатками, т.е. происходили процессы гидротенизации т.е. обогащения органики водородом, далее образование сложных смесей углеводородов а так же H2O, H2S, NH4 и далее различных типов жидких и газообразных CH-соединений. То есть характер и состав нефти и газа определяется не только средой, где происходило их образование, но и составом первичных исходных продуктов растительного и животного происхождения.
Естественные, или природные газы делятся на:
– природные, добытые из газовых месторождений,
– попутные, добываемые попутно у месторождений нефти.
Среди природных газов различают сухие – содержащие 95-99% CH4 и жирные, содержащие также его гомологи – этан, пропан, бутан.
Как правило, все попутные газы относятся к жирным.
Все виды природных топлив (кроме древесины) представляют собой горючие ископаемые – т.е. горные породы органического происхождения – каустобиолиты, которые подразделяют на: гумусовые породы (торф, каменные и бурые угли); сапропелевые породы (сапропелевые угли, горючие сланцы); петролиты (нефть, озокерит, горючие газы).
Состав топлива. Основные технические характеристики топлива
С остав
топлива – наиболее важная техническая
характеристика, определяющая процесс
горения и количество выделяющейся при
этом энергии.
остав
топлива – наиболее важная техническая
характеристика, определяющая процесс
горения и количество выделяющейся при
этом энергии.
Основные топливообразователи – СГ, НГ, ОГ Состав горючей массы.
В небольших количествах – SГ и NГПроцентное содержание
этих веществ по отношению
к горючей массе
Углерод С – основная составная часть топлива ( в горючей массе различных топлив С от 50 до 95%), при полном сгорании 1 кг. С выделяется 8100 ккал тепла. При большем содержании С повышается выделение тепла но затруднено воспламенение.
Водород Н – наиболее теплотворная составляющая ( в горючей массе различных топлив Н от 2 до 15%), %), при полном сгорании 1 кг. Н выделяется 30000 ккал. Часть водорода уже соединена с кислородом топлива и участия в горении не принимает.
Кислород О является вредной составной частью топлива, не является горючей частью топлива, участия в горении не принимает, ( в горючей массе различных топлив О от 0.05% -бензин до 42% - дрова).
Азот N также не участвует в горении (внутренний балласт) и выделяется из топлива при горении в чистом виде в дымовых газах, (содержание N в твердых и жидких топливах от 0.5% до 2.7%). Большие содержания азота в генераторных газах резко снижают тепловыделения.
Сера S содержится в топливе в виде пиритной серы (горючая), органической серы (горючая) и сульфатной серы (не горючая, выпадает с золой и шлаками).
Все эти компоненты составляют горючую массу топлива, им присваивается индекс. Процентное содержание в топливе всех веществ (включая золу), входящих в состав одной сухой массы, называют элементарным составом сухой масс (индекс СС).
СС + НС + ОС + NС + SС + АС = 100 %
Минеральные примеси, попадающие в состав топлива, составляют золу топлива (А). Зола не принимает участия в реакции окисления (горении, снижает теплотворную способность топлива.
Во всех топливах имеется некоторое количество влаги (W).
Общая масса топлива, включая золу и влагу, называется рабочей (индекс Р)
СР + НР + ОР + NР + SР + АР + WР = 100 %
Состав горючих газов характеризуется чаще всего в виде процентов объемного содержания составляющих газов, например,
СО + Н2 + СО2 + Н2О + СН4 + СnНm + О2 = 100 %
Тепловую ценность топлива принято характеризовать его теплотворной способностью Q, выражаемой в ккал/кг (Дж/кг) или ккал/м3 (дж/м3).
Т.к. в продуктах
сгорания топлив всегда содержится вода
(пары воды – из-за наличия воды в топливе
и образовании воды при сгорании водорода),
то и обращается энергия на парообразование
и конденсацию паров. В связи с этим для
расчетов обычно применяется значение
низшей теплотворной способности
![]() ,
которая учитывает тепловые потери с
парами воды.
,
которая учитывает тепловые потери с
парами воды.
Одной из основных особенностей твердых природных топлив (также древесины, композиций) является способность выделять при нагревании газообразные и жидкие продукты термического разложения их органической массы, так называемые летучие, обозначаются символом V.
Летучие играют значительную роль при воспламенении и на начальных стадиях горения, в значительной степени определяют реакционную способность горючего вещества.
Пример иллюстрации среднего состава природного топлива.
|
Топливо |
VГ,% |
СГ, % |
НГ ,% |
ОГ ,% |
NГ,% |
SГ,% |
АС ,% |
|
WР,% |
|
Древесина |
85 |
51 |
6 |
43 |
|
|
|
4500 |
|
|
Торф |
70 |
55-60 |
5-6 |
35-40 |
|
|
|
4800-6000 |
|
|
Бурый уголь |
45-55 |
65-75 |
5-5.5 |
18-25 |
|
|
30-50 |
5000-7000 |
|
|
Каменный уголь |
15-45 |
78-93 |
4-5.5 |
4-15 |
|
|
|
7500-8800 |
|
|
Антрациты |
5-10 |
93-97 |
1-2 |
1-2 |
|
|
|
8200-8300 |
|
|
Углерод |
0 |
100 |
- |
|
|
|
|
8100 |
|
Теплопроизводительность топлива
Теплопроизводительность топлива органического происхождения определяется в основном степенью окисления углеродной основы топлива.
Чем больше степень окисления углеводородной основы топлива, тем меньше теплопроизводительность.
Наибольшая теплопроизводительность наблюдается у топлива, состоящего из не окисленных углеводородов, например, у нефти, природного газа.
В качестве примера рассмотрим молекулу метана, составляющего основу природного газа, СН4.
Один атом С связан, т.е. весовое содержание водорода в молекуле метана составляет 25 %, т.е. ни один углеводородный продукт не содержит в себе такого большого количества водорода. При этом следует иметь в виду, что водород по своей теплотворной способности выше углерода в 4 ряда. Т.о. метан имеет самую высокую теплотворную способность, которая составляет 13300 ккал/кг.
Химически формула метилового спирта – СН4О. В момент такого окисления уже выделилось некоторое количество энергии, теплотворная способность спирта метилового – 5340 ккал/кг.
Присоединение еще одного атома кислорода приводит к образованию нового вещества – формальдегида – СН2О + Н2О, при этом происходит отделение одной молекулы воды.
Теплотворная способность формальдегида – 2790 ккал/кг.
Если к молекуле метана прибавить 4 атома кислорода, то это разбивает молекулу СН4
СН4 + 4О СО2 + 2Н2О
Такая смесь вообще гореть не может, и ее теплотворная способность равна 0.
Падение теплотворной способности от наивысшего значения у чистого углерода до нулевого значения у продуктов полного окисления и иллюстрируется на рисунке 1.
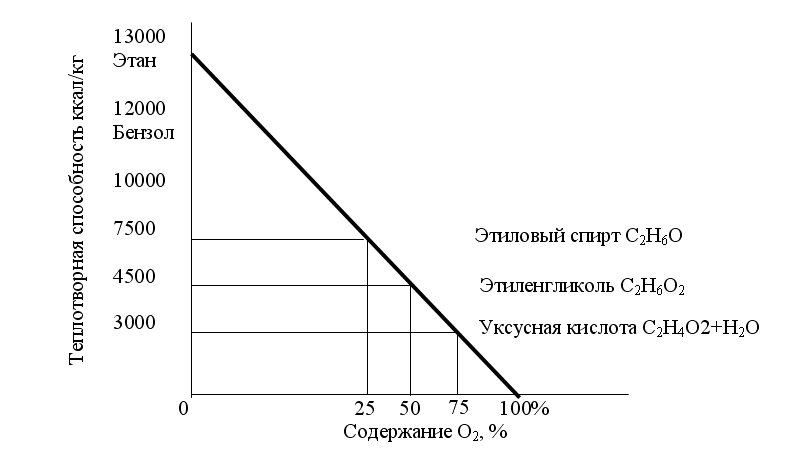
Рисунок 1 - Случай последовательного окисления этана – С2Н6.
